Lexikon der Biologie: B-Zell-Entwicklung
B-Zell-Entwicklung, beschreibt den Entwicklungsweg der B-Lymphocyten von hämatopoetischen Stammzellen über reife immunkompetente B-Zellen zu Antikörper-produzierenden Plasmazellen. Die B-Zell-Entwicklung verläuft in zwei Abschnitten. Der erste, antigenunabhängige Abschnitt umfaßt die Bildung und die Überprüfung funktioneller B-Zellen. Er findet bei Säugern in der fetalen Leber und später im Knochenmark statt. Der zweite Abschnitt beschreibt die Differenzierungsschritte, die durch eine Aktivierung der B-Zellen in der Peripherie durch die Bindung von Fremd-Antigenen ausgelöst werden. Das in beiden Abschnitten entscheidende Element ist der B-Zell-Rezeptor. Seine Funktionsfähigkeit ist, in Kombination mit der richtigen Mikroumgebung und den richtigen Wachstumsfaktoren, Voraussetzung für das Erreichen der jeweils nächsten Entwicklungsstufe.
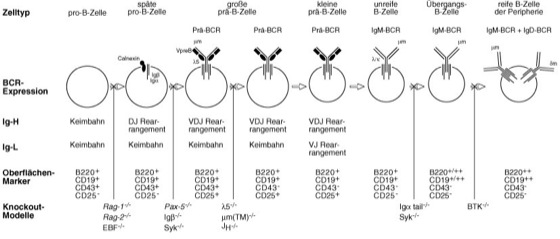
Die erste Zellpopulation innerhalb des Knochenmarks, die eindeutig der B-Zell-Entwicklungslinie zuzuordnen ist, sind die pro-B-Zellen (vgl. Abb.). Sie entstehen aus lymphoiden Vorläuferzellen des hämatopoetischen Systems (Blutbildung) und exprimieren bereits die B-Zellmarker CD19 und die CD45-Isoform B220 (CD-Marker). Weitere wichtige Marker sind CD43 und CD25, die eine Unterscheidung verschiedener Entwicklungsstadien erlauben. In diesem Stadium beginnen die Zellen mit der Umlagerung von Gensegmenten auf einem Allel des Immunglobulin-(Ig-) schwere-Kette-Locus (Immunglobulin-Gene, Immunglobulin-Gen-Rearrangement). Dabei findet zunächst eine Verknüpfung eines D- mit einem J-Segment und dann eine V-zu-DJ-Verknüpfung statt. Führt dieser Vorgang zur Bildung eines durchgehenden Leserasters für die Ig-schwere Kette, so erreicht die Zelle das prä-B-Zell-Stadium. Sie trägt nun einen prä-B-Zell-Rezeptor auf der Oberfläche, der von der Ig-schweren Kette, den Ersatz-leichten Ketten λ5 und VpreB sowie den signalleitenden Untereinheiten Igα und Igβ gebildet wird. Das Erscheinen des prä-B-Zell-Rezeptors markiert den ersten Selektionspunkt in der B-Zell-Entwicklung. Er übermittelt der Zelle ein positives Signal, das sie zum Eintritt in den Zellzyklus und zur Durchführung von ca. 6 Zellteilungen bewegt (große, teilende prä-B-Zelle). Kann er z. B. aufgrund eines fehlerhaften Immunglobulin-Gen-Rearrangements nicht exprimiert werden, so wird das Rearrangement auf dem zweiten Allel wiederholt (alleler Ausschluß). Mißlingt auch dies, so leitet die Zelle ein Apoptose-Programm (Apoptose) ein und stirbt. Im Erfolgsfall beginnt die prä-B-Zelle nun mit dem Rearrangement des Ig-leichte-Ketten-Locus (kleine, ruhende prä-B-Zelle). Dabei werden zunächst die Gensegmente des Igκ-Locus verknüpft, bevor bei Nichtgelingen die Segmente des Igλ-Locus benutzt werden. Insgesamt ist die Bildung eines Ig-leichte-Ketten-Gens jedoch fast immer erfolgreich. Die nun gebildete Ig-leichte-Kette paart mit der Ig-schweren-Kette, so daß es nun erstmals zur Oberflächenexpression eines B-Zell-Rezeptors kommt (Immunglobulin-Synthese). Die jetzt unreifen B-Zellen durchlaufen aufgrund der Spezifität ihres Rezeptors eine negative Selektion (Clone-selection-Theorie; Burnet). Zellen, die einen autoreaktiven B-Zell-Rezeptor exprimieren, werden unschädlich gemacht. In Abhängigkeit von der Affinität zum Autoantigen geschieht dies entweder durch Apoptose, oder aber die Zellen werden erneut zur Rekombination ihrer Immunglobulin-Gene veranlaßt. Nur etwa 10% der täglich generierten 107 unreifen B-Zellen ereichen bei der Maus nach der negativen Selektion das periphere lymphatische System. Mit dem Verlassen des Knochenmarks beginnen die B-Zellen über alternatives Spleißen mit der Expression von B-Zell-Rezeptoren der Klasse IgD gemeinsam mit IgM-B-Zell-Rezeptoren. In diesem Stadium (Übergangs-B-Zelle, IgM+++IgD+) findet vermutlich nochmals eine Negativ-Selektion gegen Autoantigene der Peripherie statt. Das naive B-Zell-Repertoire wird letztendlich von reifen, IgM+/IgD+++-B-Zellen gebildet. Alle weiteren Differenzierungsschritte sind nun abhängig vom Kontakt mit Fremdantigen. Treffen die B-Zellen auf ihrem Weg zwischen Blut, Lymphe und sekundären lymphatischen Organen (Lymphocyten-Rezirkulation) nicht innerhalb von ca. 3 Tagen auf ein passendes Antigen, so sterben sie in der Regel ab. Einige B-Zellen scheinen ihre Lebensdauer jedoch über Interaktionen mit follikulären dendritischen Zellen in den Follikeln der sekundären lymphatischen Organe verlängern zu können. Bindet eine reife B-Zelle nun über ihre B-Zell-Rezeptoren an ein passendes Antigen, so wird sie über intrazelluläre Signalkaskaden aktiviert (Lymphocyten-Aktivierung) und zur Proliferation und weiteren Differenzierung angeregt. In Abhängigkeit von der Form des Antigens differenziert die B-Zelle nun direkt zu einer Antikörper-sezernierenden Plasmazelle aus (Thymus-unabhängige Antigene), oder sie benötigt für diesen Schritt die Interaktion mit T-Lymphocyten (Thymus-abhängige Antigene). Die T-B-Lymphocyt-Kollaboration findet in besonderen Bereichen der lymphatischen Organe, den Keimzentren (Keimzentrum), statt. Die B-Zellen werden hier über Kontakte mit T-Lymphocyten und mit von diesen gebildeten Cytokinen zu starker Proliferation angeregt. Darüber hinaus kommt es über chromosomale Umlagerungen zu einem Wechsel der Immunglobulin-Isotypen (Klassensprung), so daß jetzt unter Beibehaltung der ursprünglichen Rezeptorspezifität auch Immunglobuline der Klassen IgG, IgE oder IgA gebildet werden können. Ein wesentliches Merkmal von B-Zellen, die eine solche Keimzentrums-Reaktion (Keimzentrum) durchlaufen haben, ist eine erhöhte Affinität ihrer B-Zell-Rezeptoren gegen das auslösende Antigen. Dies wird durch somatische Mutation und den Prozeß der Affinitätsreifung erreicht. Dabei werden Punktmutationen in die DNA-Bereiche eingeführt, die für die Antigen-Bindestellen der Immunglobuline codieren. Über erneute Selektionsprozesse wird dabei sichergestellt, daß tatsächlich nur höher affine und nicht etwa nun autoreaktive B-Zellen an der weiteren Immunantwort teilnehmen. Unter Umständen kann hier sogar noch ein erneutes Rearrangement der Immunglobulin-leichte-Kette-Gene stattfinden (editing), wenn die somatische Mutation zur Autoreaktivität geführt hat. Diejenigen B-Zellen, die Antigene erfolgreich gebunden und die Selektion überlebt haben, verlassen die Keimzentren, um entweder B-Gedächtniszellen oder antikörpersezernierende Plasmazellen zu werden. Es ist bislang nicht bekannt, welche Faktoren diese Differenzierungsentscheidung beeinflussen. Als Plasmazelle entwickelt die B-Zelle ein stark ausgeprägtes rauhes endoplasmatisches Reticulum, in dem große Mengen von nun sezernierten Immunglobulinen gebildet werden. Die meisten Plasmazellen besitzen eine begrenzte Lebenszeit von ca. 4 Wochen, während derer sie sich vor allem in den Lymphknoten, der Milz und dem Knochenmark aufhalten. Neuere Forschungen belegen jedoch die Existenz auch langlebiger Plasmazellen im Knochenmark. Diese sorgen nach einer Erstinfektion über längere Zeit für einen konstanten Antikörper-Titer im Blut und tragen so zum immunologischen Gedächtnis bei. Die Gedächtniszellen weisen keine morphologischen Besonderheiten auf. Sie tragen meist B-Zell-Rezeptoren der Klasse IgG, haben also einen Klassenwechsel durchgeführt. Funktionell sind sie jedoch von naiven B-Zellen (naive Lymphocyten) durch eine deutlich schnellere und stärkere Stimulation bei erneutem Antigen-Kontakt zu unterscheiden. Die dann von ihnen gebildeten Antikörper weisen aufgrund der Affinitätsreifung darüber hinaus auch höhere Affinitäten gegen das Antigen auf.
Die meisten Erkenntnisse über den Entwicklungsweg von B-Zellen sind aus Studien von sogenannten Knockout-Mäusen gewonnen worden (vgl. Abb.). Das Inaktivieren von Genen für Rekombinationsenzyme (RAG1, RAG2), Transkriptionsfaktoren (Pax-5, EBF), B-Zell-Rezeptor-Untereinheiten (Igβ, Igα, λ5, μm) oder signalleitende Elemente in der B-Zell-Stimulation (Syk, BTK) führt dabei zu einem Block der weiteren Entwicklung in Mäusen. Patienten mit X-gekoppelter-Agammaglobulinämie (XLA) weisen zwar, ausgelöst durch einen Defekt im Gen für die Tyrosin-Kinase BTK, eine erhöhte Anzahl an prä-B-Zellen auf, können jedoch keine reifen B-Zellen entwickeln. Interessanterweise erfolgt die B-Zell-Entwicklung bei einigen Spezies nach einem anderen Muster. Bei Vögeln und Kaninchen entsteht die Rezeptor-Diversität z. B. nicht durch Gen-Rearrangement, sondern wird erst nach der Expression eines für alle ähnlichen B-Zell-Rezeptors über Genkonversion in der Bursa Fabricii bzw. dem Bursa-Äquivalent erreicht. Blutbildung .
O.L.
Schreiben Sie uns!