Lexikon der Biologie: Hormone
Hormone [von *hormon- ], von anderen Wirkstoffen nicht streng zu trennende Gruppe von Substanzen im Tier- und Pflanzenreich (Phytohormone), die bei Tier und Mensch – häufig in spezifischen endokrinen Drüsen (Hormondrüsen; vgl. Tab. 1 ) gebildet (glanduläre Hormone) – in sehr niedrigen Konzentrationen ins Blut oder in die Hämolymphe abgegeben werden und an Organen, die über entsprechende Rezeptoren (Hormonrezeptoren) verfügen, spezifische Wirkungen entfachen. Werden Hormone nicht in spezialisierten Drüsen gebildet, sondern in einzelnen Zellen (Darmwand, Niere), bezeichnet man sie als Gewebshormone oder Zellhormone (aglanduläre Hormone), wobei die letztere Bezeichnung, die auf die Bildungsstätte der Hormone abhebt, die zutreffendere ist. Sie wirken dann im Gegensatz zu den Hormonen i.e.S. oft direkt in der Nachbarschaft ihres Produktionsorts im „Gewebe“. Dieser Sekretionsmechanismus wird als parakrin bezeichnet. Wirkt das Hormon auf die synthetisierende Zelle selbst, handelt es sich um einen autokrinen Mechanismus. Endokrine Hormone hingegen (z.B. Sekretin, Cholecystokinin des Zwölffingerdarms) wirken als „echte“ Hormone auf weiter entfernte Organe (in diesem Fall Pankreas und Galle), so daß die Bezeichnung „Gewebshormone“ unscharf ist. Die Freisetzung von Hormonen erfolgt – abgesehen von einer Basalsekretion – ereignisgesteuert oder in regelmäßigen, pulsatilen Rhythmen. Die Frequenz dieser Rhythmen (Chronobiologie) kann im Bereich von Minuten (z.B. Insulin) oder Stunden (z.B. gonadotrope Hormone) liegen oder circadianen (z.B. Cortisol), monatlichen (z.B. Menstruationszyklus) oder jahreszeitlichen Schwankungen (z.B. Hormone zur Fortpflanzung; Sexualhormone) unterliegen. Für viele Hormone kann die Freisetzungsrate auch über die Lebenszeit stark variieren (z.B. Testosteron). Die pulsatile Freisetzung kann durch eine ereignisgesteuerte überlagert werden. Die Freisetzung von Peptidhormonen ( vgl. Tab. 2 ) erfolgt meist als Prä-Pro-Hormon (Prä-Pro-Proteine) oder als Prohormon, welches noch durch Glykosylierung, Phosphorylierung, Acetylierung und/oder Amidierung prozessiert werden muß. Diese Prozessierung findet teilweise erst gewebespezifisch in der Zielzelle statt. Auch Steroidhormone werden am Ort ihrer Wirkung unterschiedlich modifiziert. – Obwohl endokrine Drüsen, deren Tätigkeit C. Bernard (1855) als innere Sekretion (Innersekretion) beschrieb, schon seit Jahrhunderten bekannt waren, gelang erst 1849 der eindeutige Nachweis ihrer Hormonwirkung durch A. Berthold, der kastrierten Hähnen Hoden einpflanzte und damit bei ihnen normales sexuelles Verhalten sowie Ausbildung sekundärer Geschlechtsmerkmale auslösen konnte. Die Bezeichnung Hormone stammt von E.H. Starling (1905; Bayliss), der sie erstmalig für das Sekretin verwendete. – Der Metazoenorganismus verfügt über 2 verschiedene Informationssysteme: eines, in dem Sender und Empfänger direkt verschaltet sind (neuronale Koordination; Nervensystem), und eines, in dem nur spezielle Empfänger eine „an alle“ gerichtete Information empfangen können (humorale Koordination; Hormon- und Immunsystem). (Telefon und Rundfunkempfänger verdeutlichen in der Technik das Prinzip.) Da jedoch auch bei der neuronalen Koordination Wirkstoffe (als Neurotransmitter) eine Rolle spielen und diese darüber hinaus teilweise Hormonwirkung (Neurohormone) besitzen (z.B. Adrenalin und Noradrenalin) und fernerhin nervöse Zentren über Blut- oder Hämolymphbahnen in Kontakt mit endokrinen Drüsen treten können (hypothalamisch-hypophysäres System, Neurohämalorgane), kann von einer strikten Trennung beider Informationssysteme nicht die Rede sein. Im Gegenteil weist die enge Verknüpfung auf eine gemeinsame phylogenetische Wurzel hin. Ebenfalls von Nervenzellen gebildet und funktionell zwischen reinen Neurotransmittern und „echten“ Hormonen angesiedelt sind die sog. Neuromodulatoren, zu denen die Endorphine – sie werden ebenfalls unter „Gewebshormonen“ geführt – und die Substanz P gehöre:W Schon bei Hohltieren kann man die Tätigkeit von neurosekretorischen Zellen beobachten. Sie liegen bei diesen wie auch bei Plattwürmern und Schlauchwürmern (Nemathelminthes) vereinzelt im Nervensystem – das noch wenig konzentriert ist – und geben ihre Sekrete, die innerhalb der Axone transportiert werden, direkt an die Körperflüssigkeit ab. Die phylogenetische Höherentwicklung der neurosekretorischen Zellen besteht zum einen darin, daß sie zu Zentren zusammengefaßt werden (bereits bei Saugwürmern), und zum anderen in der Ausbildung von Neurohämalorganen, in denen die sekretausscheidenden Nervenendigungen gruppiert, von Bindegewebe umgeben und in Kontakt mit kapillarartig verzweigten Gefäßen auftreten. Wohl ausgebildete Neurohämalorgane finden sich als Cerebraldrüsen bei Hundertfüßern, Sinusdrüsen bei Krebstieren, Corpora cardiaca bei Insekten und Neurohypophyse bei Wirbeltieren. In den letzteren 3 Gruppen wirken sie zusammen mit echten (vom Nervensystem unabhängigen) endokrinen Drüsen (Insektenhormone, hypothalamisch-hypophysäres System). Von Wirbeltieren ist jedoch bekannt, daß sich auch die „echten“ endokrinen Drüsen – soweit sie Peptidhormone erzeugen – histologisch-ontogenetisch aus dem Neuroektoderm ableiten (Beispiel: Nebennierenmark). Eine Evolution von endokrinen Drüsen, deren Hormone auf längere Distanz wirken, bedingt zwangsläufig eine entsprechende Evolution von Rezeptoren, welche die Signale der Hormone empfangen können (Evolution der Hormone: vgl. Infobox ). Die Spezifität der Hormonwirkung ist nicht zuletzt auf eine Spezifität der Rezeptoren zurückzuführen. Bei Tieren mit einer hochentwickelten humoralen Koordination ist das Hormonsystem hierarchisch gegliedert, kontrolliert über Neurosekrete bzw. Releasing-Hormone (früher als Releasing-Faktoren bezeichnet) höherer zentralnervöser Zentren und Hormondrüsen (Augenstiel-Y-Organkomplexe [Augenstielhormone, Y-Organ] der Krebstiere; Protocerebrum [Pars intercerebralis] – Corpora cardiaca – Corpora allata – Prothoraxdrüsenkomplex der Insekten; hypothalamisch-hypophysäres System mit den entsprechenden Zielorganen bei Wirbeltieren). Generell kann die Funktion von Hormonen als kybernetisches Modell in der abstrakten Form von Regelkreisen mit negativen, aber auch positiven Rückkopplungen beschrieben werden. Häufig ist jedoch das Zusammenspiel mehrerer Hormone wesentlich komplexer, als mit einem einfachen Regelkreis (Regelung) darzustellen wäre. Die hormonale Regulation des Blutzuckers und das adrenogenitale Syndrom sind einfachere Beispiele, die das Prinzip der Rückkopplung verdeutlichen. Abgesehen von Pflanzenhormonen (Phytohormonen) und mit Ausnahme des Juvenilhormons bei Insekten, einem Terpenderivat, ist die chemische Zugehörigkeit der Hormone auf Aminosäure-Abkömmlinge (Phenylalanin; Aminosäuren), auf Peptide bis hin zu echten Proteinen (Peptidhormone, Proteohormone), auf Steroide (Steroidhormone) und Derivate ungesättigter Fettsäuren (Eikosanoide) beschränkt. – Die Primärwirkung der Hormone läßt sich 3 verschiedenen Mechanismen zuordnen ( vgl. Abb. ), die allerdings nicht in jedem Fall scharf zu trennen sind: a) Aktivierung einer in die Zellmembran integrierten Adenylat-Cyclase. Auf diesem Weg wird eine Verstärkung des Hormonsignals erreicht. Die Antwort wirkt in der Regel kurzfristig (Adrenalin, Noradrenalin, Glucagon, Parathormon, Thyreotropin, Adiuretin, luteinisierendes Hormon, hypothalamische Releasing-Hormone). b) Induktion (Stimulation) der Synthese spezifischer (meist Enzym-)Proteine durch Aktionen am Zellkern. Die so hervorgerufenen Effekte sind meist lang anhaltend (Steroidhormone, Schilddrüsenhormone). c) Regulation der Zellmembranpermeabilität (Insulin, Adiuretin – über cAMP-Mechanismus; cAMP). Ein wesentliches Kriterium der Hormonwirkung besteht in der Begrenzung ihrer Wirkzeit, gemessen über die Halbwertszeit (biologische Halbwertszeit). Diese kann sich zwischen Tagen (Thyroxin), Stunden (Cortisol) und Minuten (Insulin, Adiuretin) bewegen. Eine weitere Möglichkeit, die Wirkung von Hormonen zu modifizieren, besteht darin, die Dichte der Rezeptoren zu erhöhen (Aufwärtsregulation) oder zu vermindern (Abwärtsregulation). Diese Regulation kann durch das entsprechende Hormon selbst, aber auch duch andere Hormone (z.B. Steroidhormone) erfolgen. Das second-messenger-System (sekundäre Boten) kann ebenfalls unterschiedlich auf ein Hormonsignal reagieren. Ein pulsatiles Hormonsignal kann in ein intrazelluläres Signal mit der gleichen Frequenz umgewandelt werden, es kann zu einer Aufaddierung und somit zu einer Verstärkung auf einem kontinuierlichen Niveau kommen oder zu einer Abnahme des intrazellulären Signals durch eine Rezeptordesensibilisierung aufgrund einer zu hohen Stimulationsfrequenz. Für die Beseitigung von Hormonen sorgen direkte Abbauprozesse oder Konjugationsreaktionen (in der Leber oder entsprechenden Organen; Konjugation). Die Endprodukte werden als Exkrete (Exkretion) ausgeschieden und können so z.B. im Harn nachgewiesen werden (z.B. Nachweis der Schwangerschaft; Schwangerschaftstests). Die beschriebenen Primärwirkungen der Hormone führen über zahlreiche in ihrer kausalen Abfolge nicht generell verstandene Zwischenstufen zu so hochintegrativen Leistungen wie Verhaltenssteuerungen (Brutpflege, Balz, sexuelle Aktivitäten [Brunst]) und beim Menschen zu psychischen Veränderungen (Pubertät, Klimakterium). Bedeutende Beiträge zur Hormonforschung lieferten u.a.: W.M. Bayliss, C.É. Brown-Séquard, A.F.J. Butenandt, H.H. Dale, E.A. Doisy, J. Fitting, R.C.L. Guillemin, G.J.F. Haberlandt, E.C. Kendall, A. Kühn, G.G. Pincus, F. Pregl, T. Reichstein, E.W. Sutherland, J. Takamine, V. du Vigneaud. – adrenerge Rezeptoren (Abb.), Auxine, Biochemie (Geschichte der), Endokrinologie, Genaktivierung, glandotrope Hormone, Glykogen, G-Proteine, Hormoneinheit, Insektenhormone (Tab.), Membran, neuroendokrines System, Neuroimmunologie, Neuropeptide, Pheromone, Signaltransduktion; Hormone , Menstruationszyklus.
K.-G.C./L.W.
Lit.: Spindler, K.-D.: Vergleichende Endokrinologie. Stuttgart 1997.
Hormone
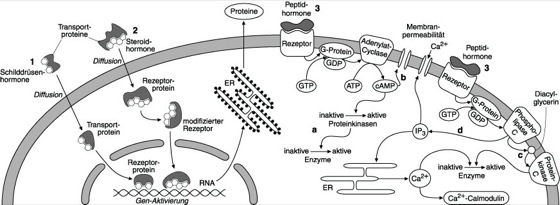
Prinzipien der verschiedenen Primärwirkungen von Hormonen an der Zellmembran und in der Zelle
1 Das hydrophobe Schilddrüsenhormon löst sich von seinem plasmatischen Transportprotein (verschiedene Globuline und Albumine), wandert durch Diffusion und teilweise Carrier-vermittelt in die Zelle ein und bindet dort an ein neues Transportprotein. Bei dem Hormon handelt es sich überwiegend um das biologisch inaktive Thyroxin (Tetraiodthyronin, T4), das in der Zelle durch De-Iodierung in das aktive Triiodthyronin (T3) umgewandelt wird. Das T3 kann nun an den entsprechenden Rezeptor im Kern binden und so die Transkription regulieren. Hinzu kommt vermutlich noch eine Stimulierung der Proteinbiosynthese durch Beeinflussung der Translation.
2 Diffusion des lipophilen Hormons durch die Zell-Membran, nachdem es sich von seinem plasmatischen Transportprotein gelöst hat. In der Zelle erfolgt die Bindung an einen spezifischen intrazellulären Rezeptor, der in den meisten Fällen im Cytosol vorliegt, aber auch im Zellkern lokalisiert sein kann. Durch die Bindung kommt es zu einer Konformationsänderung des Rezeptors. Infolgedessen löst sich ein Schutzprotein von der DNA-Bindungsdomäne. Der so aktivierte Hormon-Rezeptor-Komplex dringt nun in den Zellkern ein und tritt über die DNA-Bindungsdomäne in Kontakt mit den spezifischen DNA-Abschnitten, den sog. hormonresponsiven Elementen. Die Gen-aktivierende Domäne induziert die Synthese von (Enzym)-Proteinen über die Aktivierung von Transkription und Translation (gilt für alle Steroidhormone). – Die fettlöslichen Hormone werden nur in ihren Zielzellen durch den jeweiligen Rezeptor gebunden und festgehalten und können sich dort sehr schnell anhäufen. Aus Zellen, die keine entsprechenden Rezeptoren haben, diffundieren sie wieder heraus. Eine Ausnahme bilden die ebenfalls fettlöslichen Prostaglandine. Sie binden an membranständige Rezeptoren und rufen schnelle, kurzfristige Änderungen hervor.
3 Bindung an Rezeptoren auf der Zellmembran und Bildung eines „second messenger“ (gilt für alle Aminosäure- und Peptidhormone, außer Schilddrüsenhormone). Die Signalübermittlung verläuft zum einen über eine Adenylat-Cyclase und cAMP (zyklisches Adenosinmonophosphat). Hierbei wird die Hormoninformation vom Rezeptor über ein G-Protein (dieses Protein wird durch Bindung von GTP [Guanosin-5'-triphosphat] aktiviert) an eine Adenylat-Cyclase übermittelt, die ATP (Adenosintriphosphat) in cAMP umwandelt. Die Informationsweiterleitung erfolgt a) über eine Proteinkinase (hierbei kommt es zu einer Vervielfältigung [Amplifikation] des Signals um einen Faktor von bis zu 107) oder b) über die Beeinflussung der Membranpermeabilität. Auf einem anderen Weg wird die Information vom Hormonrezeptor über ein G-Protein an die Phospholipase C übermittelt. Dieses Enzym spaltet Phospholipide aus der Membran in die second messenger c) Diacylglycerin (Diacylglycerol; DAG oder DG) und d) Inositol-1,4,5-triphosphat (Inositolphosphate, IP3). Das membrangebundene DG aktiviert die ebenfalls membrangebundene Proteinkinase C und aktiviert über diesen Weg weitere Enzyme. IP3 diffundiert in das Cytosol und erhöht den intrazellulären Ca2+-Spiegel, indem es entweder Ca2+-Ionen (Calcium) aus dem endoplasmatischen Reticulum (ER) freisetzt oder – nach Umwandlung zu Inositoltetraphosphat (IP4), die Membranpermeabilität für den Ca2+-Einstrom erhöht. Ca2+ aktiviert nun entweder direkt verschiedene Enzyme oder bindet an Proteine wie Calmodulin oder Troponin C, welche die Aktivitäten anderer Proteine regulieren. Auch auf dem IP3-DG-Weg kommt es zu einer äußerst effektiven Verstärkung des Ursprungssignals.
Mit dem cGMP (zyklisches Guanosinmonophosphat) wird noch ein weiteres Nucleotid als second messenger eingesetzt; allerdings wirkt hier der Hormonrezeptor direkt auf die membranständige Guanylat-Cyclase (eine weitere Form liegt frei im Cytoplasma vor). Der cGMP-Weg ist noch nicht vollständig aufgeklärt, unterscheidet sich aber wesentlich von dem des cAMP. Ein wichtiger Unterschied zwischen Adenylat- und Guanylat-Cyclase besteht in ihrer Aktivität bei verschiedenen Ca2+-Konzentrationen. Bei niedrigen Konzentrationen ist die Adenylat-Cyclase sehr aktiv, die Guanylat-Cyclase jedoch inaktiv. Durch Zunahme der Ca2+-Konzentration wird die Adenylat-Cyclase gehemmt und die Guanylat-Cyclase aktiviert. Das cGMP-System spricht auf Insulin, Calcitonin, Oxytocin, die Neurotransmitter Serotonin, Acetylcholin und auf bestimmte Prostaglandine an – insgesamt also auf den Anabolismus stimulierende Wirkstoffe. Eine der Primärwirkungen von cGMP besteht in der Aktivierung einer Phosphodiesterase. Der cGMP-Mechanismus wirkt damit insgesamt in einigen Fällen antagonistisch zum cAMP-Mechanismus.
Hormone
Tab.: Hormondrüsen und Hormonwirkungen bei Mensch und Wirbeltieren
(Nicht aufgeführt sind die meisten „Gewebshormone“, wie Erythropoetin des juxtaglomerulären Apparats der Niere und Prostaglandine verschiedener Herkunft, ferner Serotonin, Histamin, Bradykinin, Kallikrein)
| |||
| Hypothalamus (medialer Teil) „Releasing“-Hormone | Übergeordnete Auslöserhormone (glandotrope Hormone) | Kontrolle über die Ausschüttung der spezifischen Hormone des Hypophysenvorderlappens | |
| Peptidhormone des Hypophysenhinterlappens: Oxytocin, Adiuretin (ADH, Vasopressin) | Steuerung des Milchaustritts aus der Milchdrüse (zusammen mit LTH); Prostaglandin-vermittelte Kontraktion der Uterusmuskulatur unter der Geburt; Verminderung der Harnsekretion der Niere durch Verminderung des Primärharnflusses; Vasokonstriktion | ||
| Endogene Opiate: Enkephaline und Endorphine als Bruchstücke des lipotropen Hormons (LPH) | Nicht eindeutig geklärt; Erhöhung der Schmerzschwelle, verhaltenssteuernd, Kontrolle vegetativer Funktionen | ||
| Hypophyse (Hirnanhangdrüse) Hinterlappen (Neurohypophyse) | Neurohämalorgan, das Hormone des Hypothalamus speichert und an die Blutbahn abgibt (s.o.) | ||
| Melanotropin (MSH, Intermedin) | Vergrößerung von Pigmentgranula, Dunkelfärbung der Haut bei Fischen, Amphibien und Reptilien; Steuerung der Melaninsynthese | ||
| Thyreoidea-stimulierendes Hormon (TSH, Thyreotropin) | Synthese und Sekretion der Hormone der Schilddrüse; Wachstumssteuerung der Schilddrüse | ||
| Adrenocorticotropes Hormon (ACTH, Corticotropin) | Synthese und Sekretion der Hormone der Nebennierenrinde; Wachstum der Nebennierenrinde | ||
| Follikelstimulierendes Hormon (FSH) | Bei der Frau: Wachstum der Follikel im Eierstock Beim Mann: Steuerung der Samenbildung | ||
| Adenohypophyse (Zwischenlappen und Vorderlappen) | β-Lipotropin (β-LPH) | Freisetzung von Fetten im Fettgewebe (Aktivierung einer Lipase), Wirkung umstritten | |
| Luteinisierendes Hormon (LH, Interstitialzellenstimulierendes Hormon, ICSH) | Bei der Frau: Sekretion von Östrogenen und Progesteron, Auslösung des Eisprungs (mit FSH); Bildung und Funktionskontrolle des Gelbkörpers Beim Mann: Sekretion der Androgene; Auslösung der Samenabgabe bei Niederen Wirbeltieren | ||
| Prolactin (Luteotropes Hormon, Lactogenes Hormon, LTH) | Bei Säugetieren: Synthese und Sekretion der Milchbestandteile; Steuerung der Gelbkörperfunktion bei Nagetieren Bei anderen Wirbeltieren: Auslösung der Brutpflegereflexe; Bildung der Kropfmilch bei Vögeln; Wachstum und Steuerung des Eiablageverhaltens bei Amphibien | ||
| Somatotropes Hormon (STH, GH; Wachstumshormon) | Proteinsynthese; Wachstum, speziell der Extremitäten- und Schädelknochen; an Steuerung des Schlaf-Wach-Rhythmus beteiligt | ||
| Thyreoidea (Schilddrüse) | Thyroxin, Triiodthyronin | Wachstum, Entwicklung und Funktionskontrollen des Zentralnervensystems; Auslösung der Häutungs- und Mauservorgänge bei Reptilien und Vögeln; Steigerung des Sauerstoffverbrauchs und der Stoffwechselrate bei Säugetieren und Amphibien; Wärmeproduktion bei Warmblütern; Metamorphose der Amphibien | |
| Calcitonin | Antagonist des Parathormons aus der Parathyreoidea, verhindert Ca2+-Freisetzung aus den Knochen und senkt Blutcalciumspiegel | ||
| Nebennierenrinde | Glucocorticoide (Cortisol, Corticosteron) | Proteinabbau im peripheren Gewebe; Glucosebildung und Glykogensynthese; Streßanpassung; entzündungshemmende und antiallergische Wirkungen; unterschiedliche Effekte auf Verhalten und Stimmung, Modulation der Schlafmuster | |
| Mineralocorticoide (vor allem Aldosteron) | Natrium-Rückresorption in Niere, Enddarm, Harnblase (Amphibien) und Kiemen (Fische), Na/K-Verhältnis extrazellulärer Flüssigkeiten; Blutdruckkontrolle | ||
| Androgene | Kontrolle der sekundären männlichen Geschlechtsmerkmale; auch im weiblichen Geschlecht in geringen Mengen sezerniert | ||
| Nebennierenmark | Adrenalin | Frequenz und Kraft des Herzschlags, periphere Arterienkontraktion; Erweiterung der kleinen Herzarterien und der Skelettmuskelversorgung; Erhöhung des Blutzuckerspiegels; Anregung des oxidativen Stoffwechsels | |
| Noradrenalin | Generelle Konstriktion kleiner Arterien; Blutdruckerhöhung | ||
| Ovar Follikel | Östrogene (Östradiol, Östron, Östriol) Gestagene | Weibliche primäre und sekundäre Geschlechtsmerkmale und Sexualverhalten | |
| Androgene | werden durch Aromatisierung in Östrogene umgewandelt | ||
| Progesteron | zusammen mit Östrogen Regelung des Östruszyklus | ||
| Relaxin | Entspannung der Uterushals-Muskulatur und der Ligamente des Beckengürtels unter der Geburt | ||
| Inhibin | hemmt FSH-Abgabe in der Hypophyse | ||
| Gelbkörper | Östrogene und Progesteron | Aufrechterhaltung der Schwangerschaft | |
| Hoden | Androgene (besonders Testosteron) | Primäre und sekundäre männliche Geschlechtsmerkmale, Spermiogenese | |
| Inhibin | hemmt FSH-Freisetzung (Regulation der Spermiogenese) | ||
| Pankreas (Langerhanssche Inseln) | Insulin | Verminderung des Blutzuckerspiegels, Anregung des Glucoseverbrauchs, der Fett-, Glykogen- und Proteinsynthese | |
| Glucagon | Erhöhung des Blutzuckerspiegels; fördert die Zuckerabgabe aus den Leberzellen und die Gluconeogenese | ||
| Parathyreoidea (Nebenschilddrüse, Pacinische Körperchen) | Parathormon, Parathyreoidhormon, Parathyrin (PTH) | Erhöhung des Calciumspiegels im Blut; Verminderung des Phosphatspiegels im Blut durch Phosphatspeicherung und -ausscheidung | |
| Magen | Gastrin | Magensaftausschüttung | |
| Dünndarm (Ileum und Jejunum) | Sekretin | Ausschüttung des Pankreassekrets | |
| Cholecystokinin (Pankreozymin) und viele weitere Peptide (gastrointestinale Hormone) | Entleerung der Gallenblase, Abgabe der Pankreasenzyme in das Pankreassekret | ||
| Niere | Renin | Umwandlung des Angiotensinogens im Blut in Angiotensin I | |
| Blut | Angiotensin | In der aktiven Form (Angiotensin II) Erhöhung der Aldosteronsekretion, Blutdruckerhöhung, Durstgefühl | |
| Zirbeldrüse (Epiphyse, Pinealorgan) | Melatonin | Aggregation der Pigmentgranula in den Melanocyten und Entpigmentierung; Antagonist des Melanotropins der Hypophyse, Hemmung des LH-Releasing-Hormons und damit der Aktivität der Gonaden; verantwortlich für saisonale Fertilität vieler Säuger, Tag-Nacht-Rhythmus; Hormonsynthese wird durch Licht gehemmt | |
| Placenta (Mutterkuchen) | Östrogene Progesteron | ähnlich der Wirkung des luteinisierenden Hormons | |
| Choriongonadotropin, Relaxin | steigert Progesteronsynthese im Gelbkörper | ||
| Chorionsomatomammotropin (Placentalactogen) | steigert Fetusentwicklung (möglicherweise) und Milchdrüsenentwicklung | ||
| Herz | Atrialpeptid (Atrial natriuretic factor, Atriopeptin) | Erhöhung der Diurese; Natriumelimination; hemmt Sekretion von Renin und Aldosteron; Regulation des Blutdrucks und –volumens; Hemmung der Adiuretinausschüttung; Regulation des Augenkammerdrucks | |
| weißes Fettgewebe (Adipocyten) | Leptin | Regulation des Hungergefühls, „Sättigungshormon“; mit anderen Cytokinen an der Blutbildung beteiligt | |
| Urophyse (Knorpel- und Knochenfische) | Urotensin I und II | Beeinflußt die Osmoregulation und die Flußrate von Ionen über Transportepithelien |
Hormone
Tab.: Strukturen und Vorkommen von Neurohypophysen-Hormonen (identische Aminosäuren sind nicht aufgeführt)
| |||||||||||
| Hormon | Vorkommen | ||||||||||
| Arginin-Vasotocin | Ile | Gln | Arg | alle Vertebraten (Säuger nur fetal, adult im Pinealorgan) | |||||||
| Glumitocin | Ile | Ser | Gln | Rochen | |||||||
| Valitocin | Ile | Gln | Val | Knorpelfische | |||||||
| Aspargtocin | Ile | Asn | Leu | Knorpelfische | |||||||
| Asvatocin | Ile | Asn | Val | Knorpelfische | |||||||
| Phasvatocin | Phe | Asn | Val | Knochenfische | |||||||
| Isotocin | Ile | Ser | Ile | Knochenfische | |||||||
| Mesotocin | Ile | Gln | Ile | Lungenfische, Amphibien,Reptilien, Vögel, Beuteltiere | |||||||
| Phenypressin | Phe | Phe | Gln | Arg | Beuteltiere | ||||||
| Lysin-Vasopressin | Phe | Gln | Lys | Placentale Säuger, Beuteltiere | |||||||
| Arginin-Vasopressin | Phe | Gln | Arg | Säuger (außer Hausschweine, Känguruhs) | |||||||
| Oxytocin | Ile | Gln | Leu | Säuger |
Schreiben Sie uns!