Lexikon der Biologie: Immunglobuline
Immunglobuline, Abk. Ig, Gammaglobuline i.w.S., Antikörper, Proteine (Globuline), die spezifisch mit einem Antigen reagieren. Alle Immunglobuline haben eine gemeinsame Struktur ( vgl. Abb. ): sie bestehen aus 2 großen, „schweren“ (H-Ketten, relative Molekülmasse ca. 50.000) und 2 kleinen „leichten“ (L-Ketten, Molekülmasse ca. 25.000) Polypeptidketten, die durch Disulfidbrücken (Disulfidbindung) untereinander verbunden sind. Die Immunglobuline werden von den B-Lymphocyten gebildet und exocytiert. Beim Menschen unterscheidet man 5 Antikörperklassen oder Immunglobulinklassen (Ig-Klassen: IgM, IgD, IgG, IgE, IgA; vgl. Tab. ), deren H-Ketten unterschiedlich sind (μ, δ, γ, ε, α). Die L-Ketten kommen, abgesehen von den variablen Teilen (Idiotyp, Isotyp), in 2 Formen vor, den häufigeren κ-Ketten und den λ-Ketten. IgM kommt in 2 Formen vor, löslich und als Antigenrezeptor auf der Plasmamembran von B-Lymphocyten. Löslich tritt es als pentamerer Komplex auf, durch eine zusätzliche Polypeptidkette (J-Kette) zusätzlich stabilisiert. IgG (Gammaglobulin i.e.S.) ist das häufigste Immunglobulin und kommt in 4 Subklassen (γ1–γ4) vor, die etwas unterschiedliche Eigenschaften haben (isoelektrischer Punkt, Disulfidbrücken, Plasma-Halbwertszeit). Die Antikörper-Antwort gegen ein bestimmtes Antigen setzt sich jedoch aus allen 4 Subklassen zusammen. Das sehr seltene IgE kann an Mastzellen und basophile Granulocyten binden und nach Antigen-Kontakt diese Zellen zur Ausschüttung von Histamin veranlassen (Allergie). Es kommt auch, ebenso wie IgA, in Sekreten vor. – Die Spezifität der Immunglobuline liegt im variablen Teil der hypervariablen Regionen. Dort sind die Aminosäureketten so gefaltet, daß sich Bindungsstellen für ein ganz bestimmtes Antigen bilden. Diese Antigenbindungsstellen („haptophore Gruppen“) sind nicht groß; minimal sind 5 Aminosäure- bzw. Zuckerreste nötig, um immunogen zu wirken. Da antigene Makromoleküle jedoch meist viel größer sind, also eine Vielzahl antigener Determinanten oder Epitope tragen, wird die Immunantwort in der Produktion vieler Antikörperspezies gegen verschiedene Epitope bestehen. Man nimmt an, daß der Körper nahezu unbegrenzt viele Immunglobuline unterschiedlicher Spezifität bilden kann (ca. 107). Eine diesen Spezifitäten entsprechende Vielzahl von Immunglobulin-Genen kann es jedoch nicht geben (Summe aller Gene im Genom eines Menschen ca. 4·104). Mit modernen molekulargenetischen Methoden konnte gezeigt werden, daß die Stammzellen der Immunglobulin-produzierenden Immunzellen tatsächlich keine fertigen Gene für bestimmte Antikörper enthalten, dafür aber verschiedene Genkomponenten, meist in mehrfachen Versionen, die durch Rearrangement der betreffenden DNA (somatische Rekombination; Immunglobulin-Gen-Rearrangement) in vielfältige Kombinationsmöglichkeiten während der Lymphocytenentwicklung die erforderliche Anzahl von Spezifitäten ergeben. Für jede Spezifität gibt es einen B-Lymphocyten-Klon. Innerhalb der ca. 1012 Lymphocyten eines Menschen finden sich mehr als 107 in ihren Immunglobulin-Genen unterschiedliche Klone. Bei einer Attacke durch ein bestimmtes Antigen (Infektion) werden diejenigen Lymphocyten-Klone zur Immunglobulinproduktion angeregt, deren Idiotypen den antigenen Determinanten entsprechen. Allergie, Antigen-Antikörper-Reaktion, Bogomolez (A.A.), Clone-selection-Theorie, Edelman (G.M.), Gammopathien, Immunglobulin-Superfamilie, Immunglobulinsynthese, Milchproteine, Porter (R.R.), Serumproteine, somatische Mutationen, Virusinfektion; Chromosomenkarte ( Chromosomenkarte I
Chromosomenkarte II
Chromosomenkarte III
Chromosomenkarte IV
).
B.L.
Immunglobuline
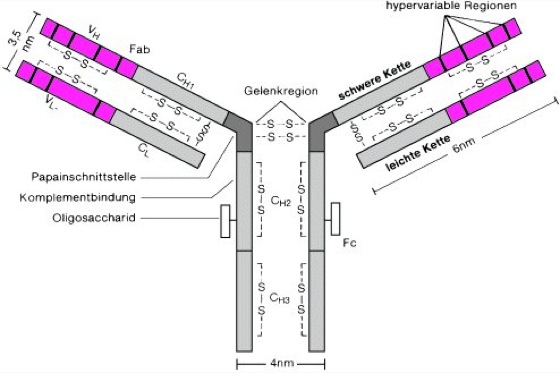
Schematische Darstellung eines IgG-Antikörpermoleküls.
Die Struktur der Immunglobuline wurde Anfang der 1960er Jahre von G.M. Edelman und R.R. Porter aufgeklärt. Dies war u.a. dadurch möglich, daß man große Mengen einheitlicher Immunglobuline aus Myelomen gewinnen konnte – Tumoren, die sich von transformierten Lymphocyten herleiten (Myelomproteine). Die großen H-Ketten (schwere Ketten) bestehen aus 1 variablen Region am Aminoende (VH) und 3 konstanten Bereichen (CH1-CH3). Zwischen CH1 und CH2 befindet sich eine Gelenkregion. Die L-Ketten (leichte Ketten) bestehen ebenfalls aus 1 variablen Anteil am Aminoende (VL) und 1 konstanten Molekülbereich (CL). Innerhalb der variablen Domänen gibt es bei den L-Ketten 3 und bei den H-Ketten 4 sog. hypervariable Regionen. Das sind diejenigen Bereiche, in denen die Aminosäuresequenzen bei Antikörpern unterschiedlicher Spezifitäten besonders stark variieren können. Innerhalb der CH2-Abschnitte befinden sich eine Oligosaccharidseitenkette sowie eine Komplementbindungsstelle. Disulfidbindungen (S-S) gibt es innerhalb der einzelnen Ketten, zwischen L- und H-Ketten und im Bereich der Gelenkregion zwischen den beiden H-Ketten. Durch Papainspaltung (Papain) in der Gelenkregion wird das Molekül in 1 Fc-Fragment (c = crystallizable; Fc) und 2 Fab-Fragmente (ab = antigen binding) zerlegt.
Immunglobuline
Eigenschaften humaner Immunglobuline
| |||||||
| IgG1 | γ1 | 148.000 | 4 | + | 9 | 21 | |
| IgG2 | γ2 | 148.000 | 4 | + | 3 | 21 | |
| IgG3 | γ3 | 159.000 | 4 | + | 1 | 7 | |
| IgG4 | γ4 | 148.000 | 4 | + | 0,5 | 21 | |
| IgM | μ | 955.000 | 5 | – | 1,2 | 5 | |
| IgA1 | α1 | 160.000 | 4 | + | 2,0 | 6 | |
| A2m(1) | α2 | 162.000 | 4 | + | ? | ||
| IgA2 | 0,5 | ||||||
| A2m(2) | α2 | 166.000 | 4 | + | 6 | ||
| IgD | δ | 175.000 | 4 | + | 0,04 | 3 | |
| IgE | ε | 190.000 | 5 | – | 0,0002 | 3 |
Schreiben Sie uns!