Lexikon der Biologie: Lysozym
Lysozym s [von *lyso- , griech. zymē = Gärmittel], Endolysin, Muramidase, ein weitverbreitetes Enzym, durch das die Zellwand besonders von grampositiven Bakterien (Bakterienzellwand) aufgelöst wird, indem es die Hydrolyse (Hydrolasen) von Murein an der glykosidischen Bindung zwischen den N-Acetylmuraminsäure-(NAM-) und N-Acetylglucosamin-(NAG-)Einheiten katalysiert (N-Acetylmuraminsäure, N-Acetylglucosamin), wodurch es zur Lyse von Bakterien (Bakteriolyse) kommt. Auch glykosidische Bindungen von Chitin werden von Lysozym hydrolysiert. Lysozym kommt u.a. in Körperflüssigkeiten wie Speichel, Tränenflüssigkeit, Nasenschleim (worin es von A. Fleming erstmals als bakteriolytisches Agens beobachtet wurde) und im Eiklar (Avidin, Eiklarproteine, Hühnerei) vor, aber auch in Pflanzen, Bakterien und speziell in phageninfizierten (Bakteriophagen) Bakterien, codiert durch ein phagenspezifisches Lysozym-Gen. Durch seine bakteriolytischen Eigenschaften wirkt Lysozym in Geweben und Körperflüssigkeiten als Schutz vor bakterieller Infektion. Tierisches und menschliches Lysozym ist aus 129 Aminosäuren (relative Molekülmasse 14.600) aufgebaut, deren komplizierte, u.a. durch 4 Disulfidbindungen und viele Wasserstoffbrücken zusammengehaltene dreidimensionale Struktur durch Röntgenstrukturanalyse so genau bekannt ist, daß die Zuordnung des aktiven Zentrums und die Enzym-Substrat-Interaktion bis zu atomaren Einzelheiten ( vgl. Abb. ) verstanden sind. Wie bei anderen hydrolytisch wirksamen Enzymen (z.B. Chymotrypsin, Papain, Ribonucleasen) wird auch die dreidimensionale Struktur des Lysozyms durch einen Spalt in 2 Hälften geteilt. Dieser Spalt ist das aktive Zentrum des Lysozyms und dient zur Aufnahme einer Hexasaccharideinheit des zu hydrolysierenden Substrats. Bakteriozidie, Chain (E.B.), Cytolyse, Proteine, Protoplast, Proteinkristallisation.
Lysozym
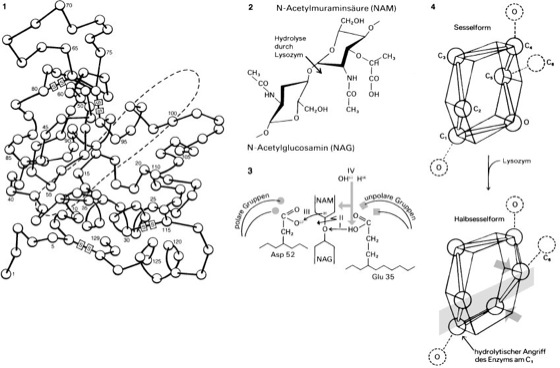
1 Räumliche Struktur des Lysozym-Moleküls. Rechtecke symbolisieren Disulfidbrücken (S–S), die Strichelung markiert das spaltförmige aktive Zentrum, die Ziffern geben die Reihenfolge (Nummern) der Aminosäuren an.
2 Das Substrat des Lysozyms: Polysaccharide z.B. der Bakterienzellwand, bestehend aus N-Acetylglucosamin- (NAG) und N-Acetylmuraminsäure-Einheiten (NAM).
3 Molekularer Wirkungsmechanismus des Lysozyms: Ein NAM- und ein NAG-Zuckerrest der Bakterienzellwand (vgl. 2) liegen eng benachbart zu 2 Aminosäuren (Glutaminsäure 35 und Asparaginsäure 52) des aktiven Zentrums des Lysozyms. Dies führt zu einer Dissoziation des H+ von der nicht peptidgebundenen Carboxylgruppe (COOH) der Glu mit anschließender Bindung an den glykosidischen Sauerstoff (O) zwischen den beiden Zuckerresten (I). Die Glykosidbindung wird dabei gespalten (II) unter Bildung eines positiv geladenen Carbeniumions; letzteres wird durch die negativ geladene Carboxylgruppe der Asparaginsäure (III) stabilisiert. Wasser (H+-, OH–-Ionen) vollendet die Spaltung, indem Glu 35 protoniert wird, das Carbeniumion mit OH– reagiert und somit die Substratspaltstücke vom aktiven Zentrum weg diffundieren können (IV).
Neben den hier gezeigten Wechselwirkungen unmittelbar zwischen dem aktiven Zentrum und der Spaltstelle des Substrats sind auch Interaktionen zwischen entfernteren Positionen des Lysozyms und des Substrats von Bedeutung. Dies zeigt sich darin, daß Substrate aus nur 2 Zuckerresten gar nicht hydrolysiert werden; eine optimale Hydrolyse erfolgt erst ab Substraten mit 6 und mehr Resten. Bei hexamerem NAG-Substrat erfolgt die Spaltung exakt zwischen dem C-1 von Rest 4 und dem Sauerstoff der glykosidischen Bindung am Rest 5.
4 Die Substratbindung im aktiven Zentrum von Lysozym sowie die Bildung des Carbeniumions werden durch Deformation der energetisch stabileren Sesselform von NAM oder NAG zur Halbsesselform erheblich verbessert (betrifft Rest 4 bei hexamerem Substrat). Das C-Atom 5 und der Ringsauerstoff werden in Pfeilrichtung bewegt, wodurch die 4 hervorgehobenen Ringatome in einer Ebene der Halbsesselform liegen.
Schreiben Sie uns!