Lexikon der Biologie: Rhodopsin
Rhodopsins [von *rhod- , griech. opsis = Sehen], Sehpurpur, Erythropsin, das visuelle Pigment (Augenpigmente) in den Stäbchen-Sehzellen der Netzhaut von Wirbeltieren. Rhodopsin stellt den bestuntersuchten Vertreter der Opsin-Proteinfamilie (eine G-Protein-gekoppelte Rezeptor-Familie; G-Proteine, G-Protein gekoppelte Rezeptoren) dar, die viele einander strukturell und funktionell ähnliche integrale Membranproteine mit Rezeptoreigenschaften umfaßt. Das lichtempfindliche, aus Chromophor (11-cis-Retinal) und Proteinkomponente („Opsin“) zusammengesetzte Chromoprotein ist in hoher Konzentration in den Disc-Membranen (Disc) der Stäbchen-Außensegmente vorhanden und stellt in den Augen (Linsenauge) von Wirbeltieren den bei weitem überwiegenden Sehfarbstoff dar. (So findet man bei Rindern wegen des weitgehenden Fehlens von Sehfarbstoffen mit anderen Absorptionseigenschaften keine Farbunterscheidung; das rote Tuch des Toreros reduziert sich damit auf den Bewegungsreiz.) Rhodopsin dient als Lichtsensor, das den einfallenden Lichtreiz (Licht) in eine chemische Reaktion umsetzt (Photoisomerisierung des Retinal-Chromophors). Diese Photochemie des Chromophors initiiert eine Reihe konformeller Änderungen in der Proteinkomponente, in deren Verlauf es zur Aktivierung der visuellen Transduktionskette (Signaltransduktion) kommt. Rhodopsin stellt somit das erste Glied einer hochverstärkten Signalkaskade dar, die schließlich in die Änderung des Membranpotentials der Sehzelle mündet. Bei Rhodopsin endet die Lichtreaktion mit einem Freisetzen des in die all-trans-Form isomerisierten Chromophors („Bleichung“; bleichen). Die dadurch freigewordene Proteinbindungsstelle steht einer Neusynthese von Rhodopsin aus Opsin und neuem 11-cis-Retinal zur Verfügung. Der freigesetzte Chromophor wird aus dem Bereich der Sehzelle abtransportiert und zum Teil in den zellulären Vitamin-A-Zyklus (Retinol) eingeschleust, zum Teil aber auch im Pigmentepithel des Auges reduziert, in die 11-cis-Form reisomerisiert und wieder oxidiert, und steht somit ebenfalls für eine Neusynthese zur Verfügung. Im Gegensatz zu der Rhodopsinbleichung wird bei einigen Insekten und Kopffüßern die Bindung zwischen Chromophor und Protein nicht gelöst. Es ergibt sich somit bei diesen Tieren ein anderer Regenerationsmechanismus, indem durch den Treffer eines zweiten Photons (Quanten) das Pigment reaktiviert werden kann. Rhodopsin weist eine Absorption um 500 nm (maximale Empfindlichkeit für grünes Licht) auf. Allerdings trägt diese Spektralempfindlichkeit (Augenempfindlichkeit) nicht zum Farbensehen bei, da die Stäbchen-Sehzellen unter Taglichtbedingungen (= hohe Lichtintensitäten; photopisches Sehen) durch Adaptation keine neuronale Aktivität aufweisen. Die durch Rhodopsin hervorgerufene Reizantwort wird nur für das Dämmerungssehen (skotopisches Sehen) eingesetzt. Unter diesen schwachen Lichtintensitäten sind die für das Farbensehen verantwortlichen Zapfen-Sehzellen nicht aktiv, so daß es zu keiner spektralen Diskriminierung des einfallenden Lichts kommt („nachts sind alle Katzen grau“). Die Verwendung des Rhodopsins bei niedrigen Lichtintensitäten erklärt die große Dichte des Rhodopsins in den Außensegmenten der Stäbchenzellen und den hohen Verstärkungsfaktor der visuellen Kaskade. Beide Effekte haben den Zweck, mit hoher Wahrscheinlichkeit jedes in das Auge einfallende Lichtquant zu detektieren und in einen neuronalen Reiz umzuwandeln. – Das sensorische Rhodopsin von Halobakterien ist dem Rhodopsin strukturell sehr ähnlich und für die positive wie negative Phototaxis dieser Bakterien verantwortlich. Es scheint über die Aktivierung eines Proteins (relative Molekülmasse 97.000) als Übermittler Einfluß auf die Bewegung der Flagellen und somit der Schwimmrichtung der Bakterien auszuüben. – Neuere Untersuchungen zeigen, daß auch die lichtsensitiven Zoosporen (Planosporen) des Bodenpilzes Allomyces reticulatus (Blastocladiales) Rhodopsin als lichtabsorbierendes Molekül nutzen. Bakteriorhodopsin, Chlamydomonas, Chromosomenkarte ( Chromosomenkarte I
Chromosomenkarte II
Chromosomenkarte III
Chromosomenkarte IV
), Halorhodopsin, Photorezeption, Proteorhodopsin, Transducin, Wald (G.).
W.G./E.G.
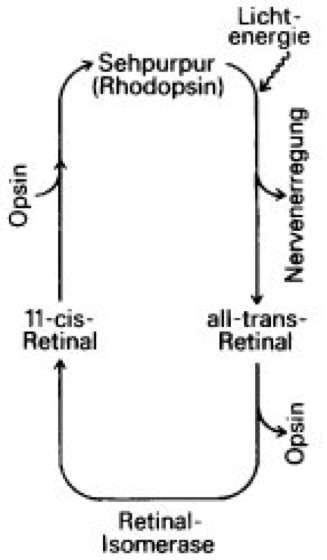
Rhodopsin
Zyklischer Sehvorgang in den Stäbchen-Zellen der Netzhaut (schematisch).
Rhodopsin (relative Molekülmasse ca. 40.000) besteht aus dem Protein Opsin und der prosthetischen Gruppe 11-cis-Retinal, dessen Vorstufe das all-trans-Retinol (Vitamin A) ist. Das 11-cis-Retinal ist mit der ε-Aminogruppe von Lys 296 des Opsins in Form einer Schiffschen Base verknüpft. Der 11-cis-Retinal-Chromophor befindet sich in einer Proteintasche annähernd im Zentrum des Siebenhelix-Motivs des Rhodopsins. Der N-Terminus (Aminoterminus) enthält zwei N-gebundene Oligosaccharideinheiten und befindet sich auf der dem Scheibenzwischenraum zugewandten Membranseite, während auf der cytosolischen Seite in der Nähe des C-Terminus (Carboxylterminus) mehrere Ser- und Thr-Reste lokalisiert sind, die durch Phosphorylierung das durch Licht erregte Rhodopsin inaktivieren. Auch in anderen eukaryotischen Membran-Rezeptoren findet sich das Siebenhelix-Motiv des Rhodopsins. Sehfarbstoffe (Abb.).
Wenn Sie inhaltliche Anmerkungen zu diesem Artikel haben, können Sie die Redaktion per E-Mail informieren. Wir lesen Ihre Zuschrift, bitten jedoch um Verständnis, dass wir nicht jede beantworten können.