Lexikon der Chemie: Diffusion
Diffusion, der Stofftransport in Gasen, Flüssigkeiten oder Festkörpern unter dem Einfluß von Konzentrationsdifferenzen. Die D. erfolgt spontan aufgrund der mikroskopischen Teilchenbewegung. Sie strebt den Ausgleich von Konzentrationsunterschieden an. Die D. ist ein irreversibler Prozeß, der mit einer Entropiezunahme verknüpft ist und nur unter Arbeitsaufwand rückgängig gemacht werden kann.
In Gasen und Flüssigkeiten ergibt sich aus der regellosen thermischen Bewegung der Teilchen im statistischen Mittel ein Stofftransport in Richtung der niedrigeren Konzentration. In kristallinen Festkörpern existieren verschiedene Diffusionsmechanismen: 1) direkter Austausch von zwei Kristallbausteinen (Platzwechsel), 2) Wanderung über Zwischengitterplätze, 3) Wanderung über unbesetzte Gitterplätze (Leerstellenmechanismus), 4) Wanderung entlang von Gitterversetzungen oder an Korngrenzen, 5) Platzwechselvorgänge an Kristalloberflächen (Oberflächendiffusion) oder in den Poren von porösen Festkörpern (Porendiffusion).
Die Diffusionsgeschwindigkeit wächst im allg. mit der Temperatur, da die Teilchen sich schneller bewegen und sinkt mit steigender Dichte. In Festkörpern verläuft die D. erst bei Temperaturen in der Nähe des Schmelzpunktes mit merklicher Geschwindigkeit, da die Anzahl der Fehlstellen dann erheblich ansteigt.
Die mathematische Behandlung der D. erfolgt mit Hilfe der Fickschen Gesetze. Das 1. Ficksche Gesetz gilt für den Fall eines stationären, d. h. zeitlich und örtlich konstanten Konzentrationsgefälles dc/dx. Es lautet dn/dt = -DA(dc/dx). Dabei ist dn/dt die Diffusionsgeschwindigkeit, d. h. die Stoffmenge dn, die in der Zeit dt durch eine Fläche A in Richtung der Ortskoordinate x diffundiert. D ist der Diffusionskoeffizient, der meist in der Einheit cm2 s-1 angegeben wird. Die Annahme, daß D konzentrationsunabhängig ist, wird nur für Gase und stark verd. Lösungen gut erfüllt. Ist das Konzentrationsgefälle räumlich und zeitlich nicht konstant (instationäre D.), dann gilt das 2. Ficksche Gesetz. Für den eindimensionalen Fall der D. in x-Richtung lautet es (∂c/∂t)x = D(∂2c/∂x2)t.
Die Lösungen dieser Differentialgleichungen hängen von den Randbedingungen des jeweiligen Diffusionsvorganges ab und beschreiben, wie sich die Konzentrationen in Abhängigkeit vom Ort und der Zeit ändern.
Ist der Diffusionskoeffizient konzentrations- und damit ortsabhängig, muß die allgemeine Transportgleichung
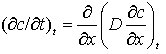
zur Beschreibung der D. verwendet werden.
Die Diffusionskoeffizienten in Gasen, Flüssigkeiten und Festkörpern unterscheiden sich um viele Zehnerpotenzen. Dabei muß man zwischen Selbstdiffusion (Platzwechsel einer Teilchensorte) und Gegendiffusion unterscheiden. Die Gegendiffusion ist die D. verschiedener Stoffe gegeneinander, z. B. bei Vermischung von zwei Stoffen.
Die kinetische Gastheorie liefert für den Selbstdiffusionskoeffizienten eines Gases D = v l/3, wobei v die mittlere Teilchengeschwindigkeit und l die mittlere freie Weglänge bedeuten. Für den Gegendiffusionskoeffizienten zweier Stoffe 1 und 2 (mit den Teilchendichten N1, N2 ergibt sich D12 = (N1v1l1 + N2v2l2)/3(N1 + N2). Für leichte Gase mit annähernd gleicher mittlerer Geschwindigkeit und freier Weglänge ist D12 ≅ D.
Diffusionskoeffizienten in flüssiger Phase können nach der Einstein-Stokes-Gleichung D = kT/6πηr abgeschätzt werden. Dabei ist η die Viskosität, k die Boltzmann-Konstantze und r der Radius kugelförmiger Teilchen. In Festkörpern gilt für die Temperaturabhängigkeit D = D0e-ED/RT. Dabei ist ED eine Aktivierungsenergie der Diffusion, die etwa 150 bis 500 kJ mol-1 beträgt, D0 ist eine Konstante. Die Beziehung ist auf Flüssigkeiten übertragbar. Die ED-Werte liegen dann bei 5 bis 20 kJ mol-1.
Die D. spielt ebenso wie der Wärmetransport bei großtechnischen Reaktionen eine zentrale Rolle. Bei den meisten Festkörperreaktionen und schnellen Vorgängen in Lösung wird die Reaktionsgeschwindigkeit durch die Diffusionsgeschwindigkeit bestimmt (Diffusionskontrolle). Stofftrennprozesse sowie Vakuum-Diffusionspumpen basieren auf einer Nutzung der D.
Eine besondere Form der D. erfolgt in hochverdünnten Gasen, in denen die mittlere freie Weglänge der Teilchen groß gegenüber den Gefäßabmessungen ist. Dann finden praktisch keine Stöße zwischen den Molekülen, sondern nur solche mit der Wand statt. Der Ausgleich von Konzentrations- und Druckunterschieden erfolgt wesentlich langsamer als bei Normaldiffusion. Man spricht von Knudsen-Diffusion (Knudsen-Strömung). Ein weiterer Sonderfall der D. ist die Thermodiffusion.
Schreiben Sie uns!