Neuer Mechanismus: Hoffnung auf neues Autismusmedikament verfrüht
Es ist ein durchaus bemerkenswerter Mechanismus, dem französische Forscher seit einiger Zeit auf der Spur sind. Sie versuchen nicht weniger, als damit ein für alle Mal zu erklären, warum es beim Menschen aus ganz unterschiedlichen Gründen zu den typischen Autismussymptomen kommt. Und wie sie sich – zumindest im Tierversuch – verhindern lassen.
Bei den Betroffenen, so erklären es Yehezkel Ben-Ari vom Institut de Neurobiologie de la Méditerranée des INSERM in Marseille und seine Kollegen, versage während der Geburt ein Schalter im Gehirn: Das Hormon Oxytozin, das unter anderem auch die Wehen auslöst, senkt den Gehalt an Chloridionen in den Hirnzellen während der Geburt drastisch ab. Das wiederum führt normalerweise dazu, dass der Neurotransmitter GABA fortan nicht mehr, wie im Fötus, erregend auf die Nervenzellen wirkt, sondern hemmend wie bei Erwachsenen.
Unterbleibt jedoch – aus welchen Gründen auch immer – diese Wirkung des Oxytozins, blieben die Chloridwerte dauerhaft hoch, und der Schalter klemmt. Das, so die Spekulation der Forscher, lenke das Gehirn im entscheidenden Moment auf eine falsche Bahn. Das neuronale Netzwerk könne sich nicht mehr ungestört entwickeln.
Die Studie sei "ziemlich klasse", meint dazu im Magazin "Science" der Hirnforscher Emanuel DiCicco-Bloom von der Robert Wood Johnson Medical School der Rutgers University in Piscataway: Kaum jemand habe bisher einen solchen Effekt auf dem Plan gehabt. Das bestätigt auch Nils Brose vom Max-Planck-Institut für experimentelle Medizin in Göttingen: Das Team habe einen "hochinteressanten Befund" geliefert. Doch überzeugt sind beide Forscher trotzdem noch nicht.
Klinische Studien unterstützen die Annahme
Die Wirkung der Chloridionen erforscht die Gruppe um Ben-Ari bereits seit einigen Jahren. Zuletzt hatten sie eine kleine Studie vorgelegt, für die sie an Autismus erkrankte Kinder und Jugendliche mit dem Diuretikum Bumetanid behandelten, einem harntreibenden Medikament, das Chloridionen mit dem Urin ausspült und so den Gehalt im Gehirn senkt. Bei den drei- bis elfjährigen Probanden zeigten sich leichte Verbesserungen der Symptome, allerdings gilt die Aussagekraft der Studie als sehr begrenzt. Eine größer angelegte Phase-II-Studie ist bereits angelaufen und soll Ende des Jahres veröffentlicht werden. Überdies hat Ben-Ari bereits eine Firma gegründet, mit der er den Einsatz von Chloridsenkern bei neurodegenerativen Erkrankungen erforschen will.
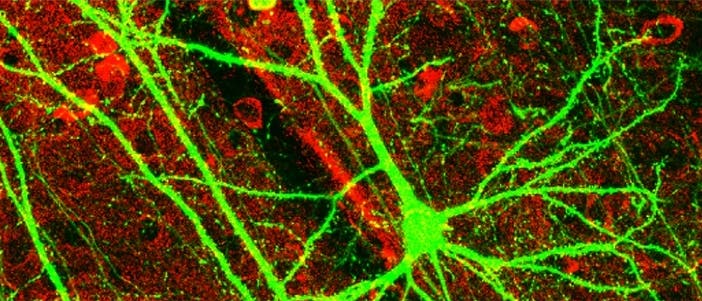
In diesem Ausschnitt aus dem Kortex einer Maus sind Neurone ohne GABA grün angefärbt. Die rot gefärbten GABA-Interneuronen tragen wohl durch ihre hemmende Wirkung dazu bei, die Erregung im Gehirn unter Kontrolle zu halten.
Behalten sie jedoch die erregende Rolle, die sie während der Hirnentwicklung spielen, nach der Geburt bei, könnte dies autistische Symptome auslösen.
Die aktuelle Untersuchung seines Teams ist nun darauf ausgelegt, die angenommenen neurobiologischen Grundlagen des Mechanismus zu erhärten [1]. Dazu griffen sie auf zwei verbreitete Tiermodelle für Autismus zurück: Zum einen schalteten sie bei Mäusen ein Gen aus, dass auch beim Fragile-X-Syndrom eine Rolle spielt, einer gängigen Ursache für autistische Störungen bei Kindern; zum anderen verabreichten sie schwangeren Rattenmüttern Valproinsäure, was auch bei Menschen das Autismusrisiko erhöht.
Beides führte erwartungsgemäß bei den neugeborenen Nagern zu untypischen Verhaltensweisen, die nach üblicher wissenschaftlicher Praxis als tierische Entsprechung einer Störung aus dem autistischen Spektrum aufgefasst werden können. Die Tiere haben beispielsweise ein abnormes Sozialverhalten und rufen deutlich seltener nach ihrer Mutter, wenn sie von ihr getrennt sind.
Erwartete Veränderungen in den Hirnzellen
Neben diesen Verhaltensauffälligkeiten beobachteten Ben-Ari und sein Team jedoch auch die Veränderungen auf Zellebene, die laut ihrer Theorie zu erwarten sind: Bei beiden Tiergruppen unterblieb das übliche Absinken des Chloridspiegels während der Geburt, beide Gruppen hatten über Tage hinweg erhöhte Chloridwerte und bei beiden behielt der Neurotransmitter GABA im Hippocampus seine erregende Wirkung.
Erstaunlicherweise konnten sie dieselben Effekte auch hervorrufen, indem sie den schwangeren Nagetieren eine Substanz verabreichten, die die Wirkung von Oxytozin im Gehirn blockierte. Das bestätigt ihre Hypothese über dessen Wirkung auf den GABA-Schaltvorgang.
Als entscheidendes Ergebnis ihrer Studie sehen diese allerdings auch ein ganz anderes Phänomen: Es gelang ihnen nämlich, durch Gabe von Bumetanid – also dem diuretischen Chloridsenker, den sie auch in der klinischen Studie testeten – alle genannten Effekte am Erscheinen zu hindern. Die Wissenschaftler gaben das Medikament dazu bereits den werdenden Nagetiermüttern. Daraufhin zeigte deren Nachwuchs keines der autismustypischen Kennzeichen mehr, obwohl sie entweder das defekte Fragile-X-Gen trugen oder als Embryo der Valproinsäure ausgesetzt waren. Wenn man so will, haben die Forscher damit die Tiere von ihren autistischen Symptomen geheilt.
Neue Perspektiven für die Autismustherapie
Dementsprechend eröffne die Studie gänzlich neue Perspektiven für die Autismustherapie, erläutern Andrew Zimmermann und Susan Connors in einer begleitenden Veröffentlichung in "Science" [2]. Die Theorie von Ben-Ari und Kollegen habe den Vorteil zu erklären, warum unterschiedlichste Ursachen wie etwa Genveränderungen oder auch Umweltgifte Autismus auslösen können: Allen oder zumindest einigen davon wäre demnach gemein, dass sie das Wechselspiel von Oxytozin, Chlorid und GABA aus dem Tritt bringen.
Dass sich dieser Schluss jetzt schon aus der Studie ziehen lässt, bezweifelt allerdings der Göttinger Forscher Brose: "Die verwendeten Tiermodelle sind nicht optimal geeignet, um Aussagen über Autismus bei Menschen zu treffen." Beide Verfahren, autismusähnliche Symptome auszulösen, hätten noch eine Reihe ganz anderer Wirkungen, die mit Autismus nicht direkt in Zusammenhang stünden. "Es wäre daher interessant zu sehen, ob der Mechanismus auch bei Mausmodellen auftritt, die den menschlichen Autismus besser modellieren." Als Beispiel nennt er genetische Störungen der Gene, die bei der Synapsenbildung eine Rolle spielen. Sie kämen bei Erkrankungen des autistischen Spektrums gehäuft vor und ließen sich ebenfalls im Tierexperiment nachbilden. Erst dann zeige sich, ob es die zentrale Gemeinsamkeit wirklich gebe.
In einer telefonischen Pressekonferenz kündigte Ben-Ari bereits an, in einer Nachfolgestudie weitere Tiermodelle einzusetzen. Aber möglicherweise ist die Hirnentwicklung von Nagetieren und Menschen grundsätzlich nicht gut vergleichbar, wendet DiCicco-Bloom ein. Sie verläuft bei den Mäusen und Ratten erheblich rascher als bei Kindern, der GABA-Effekt schlägt darum vielleicht wesentlich deutlicher zu Buche. Die Wissenschaftsjournalistin und Autismusexpertin Emily Willingham wendet außerdem ein, dass sich sowohl Valproinsäure als auch das Fragile-X-Syndrom bekanntermaßen auf GABA auswirken. Möglicherweise kompensieren die Wissenschaftler also lediglich einen speziellen Effekt beider Auslöser, der mit "üblichen" Störungen des autistischen Spektrums bei Menschen wenig zu tun hat.
Chloridsenker vor der Geburt?
Sollte er sich dennoch in weiteren Untersuchungen erhärten, wäre es die nächstliegende Konsequenz, das Bumetanid prophylaktisch allen werdenden Müttern kurz vor der Geburt zu verabreichen oder den Neugeborenen kurz danach. Das aber halten selbst die Autoren für nicht praktikabel. Es bestehe keine Möglichkeit, einen Fötus auf sein Autismusrisiko zu untersuchen. In der Regel wird eine autistische Störung erst in einem Alter von zwei Jahren erkannt. Frühestens dann sei eine Therapie mit Chloridsenker ratsam.
In diesem Sinn liefert die Studie der französischen Forscher wohl eher neue Impulse für die Grundlagenforschung als konkrete Hoffnungen auf einen baldigen Einsatz in der Therapie. Bumetanid selbst gilt im Allgemeinen immerhin als gut verträglich: Es wird seit den 1970er Jahren unter anderem bei Nierenerkankungen und Herzproblemen angewendet – in Ben-Aris klinischer Studie von vor einigen Jahren blieb es weitestgehend ohne Komplikationen.

Schreiben Sie uns!
1 Beitrag anzeigen