Lexikon der Biochemie: aktive Einkohlenstoff-Einheiten
aktive Einkohlenstoff-Einheiten, C1-Einheiten, molekulare Gruppierungen, die ein einzelnes Kohlenstoffatom enthalten und entweder durch die Bindung an Tetrahydrofolsäure oder (seltener) an Thiaminpyrophosphat aktiviert werden. Die C1-Einheiten werden an das N5 und/oder das N10 der Tetrahydrofolsäure (THF) gebunden (Abb. 1).
Die Hauptquelle der C1-Einheiten ist die Hydroxymethylgruppe des Serins, die mit Hilfe der Hydroxymethyltransferase (EC 2.1.2.1) auf THF übertragen wird, wodurch N10-Hydroxymethyl-THF (aktivierter Formaldehyd) entsteht. Von besonderer Bedeutung ist die Bildung von C1-Einheiten im Histidinkatabolismus und beim anaeroben Abbau von Purinen. C1-Einheiten werden während der Purinbiosynthese eingebaut und stellen die 5-Methylgruppe von Thymin. An THF gebundene C1-Einheiten werden umgewandelt (Abb. 2). Andere metabolische Quellen und Verwendungen für C1-Einheiten sind in der Legende von Abb. 2 aufgeführt.
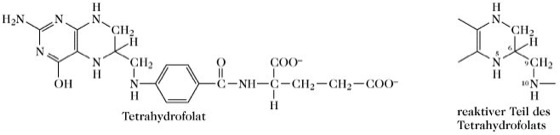
aktive Einkohlenstoff-Einheiten.Abb. 1. Struktur des Tetrahydrofolats (THF) und des reaktiven Teils von THF.
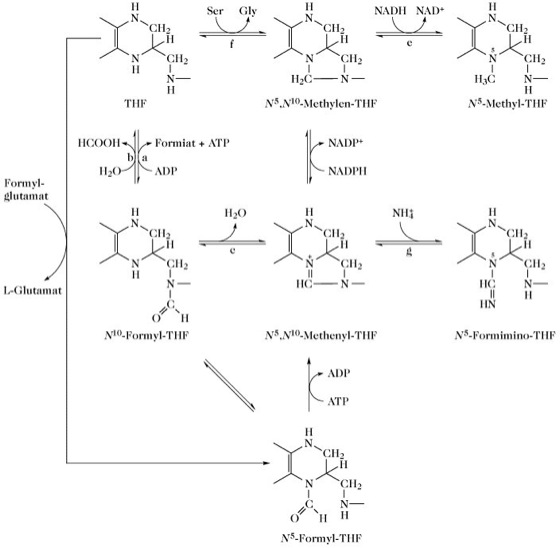
aktive Einkohlenstoff-Einheiten.Abb. 2. Interkonversion aktiver Einkohlenstoff-Einheiten.
Katalysierende Enzyme:
a. Formyl-FH4-Synthetase (EC 6.3.4.3)
b. Formyl-FH4-Deformylase (EC 3.5.1.10)
c. Methenyl-FH4-Cyclohydrolase (EC 3.5.4.9)
d. Methylen-FH4-Dehydrogenase (NADP+) (EC 1.5.1.5)
e. 5,10-Methylen-FH4-Reduktase (FADH2) (EC 1.7.99.5)
f. Serin-Hydroxymethyltransferase (EC 2.1.2.1)
g. Formimino-FH4-Cyclodesaminase (EC 4.3.1.4)
Assoziierte Systeme und Reaktionen:
1. N5-Formimino-FH4 wird aus FH4 und Formiminoglycin (aus der bakteriellen Fermentation der Purine) gebildet, bzw. aus FH4 und Formiminoglutamat (Histidin).
2. In Clostridium dient die Umkehr der Reaktion a dazu, ATP zu erzeugen.
3. N5,10-Methylen-FH4 fungiert sowohl als Reduktionsmittel als auch als Quelle für Einkohlenstoffeinheiten in der Synthese von Thymidylsäure (Pyrimidinbiosynthese).
4. Auch das Glycinspaltungssystem wandelt FH4 in N5,10-Methylen-FH4 um.
5. N5-Methyl-FH4 dient als Methylgruppenquelle für die Umwandlung von L-Homocystein in L-Methionin (5-Methyltetrahydrofolat-Homocystein-Methyltransferase, EC 2.1.1.13) (L-Methionin).
6. Die Wirkung der Enzyme EC 2.1.2.2 und 2.1.2.3 wird bei dem Stichwort Purinbiosynthese beschrieben.
7. N5-Methyl-FH4 ist ein Substrat der Methanbildung in methanogenen Bakterien.
8. Andere wichtige Reaktionen: Einkohlenstoffzyklus.
THF und FH4 sind beides allgemein verwendete Abkürzungen für die Tetrahydrofolsäure.
Wenn Sie inhaltliche Anmerkungen zu diesem Artikel haben, können Sie die Redaktion per E-Mail informieren. Wir lesen Ihre Zuschrift, bitten jedoch um Verständnis, dass wir nicht jede beantworten können.