Lexikon der Biochemie: Chiralität
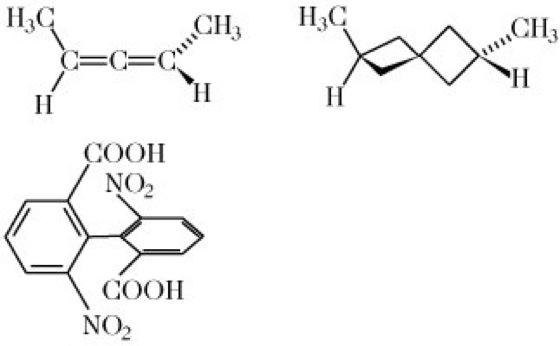
Chiralität, Bezeichnung für die topologische Eigenschaft eines Moleküls, sich wie Bild und Spiegelbild (Enantiomere) zueinander zu verhalten, die nicht miteinander zur Deckung gebracht werden können. Diese Inkongruenz von Molekül und Spiegelbild liegt vor, wenn das betreffende Molekül weder eine Spiegelebene (σ), noch ein Inversionszentrum (i), noch eine Drehspiegelachse (Sn) aufweist. (Eine einfache Drehachse (Cn) kann vorhanden sein.) Die Eigenschaft der Händigkeit (Chiralität), ist ein notwendiges und hinreichendes Kriterium für die Existenz von Enantiomeren und damit für optische Aktivität. Über die Beziehungen zwischen Symmetrie, Chiralität und optischer Aktivität informiert die Tabelle. Die Chiralität einer Verbindung wird durch ein Chiralitätselement bewirkt. Die überwiegende Mehrzahl aller optisch aktiven, also chiralen Verbindungen enthält ein asymmetrisches Kohlenstoffatom, d.h. ein Kohlenstoffatom mit vier verschiedenen Substituenten, als Chiralitätszentrum bzw. stereogenes Zentrum. Glycerinaldehyd, Milchsäure und Weinsäure sowie fast alle Naturstoffe, z.B. Kohlenhydrate, Eiweiße, Steroide und Alkaloide, enthalten asymmetrische Kohlenstoffatome (Abb. 1). Daneben können auch andere asymmetrisch substituierte Zentralatome Chiralitätszentren sein, z.B. Silicium in Silanen, Stickstoff in quartären Ammoniumsalzen und Aminoxiden, Schwefel in Sulfoxiden sowie Metallatome (M) in Komplexverbindungen (Abb. 2). Chiralitätsachsen enthalten entsprechend substituierte Allene, Spirane und Diphenylderivate (Abb. 3).
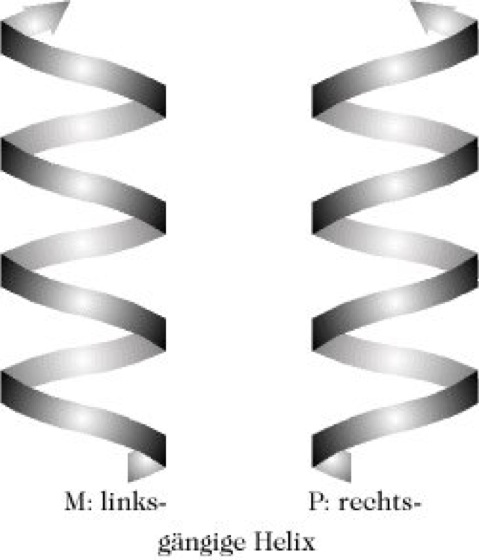
Die Helizität ist ein Sonderfall der axialen Chiralität, bei der die Enantiomerie durch den Schraubensinn einer Achse mit Gang charakterisiert ist. Eine rechtsgängige Helix beschreibt längs ihrer Achse eine Rechtsdrehung (Konfigurationsbezeichnung P für plus), eine linksgängige Helix eine Linksdrehung (Konfigurationsbezeichnung M für minus; Abb. 4).
Chirale Moleküle drehen die Polarisationsebene von linear polarisiertem Licht beim Durchtritt durch die Lösung im gleichen Winkel, aber in entgegengesetzten Richtungen (optische Aktivität der Moleküle).
Biologisch interessant ist die Chiralität der Aminosäuren. In der Natur kommen im Allgemeinen nur L-Aminosäuren vor. Auch der unterschiedliche Geruch von Orangen und Zitronen ist nur auf die Chiralität des Duftstoffs Limonen zurückzuführen. Bei Arzneimitteln ist meist nur eine der beiden enantiomeren Formen pharmazeutisch wirksam. Die andere zeigt entweder keine Wirkung oder ist sogar für die Nebenwirkungen des Medikaments verantwortlich. Dies war z.B. bei Thalidomid (Contergan R) der Fall.
Chiralität. Tab. Beziehungen zwischen Symmetrie, Chiralität und optischer Aktivität.
| ||||
| achiral, symmetrisch | + | + | – | |
| chiral, axial symmetrisch | + | – | + | |
| chiral, asymmetrisch | – | – | + |
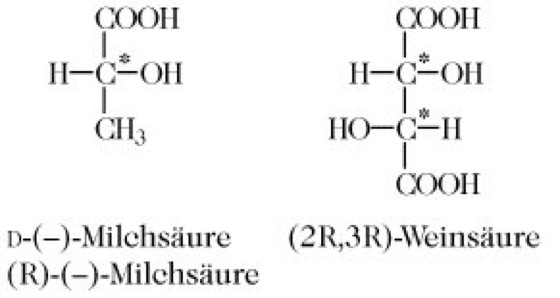
Chiralität. Abb. 1. Asymmetrische Kohlenstoffatome (durch * gekennzeichnet) als Chiralitätszentren.
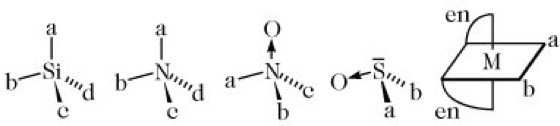
Chiralität. Abb. 2. Si, N, S und M als Chiralitätszentren
Wenn Sie inhaltliche Anmerkungen zu diesem Artikel haben, können Sie die Redaktion per E-Mail informieren. Wir lesen Ihre Zuschrift, bitten jedoch um Verständnis, dass wir nicht jede beantworten können.