Lexikon der Biochemie: Desoxyribonuclease I
Desoxyribonuclease I, DNase I (EC 3.1.21.1.), ein Enzym (das gewöhnlich aus Rinderpankreas erhalten wird und deshalb auch als Pankreasdesoxyribonuclease bekannt ist), das eine zufällige endonucleolytische Spaltung von Internucleotidbindungen in doppelsträngiger DNA katalysiert, und zwar bevorzugt, aber nicht ausschließlich zwischen benachbarten Purinen und Pyrimidinen, unter Bildung von 5'-Phospodi- oder -oligonucleotiden.
Zur Aktivität wird ein zweiwertiges Kation benötigt (ein Bedarf, den die DNase I mit allen anderen Enzymen gemein hat, die die Phosphorylübertragung katalysieren); für in-vitro-Untersuchungen wird normalerweise Ca2+ verwendet, in vivo ist jedoch Mg2+ möglicherweise wichtiger. Röntgenstrukturuntersuchungen zeigen, dass das zweiwertige Kation in der Nähe der gespaltenen Phosphodiesterbindung gebunden vorliegt, die sich ebenfalls in unmittelbarer Nähe von Glu75, His131 und einem gebundenen Wassermolekül befindet und auf diese Weise eine Glu-His-H2O-Triade bildet (Abb.). Diese Triade erinnert stark an das Protonenrelais in Chymotrypsin und anderen Serinproteasen.
Die DNase I wird in Laborexperimenten eingesetzt, bei denen zwischen DNA-Bereichen unterschieden wird, die an spezifische Proteine gebunden sind (und deshalb durch diese geschützt werden) und solchen, die diese Bindung nicht aufweisen (Footprinting). DNase I bildet mit G-Actin einen 1:1-Komplex (weshalb Actin ein natürlicher und spezifischer Inhibitor der DNase I ist), der zusammen mit einem Ca2+-Ion und einem Molekül ATP oder ADP kristallisiert werden kann.
Ähnliche Enzyme, die aus anderen Quellen stammen, sind: Streptokokken-DNase (Streptodornase), E.-coli-Endonuclease, das "Nicking"-Enzym aus Kalbsthymus, T4-Endonuclease II, T7-Endonuclease II, die Colicine E2 und E3.
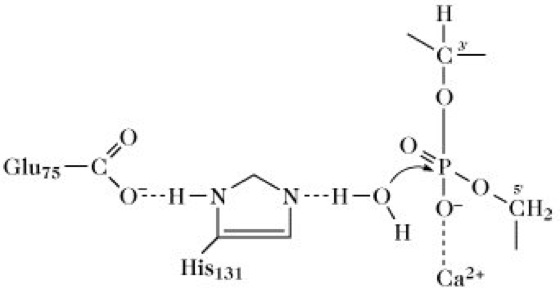
Desoxyribonuclease I. Katalyse der Phosphodiesterspaltung durch das Protonenrelais der DNase I. Durch die Übertragung eines Protons vom Wasser auf His131 entsteht auf der Imidazolseitenkette eine positive Ladung, die durch die negative Ladung der Carboxylgruppe von Glu75 stabilisiert wird. Das Hydroxidion greift das P-Atom an und es bildet sich eine fünfbindige Zwischenstufe, die durch elektrostatische Wechselwirkung des negativ geladenen O-Atoms mit dem zweiwertigen Kation stabilisiert wird. Durch den nachfolgenden Abgang der 3'-OH-Gruppe wird der DNA-Strang gespalten und es bleibt eine endständige 5'-Phosphatgruppe zurück.
Wenn Sie inhaltliche Anmerkungen zu diesem Artikel haben, können Sie die Redaktion per E-Mail informieren. Wir lesen Ihre Zuschrift, bitten jedoch um Verständnis, dass wir nicht jede beantworten können.