Lexikon der Biochemie: Ramachandran-Diagramme
Ramachandran-Diagramme, Raumkonturdiagramme, Konformationsdiagramme, Diagramme, in denen die Bindungswinkel der Cα-CCarbonyl- (Ψ-) Bindung einer Peptidbindung gegen den Bindungswinkel der Cα-N-(Φ-)Bindung aufgetragen sind (Abb.). Ein allgemeines R. wird mit Hilfe von Modellen und Computern erstellt. Unter Verwendung der allgemein anerkannten Atomradien von C, N, O und H werden mögliche Kombinationen der beiden Winkel (d.h. Bereiche ohne sterische Hinderung) durch schraffierte Flächen im Diagramm angezeigt. Wenn die Berührungsabstände geringfügig verkleinert werden, dehnen sich diese zulässigen Bereiche weiter aus und es ergeben sich neue zulässige Konformationen. Folgende sterisch erlaubten Konformationen liegen in den Bereichen: antiparallele β-Faltblätter, parallele β-Faltblätter, Polyprolin-Helix, Kollagen-Superspiralisierung, rechts- und linksgängige α-Helices, rechtsgängige ω-Helix, 310-Dreifachhelix und π-Helix (4,4 Reste je Umdrehung). Für ein bestimmtes Protein kann ein R. aus den Ψ- und Φ-Werten konstruiert werden, welche experimentell durch Röntgenbeugung und Modelle ermittelt wurden. [G.N. Ramachandran Aspects of Protein Structure, Academic Press (1963) 39]
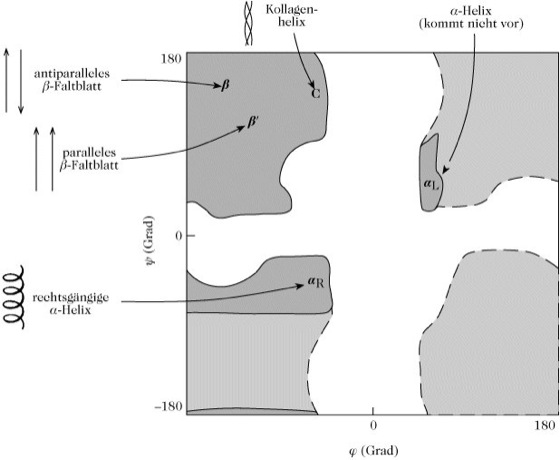
Ramachandran-Diagramm. Ramachandran-Diagramm von Polyalanin mit den erlaubten Bereichen von Ψ und Φ für Alaninreste (schraffiert). Zum Vergleich sind die erlaubten Bereiche von Glycin (grau) gezeigt, das außerhalb der Bereiche von Alanin (und der anderer Aminosäuren) auftritt, weil es eine sehr kleine Seitenkette (H) besitzt und deshalb viele Konformationen einnehmen kann.
Wenn Sie inhaltliche Anmerkungen zu diesem Artikel haben, können Sie die Redaktion per E-Mail informieren. Wir lesen Ihre Zuschrift, bitten jedoch um Verständnis, dass wir nicht jede beantworten können.