Lexikon der Biochemie: Thiaminpyrophosphat
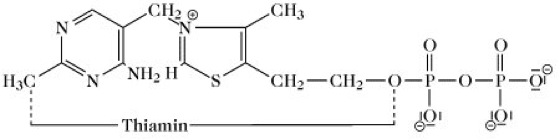
Thiaminpyrophosphat, TPP, Aneurinpyrophosphat, APP, Cocarboxylase, Diphosphothiamin, der Pyrophosphorsäureester von Thiamin (Abb. 1), die prosthetische Gruppe (bzw. das Coenzym) verschiedener Thiaminpyrophosphatenzyme, z.B. der Pyruvat-Decarboxylase, des Pyruvat-Dehydrogenase- und α-Ketoglutarat-Dehydrogenase-Komplexes, der Transketolase, der Glyoxylat-Carboligase und der Oxalyl-CoA-Decarboxylase (Oxalsäure). Das freie Kation des T. weist ein Mr von 425,3Da auf, das Chlorid (Mr 460,8Da) kristallisiert mit einem Molekül Wasser aus Ethanol (Mr 478,8Da); F. 240-244°C (Zers.); λmax 245 und 261nm (in Phosphatpuffer bei pH 5,0), 231,5 und 266nm (bei pH 8,0); λmin 248nm.
T. bildet mit den Substraten der Thiaminpyrophosphatenzyme aktive Aldehyde: 1) aktiver Acetaldehyd (Hydroxyethylthiaminpyrophosphat, HETPP);
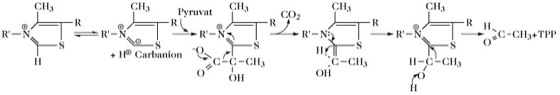
2) aktiver Glycolaldehyd [2-(1,2-Dihydroxyethyl)-thiaminpyrophosphat, DETPP]; 3) aktiver Formaldehyd (2-Hydroxymethylthiaminpyrophosphat, HMTPP). Als Zwischenprodukte der Bildung aktiver Aldehyde werden aktives Pyruvat (Pyruvylthiaminpyrophosphat) und aktives Glyoxylat [2-(Hydroxycarboxymethyl)-thiaminpyrophosphat] postuliert. Das Wasserstoffatom in Position 2 des Thiazoliumrings von T. (zwischen dem Schwefel- und dem Stickstoffatom; Abb. 2) besitzt eine hohen pK-Wert von ungefähr 12,6. Vermutlich ist das dipolare Thiazoliumion (das Ylid; d.h. das C2 bildet ein Carbanion, das durch die positive Ladung am Stickstoff stabilisiert wird) das entscheidende Zwischenprodukt in der Coenzymfunktion von T. Das Carbanion an C2 reagiert mit dem (δ+)-C-Atom einer Substratcarbonylgruppe und bildet ein aktives Intermediat. Elektronen können vom gebundenen Substrat in das Ringsystem von T. fließen und die Bindung zwischen dem gebundenen Substrat-C-Atom (dem ursprünglichen Carbonyl-C-Atom) und einem benachbarten C-Atom wird gespalten. Alle Reaktionen, die durch TPP-Enzyme katalysiert werden, sind mit diesem Mechanismus konform.
Wenn Sie inhaltliche Anmerkungen zu diesem Artikel haben, können Sie die Redaktion per E-Mail informieren. Wir lesen Ihre Zuschrift, bitten jedoch um Verständnis, dass wir nicht jede beantworten können.