Kompaktlexikon der Biologie: Aminosäuren
Aminosäuren, Aminocarbonsäuren, Carbonsäuren mit einer oder mehreren Aminogruppen, die entsprechend ihrer Position zur Carboxylgruppe als α-, β-, γ- usw. -Aminosäuren bezeichnet werden. Von wenigen Ausnahmen abgesehen, sind A. in Wasser gut löslich und liegen in wässrigen Lösungen zwischen pH 4 und 9 als Zwitterionen vor ( vgl. Abb. ). Bisher sind aus der belebten Natur über 260 verschiedene A. bekannt, wobei den 20 in Proteinen vorkommenden A. (proteinogene A. ( vgl. Tab. )) besondere Bedeutung zukommt. Diese sind α-A. und besitzen am α-Kohlenstoffatom, mit Ausnahme von Glycin, ein asymmetrisches Zentrum mit L-Konfiguration (asymmetrisches Kohlenstoffatom). Jeder proteinogenen A. sind durch den genetischen Code mindestens ein Codon, meist jedoch mehrere Codonen zugeordnet. Dadurch kann die Sequenz der Codonen von mRNS, die letztlich durch die Nucleotidsequenz der entsprechenden Gene bestimmt wird, in die Reihenfolge der A. (Aminosäuresequenz) der entsprechenden Proteine übersetzt werden (Translation). Die Aktivierung der proteinogenen A. zum Einbau in Proteine erfolgt durch Überführung in die 20 verschiedenen Aminoacyl-Adenylsäuren und Aminoacyl-tRNAs.
Die proteinogenen A. werden in neutrale A. (keine Ladung in der Seitenkette), saure A. (negative Ladung in der Seitenkette) und basische A. (positive Ladung in der Seitenkette) eingeteilt. Innerhalb der neutralen A. wird die Klasse der A. mit hydrophiler (hydrophil) bzw. polarer Seitenkette (Cystein, Serin, Threonin, Tyrosin, Asparagin, Glutamin) von der Klasse der A. mit hydrophober (hydrophob) bzw. apolarer Seitenkette (Alanin, Glycin, Isoleucin, Leucin, Methionin, Phenylalanin, Prolin, Tryptophan, Valin) unterschieden. Phenylalanin, Tryptophan und Tyrosin werden unter dem Begriff der aromatischen A. zusammengefasst. Diese zeigen frei oder gebunden in Proteinen charakteristische UV-Absorption (Absorptionsspektrum) bei 280 nm und bilden damit die Grundlage zur qualitativen bzw. halbquantitativen Bestimmung von Proteinen über die Messung der UV-Absorption. Der Nachweis einzelner freier A. erfolgt besonders durch die Farbreaktion mit Ninhydrin. Diese Reaktion ist spezifisch für α-A. und führt zur Bildung eines blauen Farbstoffs mit für die jeweilige A. charakteristischer Tönung.
Der Mensch und Säugetiere können nicht alle proteinogenen A. selbst aufbauen, sodass ein Teil, die Gruppe der essentiellen A ( vgl. Tab. )., durch die Nahrung aufgenommen werden muss. Die Synthese der proteinogenen A. erfolgt durch Transaminierung der entsprechenden α-Ketosäuren mit Glutamat als Aminogruppen-Donor (Aminogruppe ( vgl. Abb. )). Glutamat selbst entsteht durch direkte reduktive Aminierung von α-Ketoglutarat mit Ammoniak. Beim Abbau werden die proteinogenen A. in einem ersten transaminierenden Schritt zu den entsprechenden α-Ketosäuren umgewandelt, wobei der Aminostickstoff auf α-Ketoglutarat unter Bildung von Glutamat übertragen wird. Letzteres kann durch dehydrierende Desaminierung unter der Wirkung von Glutamat-Dehydrogenase zu Ammoniak und α-Ketoglutarat gespalten werden. Das Gleichgewicht nimmt daher eine Schlüsselstellung bei Aus- und Einschleusung von Ammoniak in die Aminogruppen der A. ein.
Die A. Alanin, Aspartat und Glutamat stehen über ihre Ketosäuren (Pyruvat, Oxalacetat, α-Ketoglutarat) direkt mit dem Citratzyklus in Verbindung. Dazu gehören auch Asparagin und Glutamin, da diese durch Hydrolyse der Säureamidgruppe (Amide) in Aspartat und Glutamat überführt werden können. Die α-Ketosäuren weiterer A. werden durch zusätzliche, zum Teil komplizierte Folgereaktionen in den Citratzyklus eingeschleust und können über den Weg der Gluconeogenese letztlich in Kohlenhydrate (Glucose, Glykogen) umgewandelt werden. Diese Gruppe von Aminosäuren wird daher unter dem Begriff der glucogenen A. oder glucoplastischen A. zusammengefasst. Ihnen gegenüber stehen A., die ebenfalls in Folgereaktionen, ausgehend von den entsprechenden α-Ketosäuren, zu Acetoacetyl-Coenzym A und Acetyl-Coenzym A abgebaut werden und auf diesem Wege in Fettsäuren umgewandelt werden können. Sie können im Zuge dieser Reaktionen auch zu Ketonkörpern wie Acetoacetat (Acetessigsäure) und dessen Decarboxylierungsprodukt Aceton umgesetzt werden und werden deshalb unter dem Begriff der ketogenen A. oder ketoplastischen A. zusammengefasst ( vgl. Tab. ).
Die nichtproteinogenen A. bilden mit den über 240 bisher nachgewiesenen Vertretern die zahlenmäßig größte Gruppe. Sie werden besonders zahlreich in Pflanzen gefunden. Ihre Strukturen sind sehr unterschiedlich. Die L-α -A. überwiegen, jedoch enthält z.B. das Murein-Gerüst (Murein) der Bakterienzellwand die D-α -A. D-Alanin und D-Glutamat, und unter den Nicht-α -Formen sind besonders das β-Alanin und die γ-Aminobuttersäure zu nennen. In vielen Fällen sind nichtproteinogene A. Analoge von proteinogenen A. Aufgrund dieser strukturellen Ähnlichkeit können nichtproteinogene A. als Aminosäureantagonisten wirken und dadurch zu spezifischen Stoffwechselstörungen führen. Auch der bakteriostatischen und Antitumorwirkung des Azaserins (ein von Streptomyces-Stämmen gebildetes cytotoxisches Antibiotikum) liegt ein Aminosäureantagonismus zugrunde. Einige nichtproteinogene A. fungieren als Zwischenprodukte bei Synthese oder Abbau der proteinogenen A. oder als Zwischenprodukte bei der Bildung von Purinen und Harnstoff. Speziell in menschlichen und tierischen Organismen üben einige nichtproteinogene A. spezifische Funktionen aus, wie Dihydroxyphenylalanin und 5-Hydroxytryptophan als Zwischenstufen bei der Bildung von Hormonen und γ-Aminobuttersäure als Neurotransmitter. Insgesamt jedoch sind die physiologischen Funktionen der nichtproteinogenen A. nicht wirklich verstanden. Neben der Schutzwirkung der giftigen, nichtproteinogenen pflanzlichen A. gegenüber Fressfeinden, die jedoch in Einzelfällen durch spezielle biochemische Mechanismen der jeweiligen Fressfeinde aufgehoben sein kann, werden vor allem Depotfunktionen in Betracht gezogen. Nichtproteinogene A. treten in bestimmten Pflanzenfamilien gehäuft auf und eignen sich daher als taxonomische Marker.
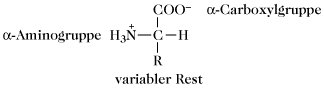
Aminosäuren: Struktur einer α-Aminosäure, die als Zwitterion vorliegt
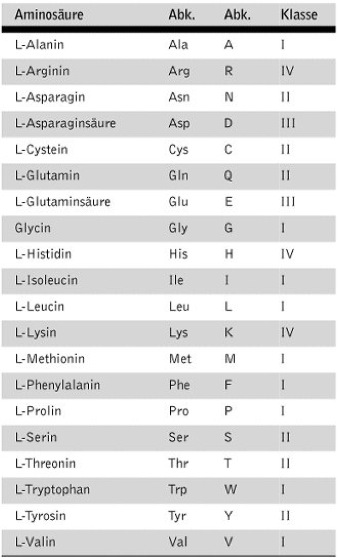
Aminosäuren:Proteinogene Aminosäuren. Die Dreibuchstabenabkürzungen sind allgemein anerkannt und werden routinemäßig für Darstellungen von Protein- und Peptidsequenzen verwendet. Die Einbuchstabenbezeichnungen (vorgeschlagen von der IUPAC-IUB-Kommission für Biochemische Nomenklatur) sollte für Veröffentlichungen von Sequenzen nicht verwendet werden. Es ist jedoch beabsichtigt, diese einzusetzen, um die Speicherung von Sequenzinformationen und die Durchführung von Sequenzvergleichen mit Hilfe des Computers zu erleichtern
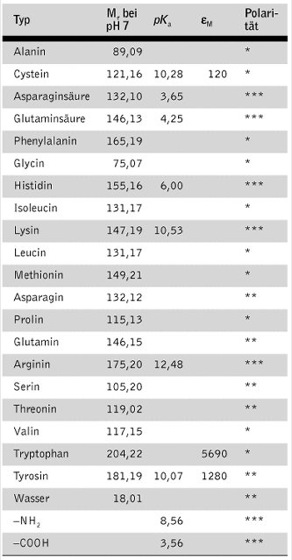
Aminosäuren: Die 20 proteinogenen Aminosäuren mit ihren physikalischen Eigenschaften (relative Molekülmasse Mr, Titrationspunkt pKa der funktionellen Gruppen, Extinktionskoeffizient εM [M-1cm-1] bei 280 nm). Die Polarität wird halbquantitativ durch die Zahl der Sternchen ausgedrückt. Die Zeilen –NH2 und –COOH beziehen sich auf alle Aminosäuren. Wasser ist zum Vergleich aufgeführt
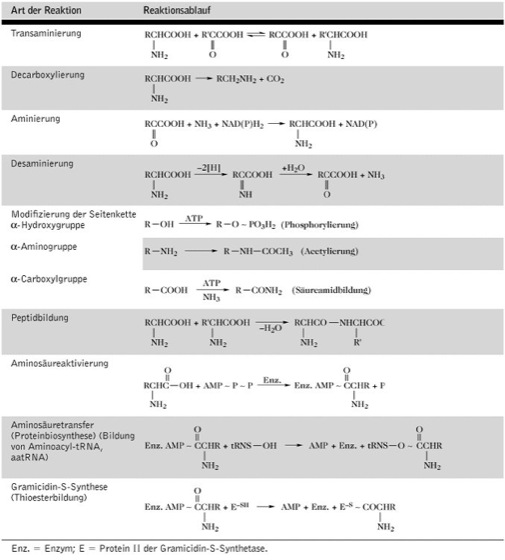
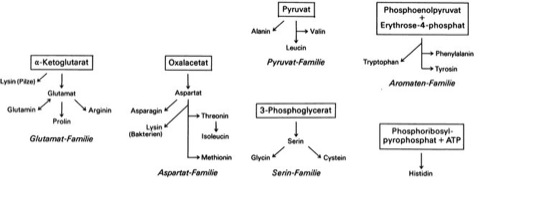
Aminosäuren: Stoffwechselreaktionen der Aminosäuren
Wenn Sie inhaltliche Anmerkungen zu diesem Artikel haben, können Sie die Redaktion per E-Mail informieren. Wir lesen Ihre Zuschrift, bitten jedoch um Verständnis, dass wir nicht jede beantworten können.