Kompaktlexikon der Biologie: DNA-bindende Proteine
DNA-bindende Proteine, Proteine, die über eine DNA-Bindungsdomäne verfügen, mit der eine sequenzspezifische Erkennung von Nucleotidsequenzen einzelsträngiger und doppelsträngiger DNA möglich ist. Sequenzen, an die D.-b.P. binden, lassen sich durch so genannte Bandshift-Assays nachweisen, bei denen die Beeinflussung der Wanderung eines DNA-Fragmentes in einem Gel in Anwesenheit eines Proteingemisches untersucht wird ( vgl. Abb. ). Zur Aufklärung von DNA-Protein-Strukturen hat vor allem die an Kristallen von DNA-Protein-Komplexen durchführbare Röntgenstrukturanalyse beigetragen. Wichtige D.-b.P. sind die prokaryotischen Regulatorproteine und Repressoren (lac-Operon) und die in allen Zellen vorhandenen Transkriptionsfaktoren. Die Fähigkeit der D.-b.P., an DNA zu binden, ist auf eine Reihe so genannter DNA-Bindungsmotive zurückzuführen ( vgl. Abb. ). Hierzu zählt das bei vielen D.-b.P. vorhandene Helix-Turn-Helix-Motiv (HTH-Motiv), das durch zwei winklig zueinander angeordnete α-Helices spezifische Kontakte zur DNA-Doppelhelix vermittelt. Die beiden Helices sind durch vier Aminosäuren voneinander getrennt, ihr Winkel beträgt ca. 120 °. Wichtige D.-b.P. mit HTH-Motiv sind bakterielle Repressoren und das Cro-Protein ( vgl. Abb. ) des Bakteriophagen λ. Auch die so genannte Homöobox zahlreicher an Entwicklungsprozessen beteiligten Gene besitzt dieses Motiv.
Beim Zink-Finger-Motiv spielt Zn2+ eine wichtige Struktur gebende Rolle zahlreicher DNA-Bindungsdomänen, wobei vier Cysteine oder Histidine als Liganden des Zink-Ions fungieren.
Leucin-Zipper (Leucin-Reißverschluss). Bei einer Reihe von D.-b.P. werden Homo- und Heterodimere gebildet, indem zwei antiparallele α-Helices ineinander winden und eine geordnete Anordnung von Leucinen einen Zusammenhalt beider Proteine ermöglicht. Dadurch werden die basische Aminosäuren enthaltenden, ungepaarten Bereiche der Untereinheiten so positioniert, dass sie mit der DNA interagieren können. Diese dimere DNA-Bindungsdomäne wird auch als bZip-Motiv bezeichnet. –Eine weitere wichtige DNA-Bindungsdomäne ist die MADS-Box.

DNA-bindende Proteine: Wichtige Motive in DNA-Bindungsdomänen sind a) Helix-Turn-Helix, b) Zinkfinger und c)Leucin-Zipper (Leucinreißverschluss)
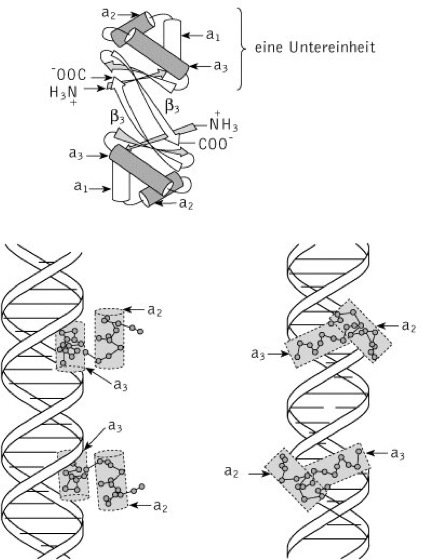
DNA-bindende Proteine: Typische Wechselwirkung zwischen einem DNA-bindenden Protein. Der obere Teil zeigt das Cro-Protein des Phagen λ mit zwei HTH-Motiven. Unten ist die Interaktion mit der großen Furche der Doppelhelix aus zwei verschiedenen Blickwinkeln dargestellt

DNA-bindende Proteine: Nachweis mittels Bandshift-Assay. Bindet ein Protein an die DNA, werden deren elektrophoretische Eigenschaften verändert. Die DNA-Bande wandert langsamer und verursacht dadurch deren Verschiebung („Bandshift“)
Wenn Sie inhaltliche Anmerkungen zu diesem Artikel haben, können Sie die Redaktion per E-Mail informieren. Wir lesen Ihre Zuschrift, bitten jedoch um Verständnis, dass wir nicht jede beantworten können.