Kompaktlexikon der Biologie: Enzyme
Enzyme, Biokatalysatoren, veraltete Bez. Fermente. Überwiegend Proteine (Ausnahme ist z.B. katalytisch wirksame RNA, Ribozyme), die in lebenden Organismen als Katalysatoren an fast allen chemischen Umsetzungen beteiligt sind, indem sie die für den Ablauf jeder chemischen Reaktion erforderliche Aktivierungsenergie herabsetzen. Dadurch bringen sie bereits unter den in lebenden Zellen herrschenden Bedingungen chemische Reaktionen in Gang, die sonst nur unter nichtphysiologischen Bedingungen mit merklicher Geschwindigkeit abliefen. Gegenüber der nicht katalysierten kann die katalysierte Reaktion um den Faktor 103-106 beschleunigt sein. Da sich Stoffwechselvorgänge aus zahlreichen Einzelreaktionen zusammensetzen, von denen jede durch ein bestimmtes, für jede Einzelreaktion spezifisches E. katalysiert wird, sind E. von fundamentaler Bedeutung für den Ablauf des gesamten Zellstoffwechsels.
Biosynthese, Struktur und Kompartimentierung: Die Synthese der Enzymproteine erfolgt wie bei allen Proteinen über Translation. Ständig gebildete E. werden als konstitutive E. bezeichnet, hingegen sind adaptive E. solche, die nur bei Bedarf gebildet werden. Die Regulation der E.-Synthese erfolgt meist auf der Ebene der Transkription (Enzyminduktion), doch gibt es auch Beispiele für Regulation auf der Ebene der Translation (z.B. bei bestimmten RNA-Phagen).
Enzymproteine können monomer sein, d.h. aus einer Polypeptidkette oder oligo- bzw. multimer sein, also aus mehreren Polypeptideinheiten bestehen. Monomere E. sind meist E., die von den produzierenden Zellen in den extrazellulären Raum ausgeschieden werden (z.B. Verdauungsenzyme), während multimere E. überwiegend zelluläre E. sind. Letztere bestehen entweder aus mehreren gleichen (z.B. Aspartat-Transcarbamylase) oder aber aus verschiedenen Peptiduntereinheiten (Ribulose-1,5-bisphosphat-Carboxylase/Oxygenase). Viele E. besitzen neben dem Proteinanteil, dem Apoenzym, auch nicht proteinogene Gruppen (Coenzyme, so z.B. Vitamine oder Nucleotide), die an das Apoenzym entweder über schwache Wechselwirkungen bzw. vorübergehend, oder aber kovalent gebunden sind (prosthetische Gruppe). Als Cofaktoren treten darüber hinaus noch als Spurenelemente bekannte Metalle (u.a. Eisen, Kupfer, Magnesium, Mangan, Zink) in Erscheinung, die als Elektronenakzeptoren dienen. Apoenzym und Coenzym ergeben zusammen das Holoenzym.
Als Enzymsysteme werden Gruppen von E. zusammengefasst, durch die zusammengehörige, mehrstufige Reaktionsfolgen katalysiert werden, so z.B. das Enzymsystem der Glykolyse. Sie können aber auch, wie im Fall des Fettsäure-Synthetase-Komplexes, durch Zusammenlagerung mehrerer Enzyme zu einem größeren Verband als Multienzymkomplexe vorliegen. Enzymsysteme sind i.d.R. in bestimmten Kompartimenten in der Zelle lokalisiert, so z.B. die Enzyme der Glykolyse im Cytoplasma, diejenigen des Citratzyklus in den Mitochondrien und diejenigen des Calvin-Zyklus in den Chloroplasten. Innerhalb der Kompartimente kann unterschieden werden zwischen frei im Plasma beweglichen Enzymen und solchen, die in den entsprechenden Membranen verankert sind, wie z.B. die Enzyme der Atmungskette in der Mitochondrienmembran ( vgl. Abb. ). Membrangebundene Enzyme können jedoch innerhalb der Membranschicht, an die sie gebunden sind, diffundieren und mit anderen membrangebundenen Enzymen interagieren.
In verschiedenen Individuen der gleichen Art, in verschiedenen Organen eines Individuums oder sogar in den verschiedenen Kompartimenten einer Zelle kommen E. vor, die zwar die gleiche Reaktion katalysieren, aber (meist geringe) Unterschiede in der Proteinstruktur und/oder den kinetischen Eigenschaften aufweisen; sie werden als Isoenzyme bezeichnet.
Wirkungsmechanismus: Als Katalysatoren erhöhen E. immer die Geschwindigkeiten von Hin- und Rückreaktion, so dass unter der Wirkung von Enzymen lediglich die Geschwindigkeit der Gleichgewichtseinstellung erhöht wird, jedoch die Lage des Gleichgewichts keine Änderung erfährt. Die unter der Wirkung des E. umgewandelte chemische Verbindung wird als Substrat bezeichnet. Dieses wird vorübergehend während der Umsetzung am aktiven Zentrum des E. unter Ausbildung eines Enzym-Substrat-Komplexes gebunden. Substrat und aktives Zentrum eines E. sind zueinander komplementär, d.h. sie passen wie Schlüssel und Schloss ineinander, weshalb jedes E. aus der Vielzahl der in der Zelle auftretenden Moleküle das jeweils passende Substrat, und nur dieses, binden und umsetzen kann (Substratspezifität). Zwei E. können aber auch dasselbe Substrat umsetzen, katalysieren jedoch verschiedene Reaktionen dieses Substrats, sodass unterschiedliche Endprodukte entstehen (Wirkungsspezifität). Während die Substratspezifität vorwiegend auf der Wechselwirkung zwischen Substrat und aktivem Zentrum beruht, ist für die Wirkungsspezifität auch die Wechselwirkung zwischen Substrat und Coenzym von Bedeutung; dies insbesondere, da Coenzyme häufig, einhergehend mit der Umsetzung des Substrats, selbst zyklische Reaktionen durchlaufen. Sie werden deshalb häufig auch als Cosubstrat bezeichnet.
Bei Bildung des Enzym-Substrat-Komplexes wird durch Wirkung des Enzyms die Elektronenverteilung im Substrat derart verändert, dass es zu einem Übergangszustand kommt, der als der Zustand mit der höchsten Energie auf dem Weg vom Substrat zum Produkt zu verstehen ist. Je nach Funktion des Enzyms werden dabei bestimmte chemische Bindungen selektiv beeinflusst, was zur Bildung des Produktes führt. Der entstehende Enzym-Produkt-Komplex ist wiederum infolge der spezifischen Eigenschaften des Enzyms sehr unbeständig und dissoziiert unmittelbar in Produkt und Enzym, welches dann für einen neuen Reaktionszyklus bereit ist.
Enzymkinetik: Neben den strukturellen Eigenschaften und der Substrat- bzw. Wirkungsspezifität sind die kinetischen Eigenschaften sowie Hemmbarkeit oder Stimulierung durch bestimmte Substanzen charakteristische Kenngrößen von E. Misst man bei vorgegebener konstanter Enzymmenge die Geschwindigkeit (Menge des umgesetzten Substrats pro Zeiteinheit) der betreffenden Reaktion in Abhängigkeit von der Substratkonzentration, so steigt zu Anfang die Reaktionsgeschwindigkeit proportional zur Substratkonzentration und erreicht schließlich eine Maximalgeschwindigkeit, die unabhängig von steigenden Substratkonzentrationen wird (Sättigungskurve). Die aus dieser Kurve abzuleitende mathematische Beziehung ist die Michaelis-Menten-Gleichung. Sie enthält zwei Größen, die nicht von der Substratkonzentration abhängen, sondern Eigenschaften des Enzyms charakterisieren: die Maximalgeschwindigkeit sowie die Michaelis-Konstante, die die Affinität des Enzyms zu seinem Substrat kennzeichnet. Bei allosterischen Enzymen (allosterische Regulation) zeigt die Abhängigkeit der Reaktionsgeschwindigkeit von der Substratkonzentration einen charakteristischen sigmoiden Verlauf. Ein weiterer kinetischer Parameter zur Charakterisierung von Enzymen ist die Wechselzahl. Sie gibt die Anzahl von Substratmolekülen an, die von einem Enzymmolekül pro Minute umgesetzt werden kann.
Die Enzymaktivität ist innerhalb gewisser Grenzen abhängig von den äußeren Testbedingungen, wie Temperatur, pH-Wert u.a. Parameter. Dies ist einerseits von praktischer Bedeutung für die standardisierte Messung von Enzymaktivitäten, spiegelt aber auch die Bedingungen wider, unter denen die Enzyme in der Zelle aktiv sind. Als international gebräuchliche Einheit für die Enzymaktivität wurde ursprünglich die Enzymeinheit (1 U) definiert, das ist diejenige Menge Enzym, die unter Standardbedingungen 1 μmol Substrat pro Minute umsetzt. Nach der heute gültigen Empfehlung der IUPAC ist die Einheit der Enzymaktivität das Katal (Symbol kat), das ist diejenige Enzymmenge, die 1 Mol Substrat pro Sekunde umsetzen kann. Da diese Einheit jedoch sehr groß ist, werden für gängige Enzymmengen die Einheiten μkat, nkat oder pkat verwendet. Für die Umrechnung zwischen den Einheiten gilt: 1 kat = 6 x 107 U bzw. 1 U = 16,67 nkat. Von praktischer Bedeutung sind außerdem die spezifische Aktivität von E., definiert als Enzymeinheiten pro mg Protein bzw. als Katal pro kg Protein (kat/kg), die molare Aktivität von E., die identisch ist mit der Wechselzahl und die Konzentration von E. als Enzymeinheiten pro ml bzw. als Katal pro Liter.
Enzymhemmung und Enzymaktivierung: E. reagieren auf Änderungen z.B. der Temperatur, des pH-Wertes oder des Redoxpotenzials, der Substrat- und Produktkonzentration sowie auf die Anwesenheit bestimmter Ionen oder Verbindungen sehr empfindlich. Eine irreversible Hemmung (Enzymvergiftung) kann durch so genannte Enzymblocker (Enzymgifte) verursacht werden. So werden viele schwermetallhaltige E. (z.B. diejenigen der Atmungskette) durch Cyanide irreversibel gehemmt. Die reversible Hemmung von E.-Aktivitäten durch so genannte Enzyminhibitoren kann nach verschiedenen Mechanismen verlaufen. ( vgl. Abb. ) Nach dem Prinzip der kompetitiven Hemmung geschieht dies durch Moleküle, die aufgrund struktureller Ähnlichkeit mit dem Substrat zwar im aktiven Zentrum binden, damit aber den Zugang für die Substratmoleküle versperren. Bei der unkompetitiven Hemmung bindet der Inhibitor an den Enzym-Substrat-Komplex und verhindert dadurch die weitere Reaktion. Die nichtkompetitive Hemmung wiederum funktioniert nach dem Prinzip der allosterischen Hemmung (allosterische Regulation), d.h. ein Effektor verändert die Konformation des Enzyms und dadurch auch die katalytische Aktivität. Als Spezialfall der kompetitiven Hemmung ist die Endprodukt-Hemmung aufzufassen, bei der das Produkt das Substrat aus dem aktiven Zentrum verdrängt. – Eine unspezifische, meist irreversible Hemmung der E.-Aktivität erfolgt durch Denaturierung (z.B. bei Temperaturen über 50 °C, extremen pH-Werten, Einwirkung von Detergentien).
Reversible Aktivierung von E. geschieht zum einen durch allosterisch wirkende Effektoren. Zum anderen kann die posttranslationale Modifizierung eines Enzyms (z.B. die Abspaltung einer Peptidkette) durch andere Enzyme zur Aktivierung oft ganzer Enzymkaskaden dienen (z.B. bei Verdauungsenzymen). Die Aktivität der E. eines Reaktionstyps wird durch die Regulation der Genexpression unter Kontrolle äußerer Signale (z.B. Hormone) gesteuert.
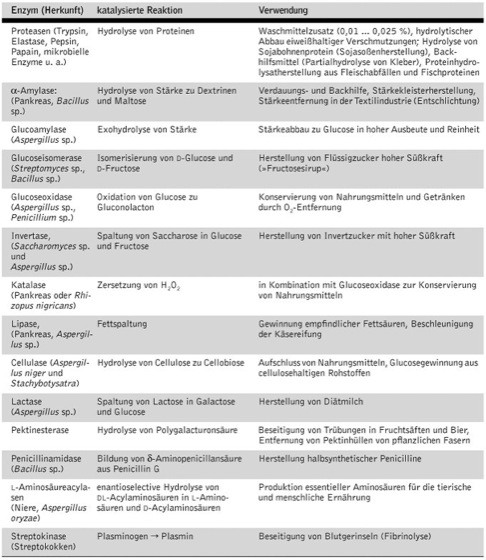
Klassifizierung der E.: Die gegenwärtig bekannten mehr als 2500 E. können nach verschiedenen Kriterien klassifiziert werden (Vorkommen in der Natur, Funktion im Stoffwechsel, funktionelle Gruppen, physikalische Eigenschaften usw.). Durchgesetzt hat sich das auf der Wirkungsspezifität beruhende internationale Einteilungssystem (EC-Nomenklatur, Abk. von enzyme commission). Danach erhält jedes E. eine vierstellige Codenummer, die die Hauptgruppe oder Klasse (Enzymklasse), die Gruppe, die Untergruppe und die Seriennummer festlegt. ( vgl. Tab. )
Zur Reindarstellung von E. aus Zellmaterial stehen heute eine Reihe von Standardmethoden (u.a. Chromatographie, differenzielle Zentrifugation, fraktionierte Fällung, Ultrafiltration) zur Verfügung. Mit Hilfe gentechnologischer Verfahren (Gentechnologie) können inzwischen auch schwer isolierbare oder nur in geringen Mengen vorkommende E. sowie komplizierte E.-Systeme zugänglich gemacht werden. Im großtechnischen Maßstab eingesetzte E. werden meist mit Hilfe von Mikroorganismen in Fermentern gewonnen (Biotechnologie). Die Vorzüge der E.-Katalyse, wie besonders schonende Bedingungen, hohe Wirkungsspezifität für komplizierte, chemisch oft sehr aufwendige Reaktionen sowie hohe Ausbeute und Reinheit der Produkte werden in zunehmendem Maße industriell genutzt (Enzymtechnologie). ( vgl. Tab. ) Ein bedeutender Fortschritt in der Enzymtechnologie wurde durch die Immobilisierung von E. erreicht; hierbei werden ursprünglich lösliche E. durch Bindung an organische oder anorganische Träger unlöslich gemacht (immobilisierte E.). Die Vorteile sind kontinuierliche und wiederholte Verwendung, höhere Stabilität und Wegfall der Diffusionsbarriere. Immobilisierte E. werden z.B. bei der Herstellung preisgünstiger Süßungsmittel aus Glucose verwendet. Eine Alternative zu den immobilisierten E. ist der Einsatz von Enzym-Membran-Reaktoren in der Biotechnologie, bei denen das verwendete E. mit Hilfe geeigneter Membranen im Reaktionsraum zurückgehalten wird. In der Medizin sind Enzymimmunoassays von Bedeutung, die E. als Marker für immunologische Reaktionen verwenden und eine schnelle Konzentrationsbestimmung von Hormonen, Immunglobulinen, Antigenen, Drogen u.a. ermöglichen.
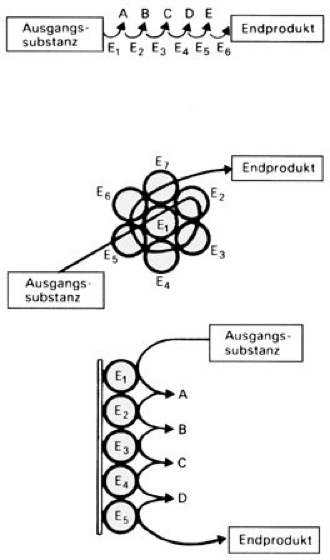
Enzyme: Typen räumlicher Anordnung von Enzymen in der Zelle: Abb. oben: frei im Plasma liegende Enzyme (z.B. Glykolyse); das Produkt der einen Enzymreaktion ist Substrat für die nächste Reaktion. E-E sind diffundierende Zwischenprodukte. Mitte: Multienzymkomplex (z.B. Fettsäuresynthese). Unten: membrangebundene Enzyme (z.B. Atmungskette)
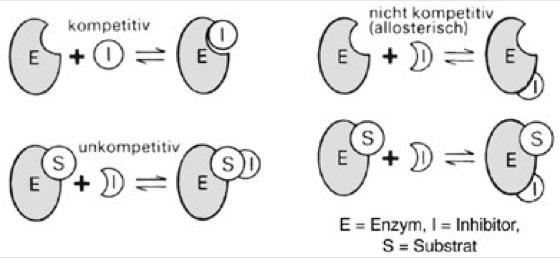
Enzyme: Typen der Enzymhemmung (Erläuterung siehe Text)

Wenn Sie inhaltliche Anmerkungen zu diesem Artikel haben, können Sie die Redaktion per E-Mail informieren. Wir lesen Ihre Zuschrift, bitten jedoch um Verständnis, dass wir nicht jede beantworten können.