Kompaktlexikon der Biologie: Fettsäuren
Fettsäuren, gesättigte und ungesättigte aliphatische Monocarbonsäuren. Die Bez. F. ist auf das Vorkommen zahlreicher F. in den Fetten zurückzuführen. Diese F. sind meist geradzahlige, gesättigte oder ungesättigte, überwiegend unverzweigte Monocarbonsäuren. In der Natur vorkommende ungesättigte F. liegen in der Z-Konfiguration vor. In mehrfach ungesättigten F. sind die Ethengruppierungen durch CH2-Gruppen getrennt, d.h. sie sind nicht konjugiert. Kurzkettige F. von C4 bis C10 sind hauptsächlich in den Milchfetten der Säugetiere enthalten. Palmitin- und Stearinsäure (16 bzw. 18 C-Atome) kommen in nahezu allen tierischen und pflanzlichen Fetten vor. Langkettige F. sind in den Hirnlipiden und in Wachsen zu finden. Die am häufigsten vorkommende ungesättigte F. ist die Ölsäure. In verschiedenen pflanzlichen fetten Ölen und Fischleberölen sind auch mehrfach ungesättigte F., wie z.B. Linol- und Linolensäure enthalten, besonders im Leinöl. Diese mehrfach ungesättigten Säuren gehören zu den essenziellen F., die für den Menschen und für höhere Tiere zur Aufrechterhaltung der normalen Körperfunktionen lebensnotwendig sind und vom Organismus nicht synthetisiert werden können, sondern mit der Nahrung aufgenommen werden müssen. Sie haben Vitamincharakter und werden als Vitamin F bezeichnet.
Fettsäurebiosynthese: Bei dieser durch die Fettsäure-Synthase katalysierten Reaktionsfolge wird schrittweise aus C2-Einheiten (die von Malonylgruppen stammen, mit anschließender Decarboxylierung) die Fettsäure-Kohlenstoffkette aufgebaut. Die Zwischenprodukte der Fettsäurebiosynthese sind Thioester des Acyl-Carrier-Proteins (ACP) und des Coenzyms A wie beim Fettsäureabbau. Malonyl-CoA wird durch eine biotinabhängige Carboxylierung (Biotin) von Acetyl-CoA synthetisiert. Die Malonylgruppe wird sodann von Malonyl-CoA auf das ACP übertragen, wo sie eine Thioesterbindung mit der SH-Gruppe des kovalent gebundenen 4-Phosphopantetheins eingeht. ( vgl. Abb. ) Dieser Phosphopantetheinarm dient als Träger für Substrate und Zwischenprodukte, die anschließend durch die anderen Aktivitäten der Fettsäure-Synthase auf ihn übertragen werden. Jede neu gebildete Acylgruppe wird vom Phosphopantetheinarm auf die SH-Gruppe eines Cysteinylrests der β-Ketoacyl-Synthetase übertragen. Anschließend wird die nächste Malonylgruppe an das frei gewordene zentrale Thiol gebunden und ein neuer Reaktionszyklus (Kondensation, Reduktion, Dehydratisierung, Reduktion) erweitert die Acylgruppe um zwei weitere Kohlenstoffatome. Diese Zyklen werden wiederholt, bis ein Palmitoylrest (C16) entstanden ist, der dann entweder als freie Säure oder als Fettsäureacyl-CoA freigesetzt wird, abhängig davon, ob das System eine Thioesterase oder eine CoA-Transacylase besitzt.
Bei den meisten Bakterien und in den Chloroplasten sind das ACP und die Enzyme der Fettsäurebiosynthese diskrete Proteine, die in einem Multienzymkomplex nichtkovalent assoziiert sind (Fettsäure-Synthase Typ II). Dagegen besteht die Fettsäure-Synthase bei Tieren (Typ I) aus einem Dimer eines einzelnen multifunktionellen Proteins. Die Fettsäure-Synthase der Hefe ist ein Zwischentyp.
Bei Tieren läuft die Fettsäurebiosynthese im Cytoplasma ab. Acetyl-CoA als Startsubstanz wird in den Mitochondrien mit Hilfe der Pyruvat-Dehydrogenase (Multienzymkomplex) produziert. Für jedes Acetyl-CoA, das von den Mitochondrien in das Cytosol transportiert wird, wird ein NADPH erzeugt. Bei der Umwandlung von acht Molekülen Acetyl-CoA in Palmitat werden acht der benötigten 14 NADPH-Moleküle durch die Malat-Dehydrogenase zur Verfügung gestellt. Die restlichen sechs NADPH liefert der Pentosephosphatzyklus. Der geschwindigkeitsbestimmende Schritt in der Synthese von Fettsäuren aus Acetyl-CoA ist die Synthese von Malonyl-CoA, die durch die Acetyl-CoA-Carboxylase katalysiert wird. Citrat und Isocitrat aktivieren das Enzym; Palmitoyl-CoA ist Antagonist des Citrateffekts, indem es den Carrier inhibiert, der Citrat durch die Mitochondrienmembran schleust.
Die Spezifität der β-Ketoacyl-ACP-Synthase bewirkt, dass das Enzym normalerweise Fettsäuregruppen bis zu einer Kettenlänge von C14 bindet, d.h. Palmitat bzw. Palmitoyl-CoA wird als Endprodukt der Fettsäuresynthese freigesetzt. Die Kettenlänge kann mit Hilfe von so genannten Elongationsreaktionen verlängert werden, die sich bei tierischen Organismen in den Mitochondrien und im endoplasmatischen Reticulum abspielen. Bei Bakterien und Pflanzen läuft die Elongation durch Fortführung der Reaktionen der Fettsäurebiosynthese über C16 hinaus, wobei Synthasen unterschiedlicher Spezifität zum Einsatz kommen. Die Bildung ungesättigter F. geschieht durch Desaturierungsreaktionen im endoplasmatischen Reticulum. Bei Säugern fehlen bestimmte Enzymsysteme für diese Reaktionen, sodass Linolsäure, Linolensäure und Arachidonsäure zu den essenziellen F. gehören, da sie nicht synthetisiert werden können. Ungeradzahlige F. können ebenfalls am Fettsäure-Synthase-Komplex gebildet werden, wobei jedoch zur Startreaktion statt Acetyl-CoA Propionyl-CoA (C3-Einheit) übertragen wird. Für die Synthese verzweigter Fettsäuren ist die Einführung verzweigter Startermoleküle oder entsprechender Substrate bei der Elongation notwendig.
Der Fettsäureabbau erfolgt hauptsächlich durch β-Oxidation (Beta-Oxidation). Dies ist ein zyklischer (spiralförmiger) Prozess, durch den die F. schrittweise vom Carboxylende her abgebaut werden. In jeder Runde des Zyklus werden zwei Kohlenstoffatome in Form von Acetyl-CoA abgespalten und das β-Kohlenstoffatom wird oxidiert. ( vgl. Abb. ) Das Acyl-CoA wird durch Acyl-CoA-Dehydrogenase zu 2,3-Dehydroacyl-CoA oxidiert. Diese Verbindung wird hydratisiert und dann oxidiert zu 3-Ketoacyl-CoA. Dieses wird gespalten (thiolytisch), wobei Acetyl-CoA und ein neues Acyl-CoA gebildet werden. Das neue Acyl-CoA ist zwei Kohlenstoffatome kürzer als das ursprüngliche und wird sofort einer weiteren Oxidation unterzogen. In jeder Runde der Fettsäurespirale entsteht ein Molekül Acetyl-CoA, das im Citratzyklus weiter oxidiert wird. Die vollständige Oxidation eines Moleküls Steroyl-CoA erzeugt 148 Moleküle ATP: Aus 18 C-Atomen entstehen 9 Moleküle Acetyl-CoA; 1 Acetyl-CoA ergibt im Citratzyklus 12 Moleküle ATP; zusätzlich werden bei jedem der 8 β-Oxidationsschritte 5 Moleküle ATP gebildet. Die Energie, die am Ende in den Phosphatbindungen von 148 Molekülen ATP gespeichert ist, entspricht 50 % der Verbrennungswärme der Fettsäure.
Bei ungeradzahligen F. führt der Fettsäureabbau zu einer C3-Verbindung, z.B. Propionyl-CoA, die auf einem alternativen Stoffwechselweg metabolisiert werden muss. Zum Abbau verzweigtkettiger F. werden verschiedene Wege beschritten, von denen einige aus dem Stoffwechsel der verzweigtkettigen Aminosäuren stammen. F. mit kurzen Ketten werden in den Mitochondrien in ihr Fettsäureacyl-Derivat überführt; langkettige F. können die innere Mitochondrienmembran nicht durchdringen und müssen in Form des Acyl-Carnitins (Carnitin) in die Mitochondrien transportiert werden.

Fettsäuren: Fettsäurebiosynthese. Die Abb. zeigt die kooperative Aktivität der Proteine der Fettsäure-Synthase, die als Multienzymkomplex oder als einzelnes multifunktionelles Protein vorliegen kann. Die Zickzacklinie stellt den beweglichen Pantetheinarm des Acyl-Carrier-Proteins dar. Der mittlere Kreis repräsentiert das Acyl-Carrier-Protein und die äußeren Kreise die anderen Enzyme. Die rein schematische Darstellung gibt nicht unbedingt die wirkliche Anordnung der Proteine wieder
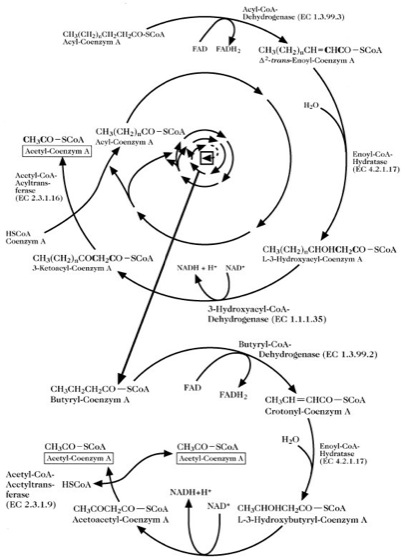
Fettsäuren: Fettsäureabbau. Die Abb. zeigt die Fettsäurespirale der β-Oxidation
Wenn Sie inhaltliche Anmerkungen zu diesem Artikel haben, können Sie die Redaktion per E-Mail informieren. Wir lesen Ihre Zuschrift, bitten jedoch um Verständnis, dass wir nicht jede beantworten können.