Kompaktlexikon der Biologie: Niere
Niere, Ren, Nephros, Exkretions- und osmoregulatorisches Organ der Wirbeltiere und des Menschen. In der Embryonalentwicklung der Amniota wird zunächst eine kurze Tubulusreihe, die Vorniere (Pronephros) angelegt, die aber nur vorübergehend oder gar nicht der Exkretion dient. Dies übernimmt ein caudal gelegenes Tubulussystem, der Mesonephros (Urniere), der beim adulten Organismus in das Ausführgangsystem der Hoden übergeht. Die Urniere wird bei den Reptilien bei der Geburt bzw. beim Schlüpfen, bei den Säugern früher durch die weiter caudal liegende Nachniere (Metanephros) ersetzt, die durch einen sekundären Harnleiter, den Ureter, nach außen mündet.
Die paarigen N. des Menschen sind unbeschadet ihres geringen Anteils (0,4 – 1 %) am Körpergewicht mit einem Zustrom von 25 % des pro Zeiteinheit aus dem Herzen gepumpten Blutes die relativ am besten mit Blut versorgten Organe, was bereits auf die große Regulationsleistung hinweist. Im grob anatomischen Aufbau lassen sich von außen nach innen die Bereiche Nierenrinde (Cortex), Nierenmark (Medulla) und das hohle Nierenbecken (Pelvis) unterscheiden. ( vgl. Abb. ) Im Feinbau dominieren zahlreiche tubuläre Abschnitte, deren funktionale Einheit das Nephron (Harnkanälchen, beim Menschen mit einer Gesamtlänge von ca. 100 km) ist. Das Nephron der Säugetiere steht mit dem Blutgefäßsystem über sein blind geschlossenes, ein Kapillarknäuel (Glomerulus) umgreifendes Ende in Verbindung und bildet an dieser Stelle das Nierenkörperchen (Malpighi-Körperchen). Nach einem kurzen Zwischensegment schließt sich an das Malpighi-Körperchen der proximale Tubulus an. Im elektronenmikroskopischen Bild stellen sich die Zellen des proximalen Tubulus als typische einschichtige transportierende Epithelzellen mit ausgeprägtem Mikrovillisaum, zahlreichen Mitochondrien und einem bis weit in den Zellkörper reichenden basalen Labyrinth dar. Der proximale Tubulus verjüngt sich und geht in die Henle-Schleife über, zunächst in einem absteigenden Ast weiter medullawärts, dann in einem dem ersteren eng und parallel anliegenden aufsteigenden Ast (Haarnadelprinzip) wieder in Richtung auf die Nierenrinde. Die Henle-Schleifen sind sowohl im Nierenmark als auch nur in der Nierenrinde zu finden und dort kürzer. Unter den Vögeln und Säugetieren (nur dort kommen Henle-Schleifen vor) haben diejenigen Arten die längsten Schleifen, die an extremen Wassermangel angepaßt sind. Dem aufsteigenden Ast der Henle-Schleife schließt sich der wieder weitlumige distale Tubulus an. Mehrere distale Tubuli inserieren in ein Sammelrohr, das funktionell zum Nephron gehört, indem es an der Harnbereitung beteiligt ist.
Die Harnbereitung in der N. beginnt mit einer Filtration des Blutplasmas. Dabei müssen mehrere Filterschichten überwunden werden, deren Porenweite so klein ist, dass nur Moleküle mit einer relativen Molekülmasse bis maximal 60000 passieren können. Lipoproteine und Globuline sowie an Albumine gebundene Substanzen, darunter auch zahlreiche Arzneimittel, werden nicht filtriert. Der Primärharn wird also als nahezu proteinfreies Ultrafiltrat abgepresst (Protein im Endharn deutet immer auf eine Störung der Filtrationseinrichtung hin). Treibende Kraft für die Druckfiltration ist der hydrostatische Druck in den Arteriolen, von dem aber nur ein bestimmter Betrag als effektiver Filtrationsdruck wirken kann, da ihm der kolloidosmotische Druck des Blutes und der hydrostatische Druck im Bereich des Malpighi-Körperchens entgegengerichtet sind. Der abgepresste Primärharn ist durch Sekretions- und Reabsorptionsprozesse in den tubulären Abschnitten des Nephrons mannigfaltigen Veränderungen unterworfen und wird bei Vögeln und Säugern in Abhängigkeit von den physiologischen Gegebenheiten mehr oder weniger stark konzentriert
Die Reabsorptions- und Sekretionsprozesse dienen einerseits dazu, zahlreiche Substanzen, die nur aufgrund ihrer Molekülgröße den Glomerulus passiert haben, dem Körper wieder zuzuführen, andererseits dazu, nicht mehr benötigte Substanzen zusätzlich dem Primärharn zuzufügen und schließlich die Ionenzusammensetzung des Harns so zu regulieren, dass das innere Milieu des Körpers konstant gehalten wird (Pufferfunktion und pH-Regulation). Die dazu benötigten Transportprozesse sind teils aktiver, teils passiver Natur. Im proximalen Tubulus werden Glucose, Aminosäuren, Ketonkörper und die Ionen HCO3–, Na+, K+ sowie Phosphat und Sulfat aktiv zurücktransportiert. ( vgl. Abb. ) Die hierzu notwendige Stoffwechselenergie wird im Wesentlichen durch die Oxidation von Fettsäuren und Ketonkörpern gewonnen, nicht dagegen über Kohlenhydratabbau, da die Hexokinase-Aktivität in diesem Nierenabschnitt sehr gering ist. Im distalen Tubulusabschnitt überwiegt hingegen, ebenso wie in den Bereichen der Henle-Schleifen, die im äußeren mitochondrienreichen Nierenmark liegen, der Abbau von Glucose zur ATP-Gewinnung. Im inneren Mark wiederum überwiegt die energetisch ungünstigere anaerobe Glykolyse. Das gebildete ATP wird ganz überwiegend zum Aufbau einer so genannten Natrium-motorischen Kraft benötigt, d.h. zum Antrieb einer Na+/K+-ATPase (Ionenpumpen) auf der Blutseite der Tubuluszellen. Zusammen mit Natrium-gekoppelten Translokatoren auf der Harnseite werden über dieses Transportsystem die meisten der zur Retention anstehenden Substanzen auch gegen die eigenen Konzentrationsgradienten dem Blut wieder zugeführt. Insbesondere gilt dies für Glucose und Aminosäuren. Mit dem Transportsystem für Glucose werden auch Fructose und Galactose transportiert. Für Glucose ist die Kapazität des Systems in der gesunden Niere bei 18 mmol/l erreicht, bei Nierenkranken wird schon unterhalb dieser Schwelle Glucose im Harn ausgeschieden (Prinzip des Glucosetoleranztests). Auch für Aminosäuren gibt es (mindestens fünf verschiedene) Transportsysteme mit unterschiedlicher Gruppenspezifität. Die stickstoffhaltigen Endprodukte Harnstoff, Harnsäure und Kreatinin unterliegen unterschiedlichen Ausscheidungsmodi. Harnstoff folgt i.d.R. dem osmotischen Gradienten im Nierenmark und wird auf diese Weise zu etwa 50 % rückresorbiert. Die Ausscheidungsrate ist, ebenso wie die von Harnsäure, von der aufgenommenen Nahrung (Anstieg bei hohem Protein- bzw. Puringehalt) abhängig. Harnsäure wird teilweise sezerniert, größtenteils aber rückresorbiert. Diese Balance muss sehr sorgfältig eingehalten werden, da es bei ernährungsbedingt vermehrter Ausscheidung wegen der schweren Wasserlöslichkeit zu Harnsäuresteinen kommen kann. Kreatinin passiert die Tubuli unverändert und wird vollständig ausgeschieden (Clearance). Auch die Ionen von Natrium, Kalium, Calcium, Phosphat und Sulfat werden sehr unterschiedlich behandelt. Das Verhältnis der Ausscheidung oder Rückresorption von Kalium und Natrium im distalen Tubulus wird durch Aldosteron reguliert; hohe Aldosteronwerte erhöhen die K+-Ausscheidung auf Kosten einer Natrium- (und damit Wasser-)Retention. Im übrigen wird K+ im proximalen Tubulus über einen nicht im Einzelnen bekannten Mechanismus weitestgehend rückresorbiert. Für die Regulation der Ausscheidungsrate von nicht proteingebundenem Calcium sorgen Parathormon (verstärkte Rückresorption mittels einer Ca2+-ATPase) und Calcitonin (vermehrte Ausscheidung). Der Gefahr einer Bildung von unlöslichem Calciumphosphat in der Niere wird dadurch begegnet, dass im Gegensatz zu Phosphat nur sehr wenig Ca2+ den Körper über die N., das meiste dagegen über den Darm verlässt.
Die N. ist neben dem Atmungssystem (Atmung) der zweite Ort der Regulation des Säure-Base-Gleichgewichts. Hierfür ist die Regulation der Ausscheidung und Resorption von Hydrogencarbonat (HCO3–) als Antwort auf eine metabolische Acidose oder Alkalose im Organismus von zentraler Bedeutung. An der Ausscheidung, Reabsorption und zusätzlichen Bereitstellung von Hydrogencarbonat sind Ionenaustauschprozesse und die Bildung von Ammoniak beteiligt. Wird viel Hydrogencarbonat filtriert, sodass es wieder reabsorbiert werden muss, kommt es zu aktiver Sekretion von H+ (intrazellulärer Kohlensäure entstammend) in das (proximale) Tubuluslumen. Na+ diffundiert im Ionenaustausch in die Tubuluszelle und wird aktiv in die umgebenden Kapillaren gepumpt. Damit kann im Lumen aus dem vorhandenen Hydrogencarbonat und H+ Kohlensäure (H2CO3) gebildet werden, die sogleich in H2O und CO2 (Kohlenstoffdioxid) dissoziiert. Das CO2 diffundiert in die Tubuluszelle und wird dort unter Katalyse einer Carboanhydrase wieder zu Kohlensäure umgewandelt. Durch deren Zerfall in H+ und Hydrogencarbonat steht zum einen neues H+ zum Transport ins Lumen und zum anderen Hydrogencarbonat zum Rücktransport ins Blut zur Verfügung. Überschüssiges H+ kann in Form von monobasischem Phosphat (H2PO4-) ausgeschieden werden. Hierzu verbindet sich sezerniertes H+ im Tubuluslumen mit abfiltrierten HPO42–-Ionen; das Phosphat wirkt ebenso wie das Hydrogencarbonat als Puffer. Eine Stabilisierung des Säure-Base-Gleichgewichts wird schließlich durch die Produktion von Ammoniak (NH3) in den Nierentubuli erreicht, insbesondere dann, wenn bei metabolischer Acidose keine Hydrogencarbonat- oder Phosphatpuffer im Tubuluslumen zur Verfügung stehen. NH3 wird aus Glutamin gebildet; andere Aminosäuren können in diesen Weg eingespeist werden. NH3 diffundiert ins Tubuluslumen und fängt dort die H+-Ionen ab, die somit als Ammoniumionen (NH4+) mit dem Harn ausgeschieden werden. Für die Osmo- und Volumenregulation der Niere sind im Wesentlichen Hormone verantwortlich, die einerseits die Tubuluspermeabilität (im distalen Tubulus und Sammelrohr) verändern bzw. auf die Natriumrückresorption Einfluss nehmen (Adiuretin, Aldosteron), andererseits vasoaktive (Gefäß verengende) Substanzen (Renin-Angiotensin- System), deren Ausschüttung (Renin) von Chemorezeptoren (Na+-sensitiv) und Druckrezeptoren gesteuert wird. (Diabetes insipidus, Exkretion, Exkretionsorgane, Harn, Osmoregulation, Phenylketonurie)
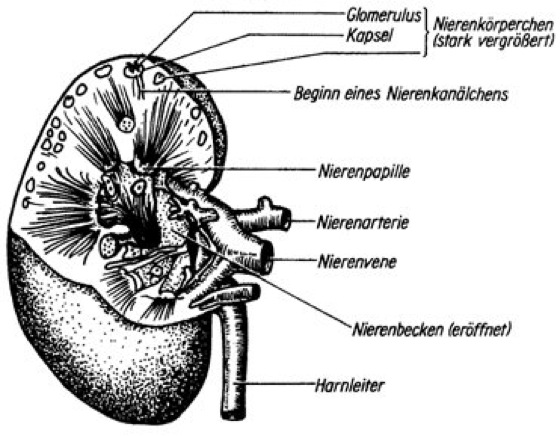
Niere: Schnitt durch die Niere des Menschen

Wenn Sie inhaltliche Anmerkungen zu diesem Artikel haben, können Sie die Redaktion per E-Mail informieren. Wir lesen Ihre Zuschrift, bitten jedoch um Verständnis, dass wir nicht jede beantworten können.