Kompaktlexikon der Biologie: Proteinfaltung
Proteinfaltung, die Faltung eines Polypeptids in seine native Struktur, d.h. seine dreidimensionale biologisch funktionelle Struktur oder native Konformation. Der Verlust dieser nativen Struktur wird als Denaturierung, die Wiederherstellung als Renaturierung bezeichnet. In der lebenden Zelle faltet sich ein neu synthetisiertes Protein rasch und spontan in seine native dreidimensinale Sruktur, Untereinheiten lagern sich zur Quartärstruktur zusammen, ein Prozess der als kooperative Selbst-Assemblierung bezeichnet wird. Diese und die vorhergehende P. werden in der Zelle durch so genannte faltungsakzessorische Proteine beschleunigt. Zusätzlich kann die Bildung von Disulfidbindungen in neu synthetisierten Proteinen die Struktur des Proteins nach der posttranslationalen Modifikation vorgeben.
Bei der P. werden zuerst kurze Abschnitte an α-Helices und β-Schleifen gebildet, die als Kerne (Gerüst) zur Stabilisierung anderer geordneter Regionen des Proteins dienen. Nur jene Kerne, die der nativen Konformation angehören, bleiben dauerhaft bestehen und wachsen, möglicherweise durch Bildung einer Domäne, die gewöhnlich nicht mehr als 200 Reste enthält. Bei der Faltung von Proteinen mit vielen Domänen tritt eine Zwischenstufe mit ausgedehnter Sekundärstruktur, jedoch ungeordneter Tertiärstruktur auf, wodurch die hydrophoben Aminosäuren teilweise der wässrigen Lösung ausgesetzt sind. Dieses intermediäre Multidomänenprotein durchläuft dann geringe Konformationsänderungen und erreicht die kompakte Tertiärstruktur des monomeren Proteins. Bei oligomeren Proteinen lagern sich die Monomere zu einer Vorstufe der Quartärstruktur zusammen. Kleine Konformationsänderungen führen zur nativen Quartärstruktur. ( vgl. Abb. )
Wenn die native Konformation erreicht ist, werden durch die spezifische Bindung von Liganden (z.B. Enzymsubstrate, Liganden von Trägerproteinen, Liganden von Rezeptoren) weitergehende feine, aber entscheidende Änderungen induziert. Veränderungen dieser Art können berechnet und mit Hilfe von Computersimulationen aufgezeichnet werden. Faltungsakzessorische Proteine sind z.B. die Protein-Disulfid-Isomerase, die Peptidyl-Prolyl-cis/trans-Isomerasen und die molekularen Chaperone. (Proteine, Translation)
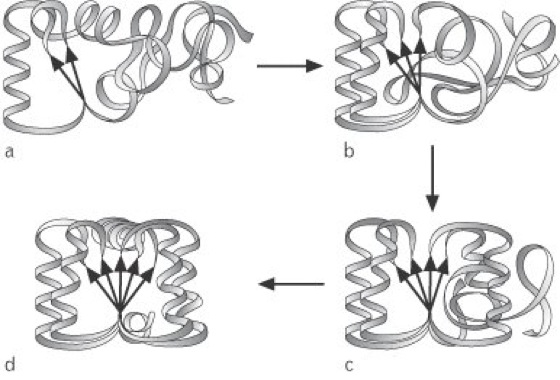
Proteinfaltung: Eine mögliche Variante der Proteinfaltung. a Bildung eines strukturellen Kerns, der aus wenigen, besonders stabilen Sekundärstruktur-Bereichen besteht; b während andere Regionen ihre Sekundärstruktur einnehmen, werden sie über weit entfernte Bereiche durch Wechselwirkungen mit dem strukturellen Kern stabilisiert; c der Faltungsprozess setzt sich fort, bis der Großteil des Polypeptids seine korrekte Sekundärstruktur angenommen hat; d die endgültige Struktur hat normalerweise die thermodynamisch stabilste Konformation
Wenn Sie inhaltliche Anmerkungen zu diesem Artikel haben, können Sie die Redaktion per E-Mail informieren. Wir lesen Ihre Zuschrift, bitten jedoch um Verständnis, dass wir nicht jede beantworten können.