Lexikon der Biologie: Caenorhabditis elegans
Caenorhabditis elegans w [von *caeno –, griech. rhabdos = Stab, latein. elegans = fein], Abk. C. elegans, ein ca. 1 mm langer Nematode (Fadenwürmer) der Ordnung Rhabditida ( vgl. Abb. 4 , vgl. Tab. ), der im Boden gemäßigter Klimate lebt und sich von Bakterien ernährt. Er wurde um 1900 von E. Maupas beschrieben. Seit er 1965 von S. Brenner als Untersuchungsobjekt für die genetische Forschung gewählt wurde, ist dieser Wurm eines der am intensivsten untersuchten Lebewesen – vor allem bedingt durch seine auf ein Minimum an Komplexität reduzierte Körperorganisation und seine problemlose Vermehrung und Handhabung im Labor. Neben Drosophila melanogaster, Saccharomyces cerevisiae (Saccharomyces), Arabidopsis thaliana (Schmalwand),Zebrafisch, Hausmaus (Mäuse) und Mensch ist C. elegans heute ein bedeutender Modellorganismus für die Analyse allgemeiner Funktionsmechanismen der Metazoen-Biologie, u. a. in der Genetik, Zellbiologie, Entwicklungsbiologie, Neurobiologie und Biochemie ( vgl. Infobox ). Ende 1998 lag das Genom von C. elegans als erstes Genom einer höherentwickelten Tierart komplett sequenziert vor. Die im Rahmen dieser Arbeit entwickelten Verfahren und Techniken kommen auch dem Human Genome Project (Genomprojekt) zugute. Nach Abschluß der Sequenzierung begannen eine umfassende computergestützte Analyse der genomischen Organisation und Feinstruktur, die intensive Suche nach Expressionsmustern und Funktionen neuentdeckter Gene und deren Vergleich mit bekannten Genen anderer Organismen. Diese Untersuchungen sind vor allem im Hinblick auf die Entwicklung von Modellsystemen für viele menschliche Krankheiten von Interesse. Altern, formative Teilung, Keimzelldeterminierung, Netrine.
R.C.
Lit.:Riddle, D.I., Blumenthal, T., Meyer, B.J., Priess, J.R. (eds.): C. elegans II. Cold Spring Harbor Press 1997. Schierenberg, E., Cassada, R.: Der Nematode Caenorhabditis elegans. Biologie in unserer Zeit 16 (1): 1–7; 1986. Wood, W.B. (ed.): The nematode Caenorhabditis elegans. Cold Spring Harbor 1988.
Caenorhabditis elegans
Kultivierung: Die Züchtung von C. elegans im Labor ist leicht und zudem billig. Sie erfolgt monoxenisch, d. h. auf einer reinen Bakterienkultur (z. B. E. coli) als einziger Nahrungsquelle. Für die Zucht werden wie bei Mikroorganismem meist mit Agar gefüllte Petri-Schalen verwendet, auf denen bis zu 100 000 Individuen wachsen können. In der Biochemie werden Flüssigkulturen eingesetzt. Die Tiere lassen sich Jahrzehnte lang bei –80°C aufbewahren und nach dem Auftauen wiederbeleben. Zellkulturen sind bislang nicht gelungen.
Lebenszyklus und Entwicklung: Die Generationsfolge beträgt unter optimalen Bedingungen nur 3 Tage und ist auch für einen Nematoden extrem kurz. Die Embryogenese dauert nur 12 Stunden; etwa 2 Tage nach Befruchtung des Eies hat sich das Adulttier entwickelt ( vgl. Abb. 1 ). Gewöhnlich ist es ein Hermaphrodit (Zwitter), der durch Selbstbefruchtung homozygote Linien erzeugt und 250–350 Nachkommen produziert. Die Eier, die 4 Larvenstadien (L1–L4) und die Adulttiere sind durchsichtig, weshalb nach Fluoreszenzmarkierung der DNA sämtliche Zellen bzw. ihre Kerne erkannt werden können ( vgl. Abb. 2 ). Außerdem ermöglicht dies, die Teilungen und Wanderungen jeder einzelnen Zelle während der Entwicklung des Wurms zu verfolgen. Dies erfolgt nach wie vor mit Hilfe der Interferenzmikroskopie, vor allem der von Nomarski entwickelten Differential-Interferenzkontrast-Mikroskopie, heutzutage zudem durch Anwendung der digitalen Videotechnik, die eine erhebliche Kontrastverstärkung sowie eine einfache Analyse optischer Schnitte bietet. Damit ließ sich für C. elegans als bislang einzigem Tier ein vollständiger Zellstammbaum ( vgl. Abb. 3 ) erstellen. Durch elektronenmikroskopische Analyse von seriellen Dünnschnitten konnte präzise für jede Zelle in jedem Entwicklungsstadium die anatomische Identität dokumentiert werden. Mittels Kombination beider Techniken ließ sich so belegen, woher jede Zelle abstammt, ob und wie sie sich noch teilt und wohin sie wandert (Zellgenealogie).
Unter ungünstigen Umweltbedingungen entsteht bei der 2. Häutung eine zum Larvenstadium L3 alternative, nicht wachsende Dauerlarve ( vgl. Abb. 1 ). Sie ist inaktiv und besitzt eine fast kristalline, sehr feste Cuticula (die Eischale aus Protein, Wachs und Chitin ist ähnlich widerstandsfähig), wodurch sie widerstandsfähig gegen Detergentien, Säure, Salze oder Hitze ist und mehrere Monate überleben kann. Sie ähnelt den infektiösen Larven parasitischer Nematodenarten und gilt daher als Modell für wichtige von Nematoden erzeugte Krankheiten.
Alle Zellteilungen im Ei sind reine Furchungen ohne Zellwachstum. Die Entwicklung von C. elegans ist streng determiniert, was zu Eutelie (Zellkonstanz) führt. Von den 558 Zellen beim Schlüpfen des Embryos teilen sich 55 postembryonal ( vgl. Tab. ). Erwachsene Hermaphroditen haben in 99% aller Fälle exakt 959 somatische Zellkerne, von denen 358 zum Nervensystem gehören. Postembryonales Wachstum wird hauptsächlich durch Zellstreckung (bis zu 100fach) mit Kernvergrößerung erreicht. – In der Embryogenese von C. elegans entstehen außerdem Zellen, deren Differenzierungsschicksal programmierter Zelltod (Apoptose) ist. Dieses Phänomen tritt vor allem in Schwesterzellen zu Nervenzellen, aber auch in allen anderen Geweben (einschließlich Keimbahn) auf. Es ist ein allgemeines Prinzip der Entwicklung Höherer Tiere und wird in allen untersuchten Tieren durch extrem konservierte Gensysteme herbeigeführt. Bei C. elegans umfaßt das die Apoptose kontrollierende Gen-Netzwerk ca. 20 sog. ced-Gene (ced = Abk. für cell death). Das Gen ced-3 codiert z. B. für die erste entdeckte Caspase, eine Apoptose-spezifische Protease.
Die Musterbildung erfolgt genau wie bei anderen Tieren größtenteils durch eine Reihe von Zell-Zell Wechselwirkungen (Induktionen) im frühen Embryo. Die vielen inäqualen Zellteilungen deuten jedoch zusätzlich auf interne Zellpolarität hin und auf unterschiedliche Verteilung von vermutlich determinierendem Material an die 2 jeweiligen Tochterzellen. Die Komplexität der Entstehung verschiedener Zelltypen (z. B. entstehen Muskelzellen aus 4 verschiedenen Teilen des Zellstammbaums) wird als Beweis für eine komplizierte evolutionäre Vorgeschichte des Zellstammbaums von C. elegans und der damit verbundenen Vorgänge gesehen. Von anterior nach posterior erkennt man in allen Geweben sich wiederholende Elemente, allerdings keine echte Segmentierung. Die (häufig geschlechtsspezifische) Identität der teilweise in Reihen angeordneten postembryonal teilungsaktiven Zellen wird durch Zell-Zell-Wechselwirkungen bestimmt, die der Kontrolle der Gene des Homöobox-Clusters (etwas einfacher organisiert als bei Drosophila melanogaster) unterliegen.
Chromosomen, Geschlechtsbestimmung: Die diploiden Tiere haben normalerweise 12 Chromosomen (5 Paare Autosomen und 2 X- oder Geschlechtschromosomen). Durch das Verhältnis von X-Chromosomen zu Autosomen wird das Geschlecht festgelegt – 2 X-Chromosomen zu 2 Autosomensätzen ergibt Hermaphroditen. Diese Hermaphroditen sind strukturell rein weiblich, im Larvenstadium L4 produzieren sie nur Spermien (Proterandrie), als Adulttiere ausschließlich Oocyten, die von den ca. 400 eigenen, gespeicherten Spermien befruchtet werden. Wenn aber in der Meiose 1 X-Chromosom verloren geht (Häufigkeit zwischen 0,1% und 10% [z. B. Hitzeschock]), entstehen X0-Individuen, die sich zu Männchen entwickeln. Als L1 haben Männchen fast die selbe Anatomie und nur 2 Zellen mehr als die Hermaphroditen, als Adulttiere jedoch 72 Zellen mehr ( vgl. Tab. ) und entsprechende Extrastrukturen, u. a. im Nervensystem und Kopulationsapparat (allerdings nur 1 Gonade). Durch Paarung von Hermaphroditen mit eingeführten Männchen entstehen zunächst aufgrund der Bevorzugung der größeren Allospermien heterozygote Nachkommen (Kreuzungsnachkommen sind zur Hälfte X0, also Männchen). Erst wenn diese aufgebraucht sind, führt die Besamung der übrigen Eizellen durch Autospermien wieder zu 100% Hermaproditen. Geschlechtsidentität wird Zelle für Zelle bestimmt und nicht wie bei Säugern global durch zirkulierende Hormone.
Anatomie, Nervensystem: Die 3 typischen tierischen Keimblätter Ektoderm, Mesoderm und Entoderm sind in dem schlauchförmigen, durchsichtigen Körper anhand ihrer Hauptprodukte Haut, Muskulatur und Darm-Trakt leicht erkennbar, ebenso exkretorische und reproduktive Organe ( vgl. Abb. 4 ). In den 2 Gonaden liegen ca. 2600 Keimbahnzellen vor. Für das Nervensystem konnte durch die Identifikation und Klassifizierung aller Nervenfortsätze und Synapsen mittels anatomischer Rekonstruktion von EM-Serienschnitten (s. o.) ein Funktionsmodell mit insgesamt 302 Nervenzellen und 56 Glia-ähnlichen Zellen erstellt werden (Drosophila insgesamt 105, Mensch 1012 Zellen). Dieses Modell wird inzwischen durch Analysen des Verhaltens und der EM-Ultrastruktur von Mutanten, durch Abtöten einzelner Nervenzellen mit Laserstrahlen und durch Computersimulation verfeinert. Der für die Nahrungsaufnahme zuständige Pharynx hat ein eigenes, abgeschlossenes 20-zelliges Nervensystem. Fast alle bekannten Neurotransmitter und entsprechende Rezeptoren wurden in C. elegans identifiziert. Zwar sind die Fortsätze der Nervenzellen kaum verzweigt, jedoch bildet jede Zelle mit vielen anderen (bis zu 30) Zellen entlang nebeneinander liegender Fortsätze Synapsen aus (insgesamt etwa 5000 chemische, 600 elektrische sowie 200 neuromuskuläre Synapsen). Dies ermöglicht eine hohe Komplexität der Signalintegration und des Verhaltens. Da die Nervenzellen extrem klein sind, sind Experimente mittels elektrophysiologischer Ableitung nur mit modernsten Spezialmethoden durchführbar.
Genetik: Vorteilhaft für die Genetik sind die geringe Größe und große Individuenzahl, die die Isolierung von Mutanten erleichtern. Inzwischen sind Mutanten in vielen Tausend Genen bekannt und eingefroren in Genbibliotheken zugänglich. Da ein einzelner Hermaphrodit durch Selbstbefruchtung einen Klon an Nachkommen produziert, lassen sich neue Mutanten schnell und ohne Kreuzungsverfahren homozygot gewinnen. Durch fakultative Paarung mit eingeführten Männchen entstehen heterozygote Nachkommen (mit 50% X0, also Männchen), die man für genetische Komplementationstests zwischen verschiedenen Mutanten und für die genetische Kartierung verwendet. Entsprechend der Chromosomenzahl wurden mehrere Tausend Gene verschiedener Phänotypen auf 6 "Linkage-Gruppen" kartiert. Diese klassische Genkarte wurde inzwischen mit der physikalischen Karte des vollständig klonierten Genoms in Übereinstimmung gebracht. Die von S. Brenner erstmals beschriebenen unc-Mutanten (unc = Abk. von uncoordinated) führten zur Entdeckung und funktionellen Analyse von Proteinen, die u. a. für die Wegfindung von auswachsenden Neuronen, aber auch zur Muskelbildung und Muskelfunktion, wichtig sind. Zu den unc-Genen homologe Gene kommen auch beim Menschen vor, weshalb sie als Modellsysteme für Krankheiten herangezogen werden. – Für verschiedene Anwendungen und genetische Techniken eignet sich C. elegans besonders: Genetische Mosaiktiere (Mosaikbastard), in denen – bedingt durch den Spontanverlust eines Chromosomenfragments oder Chromosoms – verschiedene mutante Zellklone vorkommen, erlauben Rückschlüsse über den Bildungs- oder Funktionsort von Proteinen. Gen-Rescue (Rescue-Techniken) oder Transformation von Nachkommen durch Injektion klonierter DNA in die Oogonien der Mutter erlauben die Erkennung von Genen und ihrer Funktionen. Gen-Knockout durch gene targeting und Tagging von Zielgenen durch Insertion von mobilen Transposonen dienen der Erzeugung von Mutationen und der Klonierung. Das grünfluoreszierende Protein, entweder in Form eines Fusionsproteins in rekombinanten Systemen oder durch Kopplung des gfp-Gens hinter einen Promotor, erlaubt die Untersuchung der Genexpression oder das Verfolgen von Zellinien während der Embryonalentwicklung.
Genomprojekt, Genfunktionsanalysen: Das Genom von C. elegans ist mit 97 000 Kilobasen ca. 20mal so groß wie das von Escherichia coli und 6mal so groß wie das der Hefe. Das inzwischen komplett sequenzierte Genom besteht aus ca. 19 100 Protein-codierenden und ca. 800 t-, sn- und rRNA-codierenden Genen. Durchschnittlich treten nur 5 außergewöhnlich kleine Intronen pro Gen auf, die codierenden Exonen belegen 27% des Gesamtgenoms und damit einen viel höheren Anteil als bei anderen Höheren Tieren. Dies erleichtert die Klonierung sowie die Genomanalyse erheblich. Nur einem Bruchteil der Gene konnte bislang anhand klassischer Mutantenanalyse direkt eine Funktion zugeschrieben werden. Die inzwischen möglichen Sequenzvergleiche ergaben, daß etwa 42% der Gene Homologien zu Genen aus anderen Tieren oder auch aus Mikroorganismen haben, deren Funktion man teilweise kennt. 34% weisen Homologien zu Genen anderer Nematoden auf, deren Funktion nur in wenigen Fällen bekannt ist; die restlichen 24% der sequenzierten Gene wurden bislang nur bei C. elegans gefunden. Interessanterweise liegt über ein Viertel der Gene wie bei Bakterien in Operonen organisiert vor. Die abgeleiteten polycistronischen mRNAs werden für die Translation durch sog. trans-Spleißen gespalten. Viele Gene und andere Sequenzen liegen in repetitiven Familien vor. Die mit 650 Kopien am häufigsten wiederholte Domäne codiert für ein Membranprotein mit Chemorezeptionsfunktion (Geruchserkennung). Viele wiederholt vorkommenden Gene häufen sich zu Clustern im Genom, was als Hinweis auf neuere evolutionäre Duplikation verstanden wird. Das Genom der Mitochondrien ist mit nur 15 kb sehr klein, codiert nur 40 Proteine und einige ungewöhnlich kleine tRNAs.
Fast alle Gene sind inzwischen auch als cDNA kloniert und durch Teilsequenzierungs-Information (ESTs; Expressed Sequence Tags) identifiziert. In zahlreichen Forschungsprojekten werden sie in vitro exprimiert oder auch in Form von DNA-Chips (Biochips) zum Transkriptions-Screening benutzt. Die Analyse von Proteinexpressionsmustern erfolgt mit Hilfe der zweidimensionalen Gelelektrophorese. Weitere Vorhaben umfassen die Untersuchung von Transkriptionsfaktoren, interzelluläre TranskriptionsfaktorenSignaltransduktionSignaltransduktionlarbiologische, entwicklungs- und neurogenetische Aspekte, vor allem im Bezug auf menschliche Krankheiten.
| |
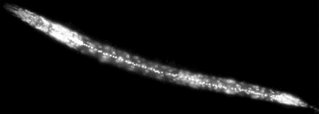
Caenorhabditis elegans Abb. 2: Hermaphrodit (L3), bei dem einzelne Zellen anhand der DNA-Fluoreszenzmarkierung der Zellkerne erkennbar sind. |
| |
Abb. 3: Zellstammbaum eines Hermaphroditen. Bis zum 1. Larvenstadium entstehen durch Zellteilungen 558 Zellen (dazu 113 "Zelltote", vgl. Tab.), von denen sich 55 weiter teilen und die Anzahl der somatischen Zellen bei Adultieren auf 959 erhöhen. Dazu kommen die Keimbahnzellen im Adulttier (in der Abb. nicht dargestellt; vgl. Tab.). Da Darm, Gh Gonadenhülle, Go Gonade, Hy Hypoderm, Km Körpermuskeln, Kz Keimzellen, Ne Nerven, Ph Pharynx, Um Uterusmuskeln, Ut Uterus, Vm Vulvamuskeln, Vu Vulva |
| |
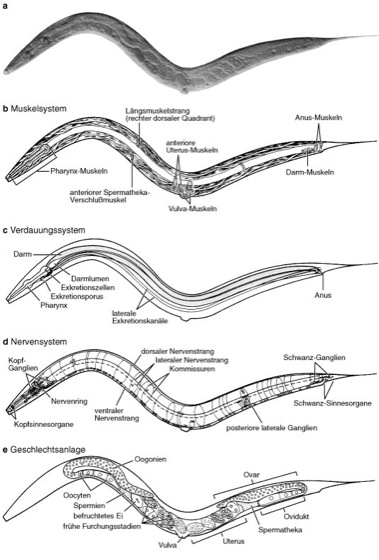
Caenorhabditis elegans Abb. 4: Schematische Darstellung der Anatomie eines adulten Hermaphroditen. a lebendes Tier im Differential-Interferenzkontrast-Mikroskop. b Muskelsystem: der Fortbewegung dienende Körpermuskeln sind in 4 Strängen angeordnet, von denen hier 2 wiedergegeben sind; daneben sind Körpermuskeln mit spezieller Funktion und Muskeln des Pharynx dargestellt. c Verdauungssystem und Exkretionsorgane. d Nervensystem: die Nervenzellen liegen fast alle in den Ganglien oder im ventralen Nervenstrang, dessen Fortsätze den dorsalen Nervenstrang bilden; 20 Nervenzellen befinden sich im Pharynx. e Geschlechtsanlage: Die Gonade besteht aus 2 gebogenen Schläuchen, in denen die Eizellen nach und nach wachsen, reifen, befruchtet werden und sich danach zu teilen beginnen, bevor sie schließlich abgelegt werden. |


Wenn Sie inhaltliche Anmerkungen zu diesem Artikel haben, können Sie die Redaktion per E-Mail informieren. Wir lesen Ihre Zuschrift, bitten jedoch um Verständnis, dass wir nicht jede beantworten können.