Lexikon der Biologie: Ecdysteroide
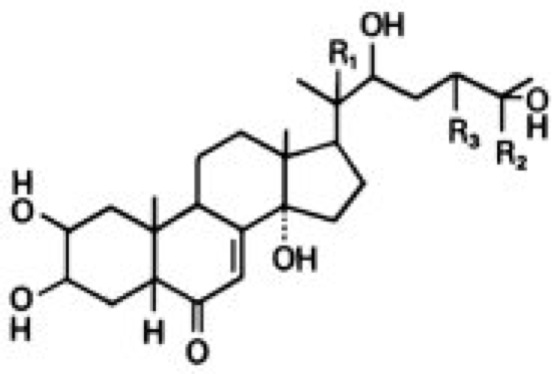
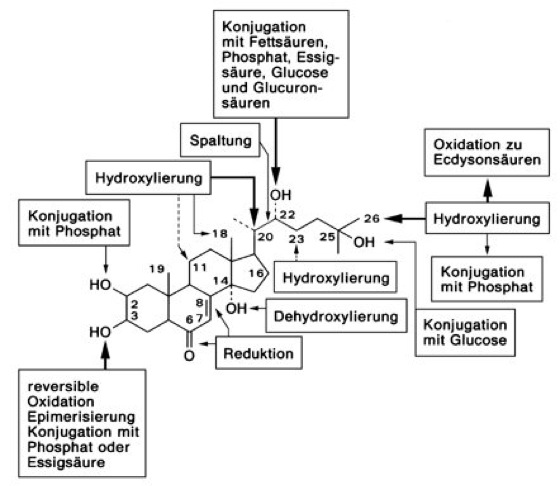
Ecdysteroide, Ecdyson und zahlreiche davon abgeleitete Substanzen, die im Tierreich (Zooecdysteroide) als Hormone und im Pflanzenreich (Phytoecdysteroide) als sekundäre Inhaltsstoffe (Pflanzenstoffe) vorkommen. Der Name leitet sich von der Funktion als Häutungshormon der Insekten ab (Ecdysis, Häutung; Insektenhormone) – eine der vielfältigen Funktionen der Ecdysteroide, welche als erste nachgewiesen wurde. 1954 wurde Ecdyson durch A.F.J. Butenandt und P. Karlson aus 500 kg Puppen des SeidenspinnersBombyx mori erstmals isoliert, die Strukturaufklärung erfolgte 1963 mit Hilfe der Röntgenstrukturanalyse. Bis heute sind weit mehr als 100 Ecdysteroide ( vgl. Abb. ) bekannt, die sich mittels Calliphora-Test (Calliphora-Einheit), Radioimmunassay, HPLC und Massenspektroskopie (Massenspektrometrie) differenzieren lassen. Grundgerüst der Ecdysteroide ist ein Steroid mit einer charakteristischen 14α-Hydroxygruppe und einer 2-enon-Struktur im Ring B, das sich vom Cholesterin ableitet, welches von Arthropoden (Gliederfüßern) nicht selbst synthetisiert werden kann. Die Biosynthese der Ecdysteroide erfolgt in vielen, bis heute noch nicht in allen Details aufgeklärten Schritten über 7-Dehydrocholesterin (Calciferol) und 2,22,25-Trideoxyecdyson (5-β-Ketodiol). Die folgenden, zum Ecdyson führenden Hydroxylierungen werden, nach bisherigen Erkenntnissen, durch von Cytochrom P450 (Cytochrom-P450-System) abhängige Monooxygenasen der Mitochondrien und Mikrosomen (endoplasmatisches Reticulum) katalysiert. Das Ecdyson ist selbst als Hormon wirksam, kann jedoch auch durch Hydroxylierung an C-20 in das aktivere 20-Hydroxyecdyson überführt werden. Ecdysteroide liegen häufig als Konjugate, gebunden an Phosphat, Sulfat, Glucose, Gluconsäuren, Acetat, Fettsäuren oder Proteine, vor ( vgl. Abb. ). Diese Konjugate können zum einen als Speicher-, zum anderen als Ausscheidungsprodukte dienen. Die Inaktivierung der Ecdysteroide erfolgt durch Hydroxylierung an C-26, Bildung von Ecdysonsäuren, Epimerisierung an C-3 sowie durch die Abspaltung der Seitenkette. Ecdysteroide synthetisierende Gewebe sind bei Insekten die Ventraldrüsen im Kopf, Prothoraxdrüse, Ringdrüse, Oenocyten, Hoden und Follikel des Ovars; bei Krebstieren das Y-Organ (Carapaxdrüse) und in anderen Gliederfüßern, z. B. Opilioniden (Weberknechten), oenocytenähnliche Zellkomplexe. Die Synthese der Ecdysteroide wird bei Insekten durch das prothorakotrope Hormon, Juvenilhormon, Ecdysteroid-Feedback und möglicherweise neuronal reguliert. Bei Krebstieren erfolgt die Regulation über das moult inhibiting hormone (MIH), Ecdysteroid-Feedback und möglicherweise über weitere, nicht näher charakterisierte humorale Faktoren. Aufgrund ihrer Polarität können Ecdysteroide als freie, gelöste Substanzen transportiert werden, jedoch existieren auch Ecdysteroid-Carrier-Proteine (ECP), die die Funktion des Transports und der Abpufferung des Ecdysteroid-Titers ausüben können. Die Lipidlöslichkeit ermöglicht die Aufnahme der Ecdysteroide in die Zellen durch Diffusion. Die Akkumulation in bestimmten Geweben (z. B. Imaginalscheiben) wird durch energie- und Na+/K+-ATPasen-abhängige, membranständige Carrier erreicht. Es existieren zumindest zwei verschiedene Typen von Ecdysteroidrezeptoren, cytosolische und kernständige, die in vielen spezifischen Zielorganen mit Hilfe immuncytochemischer Methoden oder durch Bindung des radioaktiv markierten Ecdysteroidagonisten Ponasteron A nachgewiesen werden konnten und welche zwischen einzelnen Ecdysteroiden unterscheiden (relative Molekülmassen zwischen 70 000 beim FlußkrebsOrconectes und ca. 130 000 bei Drosophila, KD zwischen 3,3–6 · 10–9 M bei Drosophila und 5–6 · 10 –11 M bei Orconectes für Ponasteron A). Das Gehirn von Insekten weist eine ganze Reihe Ecdysteroid-bindender Regionen auf. Das Wirkungsspektrum der Ecdysteroide ist sehr breit. Bei Insekten werden die Oocytenreifung, Spermiogenese, Embryonalentwicklung, Larven- und Adulthäutung, Gonadendifferenzierung sowie die Dotterproteinsynthese beeinflußt. Bei der Insektenentwicklung bestimmt das relative Verhältnis von Ecdysteroid zu Juvenilhormon den Häutungstyp (Larval-, Pupal- oder Adulthäutung). Genaue Mechanismen dieser Regulation sind noch weitgehend unbekannt. Der Titer von Ecdyson selbst ist beim Übergang vom Larven- zum Puppenstadium sowie während der Puppenentwicklung am höchsten. Während der Metamorphose von der Larve zur Puppe aktiviert Ecdyson 6 Gene, deren Produkte zum Puppenstadium führen. Ecdyson beeinflußt den an der Häutung maßgeblich beteiligten Tyrosinstoffwechsel, indem es eine Dipeptidase induziert, die β-Alanyltyrosin in Alanin und Tyrosin spaltet. Dieses wird unter hormonellem Einfluß von Bursicon zu Dihydroxyphenylalanin (DOPA) umgebaut, das wiederum von einer durch Ecdyson induzierten DOPA-Decarboxylase zu Dopamin decarboxyliert wird. Im adulten Insekt ist Ecdyson vermutlich an der Induktion von Vitellogenese und Eireifung beteiligt. Verhaltensänderungen, wie das Beenden der Freßphase und das Eintreten in die Wanderphase, ebenso wie das Spinnen des Kokons, werden ebenfalls durch Ecdysteroide induziert. Abhängig vom Entwicklungsstadium werden durch Ecdysteroide unterschiedliche Gene aktiviert, wie z. B. die Regionen 2B5, 74EF und 75B der Riesenchromosomen in Speicheldrüsenzellen während der frühen Larvalentwicklung oder das Ddc-Gen der DOPA-Decarboxylase. Weitere Ecdysteroid-induzierbare Gene sind das 67B-Hitzeschock-Gen, die Actin-Gene 5C und 42A, das Dotterprotein YP1 und viele andere. Die weitaus umfangreichsten Kenntnisse der Ecdysteroidwirkung stammen zwar aus dem Bereich der Insekten, die hormonelle Regulation durch Ecdysteroide ist aber für alle Gliederfüßer nachgewiesen. Auch bei Hohltieren, Plattwürmern, Fadenwürmern, Ringelwürmern und Weichtieren treten Ecdysteroide auf, bei manchen dieser Tiere ist die Hormonwirkung gezeigt oder wird zumindest vermutet. Daher werden die Ecdysteroide als gemeinsames Merkmal aller Protostomier ("Urmünder", "Bauchmarktiere") angesehen. Des weiteren nimmt man an, daß parasitisch lebende Einzeller, z. B. Wimpertierchen, auf den Ecdysteroid-Haushalt ihrer Wirte reagieren. Das Vorkommen der Ecdysteroide in Stachelhäutern und Wirbeltieren wird im wesentlichen auf den Ecdysteroid-Gehalt in der Nahrungskette zurückgeführt. Eine Hormonwirkung konnte in diesen Organismen nicht festgestellt werden. Durch das Auftreten bei den parasitisch lebenden Bandwürmern, Saugwürmern und Fadenwürmern haben die Ecdysteroide auch in der Medizin Bedeutung erlangt. So kann man bei infizierten Patienten einen erhöhten Ecdysteroidgehalt in Serum und Urin feststellen. Eine Konzentration von mehr als 3 nmol/l Serum wird als Indikator für eine Wurminfektion gewertet. Für die im Pflanzenreich zum Teil in enormen Mengen (bis zu 2,9% des Trockengewichts) vorkommenden Ecdysteroide, die vielfach Alkylreste in der Seitenkette am C-Atom 17 tragen, konnte bisher weder ein synthetisierendes Gewebe noch eine genaue Funktion festgestellt werden. Es wird vermutet, daß Ecdysteroide eine Rolle bei der pflanzlichen Abwehr nicht angepaßter, phytophager Schädlinge spielen. Augenstielhormone, X-Organ.
T.Z./M.B.
Wenn Sie inhaltliche Anmerkungen zu diesem Artikel haben, können Sie die Redaktion per E-Mail informieren. Wir lesen Ihre Zuschrift, bitten jedoch um Verständnis, dass wir nicht jede beantworten können.