Lexikon der Biologie: Elektrolythaushalt
Elektrolythaushalt, geregelte Aufnahme, Umwandlung und Abgabe von Elektrolyten. Ein konstanter Elektrolytbestand des Organismus ist Voraussetzung für den Ablauf aller Lebensprozesse (Leben) und steht in engem Zusammenhang mit dem Wasserhaushalt. Extrazellularraum (Plasmaraum und interstitieller Raum) sowie der Intrazellularraum (Flüssigkeitsräume) weisen dabei jeweils eine charakteristische Verteilung der Kationen und Anionen auf. Im Blutplasma des Menschen dominieren bei den Kationen Natrium (142 mmol/l) und bei den Anionen das Chlorid (Chlor) (102 mmol/l). Auch Proteine und das Hydrogencarbonat tragen zur Gesamtkonzentration bei, während Phosphat, Sulfat (Schwefelsäure) und organische Säuren (Aminosäuren, Citronensäure) nur in sehr geringen Konzentrationen vorkommen. Die interstitielle Flüssigkeit und die Lymphe entsprechen in ihrer Elektrolytzusammensetzung, mit Ausnahme der Proteine, die hier fast nicht vorkommen, der des Blutplasmas. Sehr verschieden ist dagegen die Ionenkonzentration der intrazellulären Flüssigkeit; das dominierende Anion ist das Phosphat. Die Konstanz der osmotisch wirksamen Teilchen (Osmose) im Blutplasma und im interstitiellen Raum ( vgl. Abb. ) wird über einen hormonellen Regelkreis gesteuert (Osmoregulation). Bei der Regulation der intrazellulären Ionenkonzentrationen (besonders der Na- und K-Konzentration) spielen die in den Membranen lokalisierten Ionenpumpen eine entscheidende Rolle. Täglich werden vom Erwachsenen ca. 3–4 g Na+ und 4–5 g Cl– aufgenommen und ausgeschieden. Die Regulation der Na-Konzentration erfolgt über das Renin-Angiotensin-Aldosteron-System, das die renale Ausscheidung beeinflußt. Die Konstanz von Na+ und Cl– ist für den Organismus von besonderer Bedeutung, da ihre Konzentration das Volumen der extrazellulären Flüssigkeit bestimmt. Die K-Ionen sind für die Elektroneutralität und die Osmolarität im Innern der Zellen verantwortlich (tägliche Zufuhr 2–4 g). Die extrazelluläre K-Konzentration wird über die renale Ausscheidung unter Mitwirkung von Aldosteron kontrolliert. Die Ausscheidungsrate wird dem Angebot angepaßt. Die intrazelluläre K-Konzentration wird durch aktive Transportprozesse (aktiver Transport) über Ionenpumpen reguliert. Calcium und Phosphat sind am Aufbau des Knochens und der Zähne beteiligt. Ca spielt darüber hinaus eine wichtige Rolle als second messenger (sekundäre Boten) und bei der Erregbarkeit (Erregung) von Nerven- und Muskelzellen. Der tägliche Bedarf an Ca beträgt 0,8 g, an anorganischem Phosphat 0,9 g. Die Regulation der extrazellulären Konzentration erfolgt über das Parathormon, Calcitonin, Vitamin D3 (Calciferol), Regulation der Ca-Verteilung zwischen extra- und intrazellulärem Raum über eine Ca-ATPase (Adenosintriphosphatasen). Magnesium-Ionen (Magnesium) hemmen in hoher Konzentration die Freisetzung von Acetylcholin, dämpfen die Erregbarkeit des neuromuskulären Apparats und beeinflussen viele enzymatisch gesteuerte Reaktionen (täglicher Bedarf 0,25 g). Der Mechanismus der Regulation ist noch nicht gesichert, eine mögliche Beteiligung des Parathormons, Calcitonins, Schilddrüsenhormons und Aldosterons wird diskutiert. Die Bestimmung der Ionenkonzentration im Plasma oder Serum erfolgt entweder mit der Emissions-Flammenphotometrie (Flammenphotometer) oder mit ionenselektiven Elektroden. Das Serum-Natrium wird normalerweise in einem engen Bereich (135–144 mmol/l) konstant gehalten. Bei abweichenden Werten ist zu klären, ob es sich um eine Störung der Na-Bilanz mit normaler, vermehrter oder verminderter extrazellulärer Flüssigkeit handelt. Bei einer Hyponatriämie (zu geringe Na-Konzentration) fehlen klinische Symptome oder sind dramatisch (Bewußtseinsstörungen, pathologische Reflexe, niedrige Körpertemperatur, Anorexie, Krämpfe); Ursachen sind Glucocorticoidmangel, vermehrte ADH-Sekretion (Hirntumor, Encephalitis), verschiedene Lungenerkrankungen, akute und chronische Niereninsuffizienz. Klinische Symptome bei Hypernatriämie (zu hohe Na-Konzentration) sind vor allem Polyurie, Polydipsie und Durst. Die Mortalität bei akuter Hypernatriämie ist sehr hoch. Der Referenzbereich für die Kalium-Konzentration liegt bei 3,65–5,3 mmol/l. Eine Hypokaliämie liegt bei K-Konzentrationen von < 3,5 mmol/l vor. Neben einer mangelnden K-Zufuhr (Patienten mit Anorexia nervosa) sind die Ursachen für eine Hypokaliämie akute und respiratorische Alkalose, gastrointestinale Flüssigkeitsverluste, K-Verluste über die Nieren und hormonale Regulationsstörungen. Bei einer Hyperkaliämie ist die K-Konzentration des Serums auf über 5,5 mmol/l erhöht. Sie wird verursacht durch eine vermehrte exogene Zufuhr, eine verminderte K-Elimination bei Niereninsuffizienz, einen Mineralocorticoidmangel und interne Bilanzstörungen (akute Acidose, Gewebs- und Zellzerfall z.B. durch cytostatische Therapie und Hämolyse). Die Symptome einer Hypo- und Hyperkaliämie entsprechen sich weitgehend und sind vor allem durch die Beteiligung von K-Ionen an dem Membranpotential der Muskelzelle geprägt. Diese Membranen sind für K-Ionen gut permeabel, und das Verhältnis von intra- und extrazellulärem Kalium ist die Hauptkomponente des Ruhepotentials. So führt eine Hypokaliämie zu einer Schwächung der Muskelkontraktion und damit zu Paralysen der glatten Muskulatur und quergestreiften Muskulatur, während eine Hyperkaliämie eine Übererregbarkeit der Muskelzellen zur Folge hat. Vor einer Muskelparalyse kommt es zu starken Veränderungen vor allem am Herzen mit Extrasystolie (Extrasystolen; ab 7,5 mmol/l), Vorhofflimmern (wenn kombiniert mit Digitalisglykosiden zur Vorhoftachykardie), und bei Werten über 9 mmol/l besteht die Gefahr des Herzstillstands. Im Plasma liegt das Calcium zu 55% ionisiert und zu 40% an Protein gebunden vor (Calmodulin); der Serumspiegel bewegt sich zwischen 2,2 und 2,7 mmol/l. Hypocalcämien (< 2 mmol/l) beruhen auf Fehlen oder Unterfunktion der Nebenschilddrüsen, Vitamin-D-Mangel, verminderter enteraler Absorption, UV-Licht-Mangel oder Vitamin-D-Metabolisierungsstörungen in der Leber und Niere. Als Folge einer Hypocalcämie kommt es zu einer gesteigerten Erregbarkeit des gesamten Nervensystems (tonische Muskelkrämpfe, Spasmen der glatten Muskulatur). Ursache für eine Hypercalcämie (> 2,7 mmol/l) sind maligne Erkrankungen (hämatologische Neoplasien, Tumoren mit und ohne Knochenmetastasen), Überfunktion der Nebenschilddrüse, Vitamin-D-Intoxikation, abrupter Abbruch einer Corticoidtherapie und Immobilisierung (besonders bei Osteoporose); Symptome sind Gewichtsabnahme, Appetitlosigkeit, Obstipation, Polyurie, Herzrhythmusstörungen (Gefahr der Nierensteinbildung). Eine Hypomagnesiämie (< 0,7 mmol/l) tritt auf bei chronischen Darmerkrankungen, Hyperthyreose, Hyperparathyreoidismus, Alkoholismus, Acidosen und verstärkter renaler Ausscheidung. Eine exakte Zuordnung der Symptome ist nur schwer möglich; sie ähneln denen einer Hypocalcämie, daneben treten auch Herzrhythmusstörungen auf. Bei einer Hypermagnesiämie (> 1,25 mmol/l) kommt es zu einer Herabsetzung der Erregbarkeit der quergestreiften Muskulatur und zu einer Hemmung von zentralnervösen Funktionen. Sie kommt zustande durch Gabe großer Mengen magnesiumhaltiger Infusionen oder große Gaben von Magnesiumsulfat und durch Niereninsuffizienz. Klinische Symptome sind eine Herabsetzung der Erregbarkeit der quergestreiften Muskulatur und eine Hemmung zentralnervöser Funktionen. Chlorid ist zu 88% extrazellulär und zu 12% intrazellulär lokalisiert (Normalwert 97–108 mmol/l). 5–10% des Chlorids werden täglich erneuert, und die Resorption erfolgt mit dem Natrium im Ileum (Dünndarm); die Ausscheidung geschieht fast vollständig über die Nieren. Die Regulation erfolgt durch das Aldosteron. Zu einer Erniedrigung kommt es durch einen intestinalen Verlust und bei Syndromen mit Mineralocorticoidexzessen. Zu einer Erhöhung des Chloridwerts führen renale tubuläre Acidosen, metabolische Acidose, Aldosteronmangel und chronische Hyperventilation. Ernährungsphysiologie (Tab.), Nährstoffhaushalt, Niere, Puffer, Säure-Base-Gleichgewicht.
Ch.J.
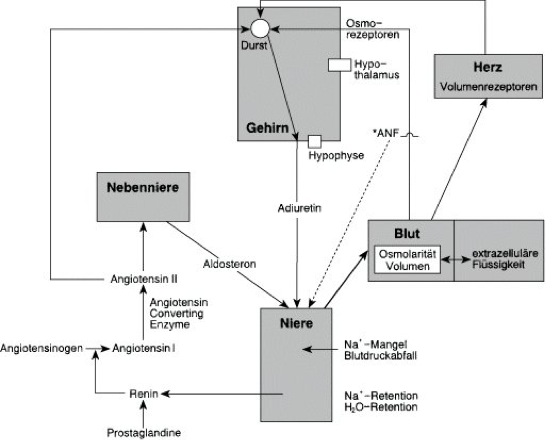
Elektrolythaushalt
Kontrolle von Osmolarität und Volumen des Blutes und der extrazellulären Flüssigkeit. *ANF = Atrial natriuretic factor; bei Na+-Mangel wird dieser Faktor nicht freigesetzt.
Wenn Sie inhaltliche Anmerkungen zu diesem Artikel haben, können Sie die Redaktion per E-Mail informieren. Wir lesen Ihre Zuschrift, bitten jedoch um Verständnis, dass wir nicht jede beantworten können.