Lexikon der Biologie: Gehörorgane
Gehörorgane, Hörorgane, dem Gehörsinn dienende Organe. Bei den Insekten haben mehrere Ordnungen unabhängig voneinander Gehörorgane entwickelt, die in 3 Grundtypen unterschieden werden können: Hörhaare, Johnstonsches Organ, Tympanalorgane ( ö vgl. Abb. 1 , ö vgl. Abb. 2 ). Die Hörhaare von Insekten sind in der Regel besonders lang, leicht beweglich und an exponierten Körperstellen (z.B. Cerci der orthopteren Insekten; Geradflügler) lokalisiert. Sie werden aufgrund ihrer leichten Beweglichkeit von schnell schwingenden Teilchen in Resonanz versetzt (Schallschnelleempfänger; Gehörsinn), können jedoch auch auf anderweitige mechanische Reize reagieren (Becherhaar), so daß häufig eine eindeutige Zuordnung dieser Sinnesorgane nicht möglich ist. Im allgemeinen reagieren Hörhaare am besten auf niederfrequente Töne (unter 200 Hz; Schall), da diese eine hohe Schallschnelle haben; in Bereichen über 300 Hz nimmt die Empfindlichkeit der Hörhaare schnell ab. Die Raupen einiger Schmetterlinge (Weißlinge, Fleckenfalter, Ritterfalter) können jedoch noch Töne bis über 1000 Hz wahrnehmen. Ebenfalls als Schallschnelleempfänger arbeitet das Johnstonsche Organ, ein bei allen ektognathen Insekten (Ectognatha) anzutreffendes Sinnesorgan, das im 2. Fühlerglied (Pedicellus) der Antennen liegt. Es besteht aus einer großen Anzahl dreidimensional angeordneter Rezeptorzellen, den Scolopidien (bei den Stechmücken 30.000; Scolopidialorgane, Scolopidium), die mit der Grundplatte des Antennen-(Geißel-)schafts in Verbindung stehen, und dient der Registrierung der relativen Bewegungen der Antennen gegenüber deren Basis. Bei Abbiegung der Geißel wird ein sehr spezifisches Erregungsmuster erzeugt, das Aufschluß über die Richtung der einwirkenden Schallquelle gibt. Bei einigen Insektenarten (z.B. Stechmücken, Zuckmücken und Taumelkäfer) dient das Organ im Fortpflanzungs-Verhaltenskontext den Männchen zur Lokalisation der Weibchen und reagiert dafür besonders empfindlich auf die Frequenzbereiche der Fluglaute weiblicher Tiere. Die schnellfliegenden Arten (z.B. Hautflügler) messen mit dem Johnstonschen Organ zudem ihre Fluggeschwindigkeit (unterschiedliche Geschwindigkeiten bewirken verschieden große Abbiegungen der Antennen). Außerdem liefert es Informationen über die Orientierung im Raum (infolge der Schwerkraft erfahren die Antennen bei verschiedener Lage des Körpers im Raum eine verschieden starke Auslenkung). Tympanalorgane sind unabhängig voneinander in verschiedenen Insektenfamilien aus Chordotonalorganen an sehr unterschiedlichen Körperteilen entstanden und besitzen ausschließlich Hörfunktion. Sie arbeiten entweder als Druck- oder Druckdifferenzempfänger oder als eine Mischung aus beiden. Die Schallwellenperzeption erfolgt immer über ein Trommelfell (in der Regel 1, bei den Singschrecken [Heupferde] und Grillen 2 auf jeder Körperseite). Tympanalorgane finden sich an der Basis der Vorderbein-Tibiae (Grillen, Laubheuschrecken) oder im Grenzbereich zwischen Thorax und Abdomen. Bei Feldheuschrecken, Spannern und Zünslern liegen sie im 1. Abdominalsegment (bei Zikaden im 2. Abdominalsegment), bei anderen Schmetterlingen (Eulenfalter, Zahnspinner, Bärenspinner) befinden sie sich im Metathorax, bei einigen Wasser-Wanzen(Corixa, Sigara, Notonecta, Naucoris, Plea) im Mesothorax. Schwärmer besitzen dagegen Gehörorgane in den verdickten Spitzen der Labialpalpen, einige Augenfalter und Eckenfalter (Fleckenfalter) sowie Florfliegen haben diese in der basalen Cubitalader (Insektenflügel) des Vorderflügels. Die Schallwellenperzeption erfolgt über eine variable Zahl von Scolopidien (1 bei Plea [Zwergrückenschwimmer], 2 bei Eulenfaltern, 4 bei Spannern, 100–1000 bei Grillen, Laubheuschrecken und Singzikaden [bis 1500]), die dem Trommelfell (Tympanum) anliegen und dessen Schwingungen registrieren. Dem Trommelfell sind in der Regel Tracheenblasen unterlagert, welche die Schallresonanz besser ausnutzbar machen. Tympanalorgane sprechen bevorzugt auf hohe Frequenzen zwischen 7 bis etwa 90 kHz an; bei Vertretern der Nachtfalter sogar bis zu etwa 240 kHz. Letztere gehören zu den wenigen Tieren, die zwar zur Lautwahrnehmung, aber nicht zur Lauterzeugung befähigt sind (Ausnahme: Totenkopfschwärmer): Die größte Empfindlichkeit ihrer Gehörorgane liegt im Frequenzbereich der Peillaute ihrer größten Feinde, der Fledermäuse (Echoorientierung, Farbtafel). In diesem Fall dienen die Gehörorgane daher nicht der innerartlichen Kommunikation, sondern der Feinderkennung. Bei den übrigen Insekten liegt die größte Empfindlichkeit der Tympanalorgane in dem Frequenzbereich, den auch die arteigenen Laute aufweisen. Frequenzanalysen können mit diesen Organen nur begrenzt durchgeführt werden, die Determination der Schallrichtung ist aber gut ausgeprägt – eine Eigenschaft, die für diejenigen Arten besonders wichtig ist, bei denen sich die Geschlechter in der Paarungszeit durch Gesang ausfindig machen (Phonotaxis; Bioakustik, Stridulation). – Die Gehörorgane der Wirbeltiere gehen einheitlich auf Teile des Labyrinths ( ö vgl. Abb. 3 und mechanische Sinne II) zurück und arbeiten als Schalldruckempfänger. Fische (Farbtafel) besitzen kein Trommelfell; viele Arten haben aber andere Strukturen zur Schallaufnahme entwickelt. So können z.B. Arten mit Schwimmblase über diese Schalldruckwellen aufnehmen und die Vibrationen auf verschiedenen Wegen an die Sinnesfelder im Innenohr weiterleiten. Bei den Heringen und Mormyriden (Eigentliche Nilhechte) reicht die Schwimmblase direkt an das Innenohr, so daß Schwingungen ohne Zwischenstrukturen auf die Hörorgane übertragen werden können. Bei anderen Arten steht die Schwimmblase in Kontakt mit den die Gehörorgane umgebenden Knochen, und die Vibrationen werden über Knochenleitung ans Innenohr weitergegeben. Ostariophyse Fische (Karpfenfische, Welse) besitzen 1–3 besondere schalleitende Knochen, die Weber-Knöchelchen, welche die Schwingungen der Schwimmblase über einen unpaaren Perilymphsack auf 2 paarige Endolymphsäcke übertragen, die wiederum an die beiden Innenohren reichen. Dort wird der Schall von verschiedenen Haarsinnesfeldern aufgenommen, die alle auch gleichzeitig dem Gleichgewichtssinn (Gleichgewichtsorgane, Gravitationsbiologie) dienen: die Macula utriculi (Utriculus), Macula sacculi (Sacculus) und Macula lagenae (Lagena). Diese Strukturen werden auch als Otolithenorgane bezeichnet, da sie aus vielen, durch Gallerte fest verbackenen Gehörsteinchen (Otolithen) bestehen, die über einigen tausend Haarsinneszellen angeordnet sind. Bei Bewegung der Otolithen durch hereinkommende Vibrationen verbiegen sich die Stereovilli der Zellen relativ zum Zellkörper. Das Hörvermögen der Fische beschränkt sich im allgemeinen auf tiefere Töne, die obere Hörgrenze ( ö vgl. Tab. ) liegt bei 1000–2000 Hz für Arten ohne Schwimmblase und bei etwa 5 kHz für Arten mit Schwimmblase und Weber-Knöchelchen. Einige Vertreter der Ostariophysen können sogar noch Töne bis zu 13 kHz hören. – Bei Amphibien haben die 3 Hörfelder der Fische nur noch Funktionen bei der Gleichgewichtswahrnehmung. Zum Hören haben sie 2 weitere Haarsinnesfelder entwickelt, die Papilla amphibiorum und die Papilla basilaris. Die Sinneszellen sind hier nicht mit Otolithen, sondern mit Tectorialmembranen (Deckmembran; Cortisches Organ) bedeckt. Die Auslenkung der Mikrovilli geschieht durch die Relativbewegung der Tectorialmembran zur Zellschicht. Als schalleitende Strukturen besitzen sie, ebenso wie die Reptilien und Vögel, 2 Gehörknöchelchen, Columella und Extracolumella, welche die Vibrationen des Trommelfells auf das Innenohr übertragen. Die Hörbereiche der Amphibien sind je nach Art sehr unterschiedlich und erstrecken sich von 100 bis zu etwa 9000 Hz. – Bei Reptilien und Vögeln ist nur noch die Papilla basilaris als Hörorgan erhalten; sie ist langgestreckt und mit bis zu 16.000 Haarzellen (bei Vögeln) besetzt. Wie auch bei den Säugern ist sie beidseitig von Perilymphräumen (Perilymphe) umgeben: Es bildet sich so eine schlauchförmige Struktur aus 3 durch Membranen voneinander getrennten Gängen, der Scala tympani, Scala media (Ductus cochlearis) und Scala vestibuli. Die Scala media, gefüllt mit Endolymphe, wird von der Scala tympani durch die Basilarmembran (Membrana basilaris) und das ihr aufliegende Cortische Organ getrennt. Zwischen Scala media und Scala vestibuli ist die Reissnersche Membran gelegen. Das Gehör der Reptilien ist für die verschiedenen Arten sehr unterschiedlich ausgeprägt. So haben Schlangen nur ein sehr geringes Hörvermögen (sie orientieren sich hauptsächlich über chemische Sinne und mit Hilfe des Temperatursinns), viele Arten der Schildkröten und Eidechsen weisen jedoch offensichtlich ein recht gutes Gehör auf. Der Hörbereich der Papilla basilaris der Reptilien liegt zwischen ca. 10 und 10.000 Hz, jedoch ist der Frequenzbereich einzelner Arten innerhalb der genannten Grenzen teilweise viel kleiner. Vögel haben durchweg ein sehr gutes Gehör mit Frequenzbereichen zwischen 10 und 12.000 Hz. Manche Arten können sogar noch Infraschall (unter 1 Hz) wahrnehmen, andere hohe Frequenzen bis 30 kHz. Einige höhlenbewohnende Vögel orientieren sich wie die Fledermäuse mit Hilfe von Ultraschall (Echoorientierung).
Bei den Säugetieren (Ausnahme: Kloakentiere) und den Krokodilen windet sich das Gangsystem schraubig auf und bildet die Schnecke (Cochlea, Abb.). Am Helicotrema, dem „Ende der Cochlea“, stehen Scala tympani und Scala vestibuli miteinander in Verbindung. Außerdem besitzen die Säugetiere 3 anstatt nur 2 Gehörknöchelchen (Reichert-Gauppsche Theorie), genannt Hammer (Malleus), Amboß (Incus) und Steigbügel (Stapes). Das Gehörorgan (Ohr) der Säugetiere ist bisher das von allen Gehörorganen am besten untersuchte. Die Schallwellen werden vom Außenohr aufgenommen und über den Gehörgang dem Trommelfell (Membrana tympani) zugeleitet. Manche Tiere können ihre Ohrmuscheln bewegen, wodurch eine verbesserte Richtungslokalisation (s.u.) von Schallquellen ermöglicht wird. Die durch die Schallwellen erzeugten Schwingungen des Trommelfells werden von den Gehörknöchelchen auf das ovale Fenster (Vorhoffenster, Fenestra ovalis) übertragen, das an der Schneckenbasis die Scala vestibuli gegenüber dem Mittelohr abgrenzt. Die Übertragungseigenschaften des Trommelfell-Gehörknöchelchen-Apparats sind frequenzabhängig und in mittleren Frequenzbereichen am besten ausgebildet. Nach früherer Auffassung sollten hohe Frequenzen durch Knochenleitung, d.h. durch Schwingungen des Schädels, übertragen werden; experimentell konnte diese Theorie jedoch nicht bestätigt werden. Beim normalen Hören im täglichen Leben spielt die Knochenleitung nur für das Hören der eigenen Stimme eine Rolle. Da Scala vestibuli und Scala media nur durch die sehr dünne Reissnersche Membran voneinander getrennt sind, können die Flüssigkeitsschwingungen in beiden Scalae, ausgelöst durch die Schwingungen des ovalen Fensters, als Einheit betrachtet werden. Wegen der Inkompressibilität sowohl dieser Flüssigkeiten als auch der die Cochlea umgebenden Knochenkapsel erfolgt der Ausgleich dieser Schwingungen in Abhängigkeit von deren Frequenz über die Basilarmembran oder über das Helicotrema (für sehr tiefe Frequenzen) und schließlich über das runde Fenster (Schneckenfenster, Fenestra rotunda), der Grenze zwischen Scala tympani und Mittelohr. Die Schwingungen bewirken ihrerseits eine frequenzabhängige Erregung der Haarsinneszellen im Cortischen Organ. Von den Sinneszellen ziehen Nervenfasern (beim Menschen 30.000–40.000), die in ihrer Gesamtheit den Gehörnerv oder Hörnerv (Nervus acusticus, Statoacusticus) bilden, zum Gehirn. Jede dieser Fasern kommt von einem eng umschriebenen Bereich des Cortischen Organs bzw. einer inneren Haarzelle ( ö vgl. Abb. 4 ). Nach der Wanderwellentheorie ist jeder Ort der Basilarmembran einer bestimmten Frequenz zugeordnet, und in der Tat findet man, daß jede Nervenfaser nur durch die entsprechende Frequenz optimal erregt werden kann ( ö vgl. Infobox , ö vgl. Abb. 5 ): Man bezeichnet diese als die charakteristische Frequenz einer Nervenfaser. Auf dem Weg zur primären Hörrinde des Gehirns durchziehen die Nervenbahnen mehrere Kerngebiete, wo sowohl eine Verschaltung der Fasern eines Ohres als auch eine mit denen des anderen Ohres stattfindet. In diesen Kernen erfolgt die erste neuronale Analyse und Verarbeitung der aufgenommenen akustischen Reize (auditorisches System, auditorischer Cortex). – Bei den Säugetieren variiert das hörbare Tonspektrum ziemlich stark: So liegt z.B. der Hörbereich des jungen Menschen ( ö vgl. Abb. 6 ) zwischenetwa 15 Hz und 20 kHz (im Alter sinkt die obere Grenze auf 12–5 kHz), Katzen können noch Töne bis zu 50 kHz wahrnehmen, und Tiere mit Echoorientierung (z.B. Fledermäuse oder Wale) vermögen noch Frequenzen über 150 kHz aufzulösen. – Eine Schallwelle muß, um gehört zu werden, d.h. um im Hörbereich zu liegen, nicht nur eine bestimmte Frequenz, sondern auch einen definierten Schalldruckpegel aufweisen ( ö vgl. Abb. 6 ). Dieser Schwellenwert (Hörschwelle, Hörbarkeitsschwelle) ist frequenzabhängig und für das menschliche Ohr in den Bereichen von 2000–4000 Hz am niedrigsten. In diesen liegt auch ein Großteil der Frequenzen der menschlichen Stimme, wobei das geübte Ohr noch Tonhöhenunterschiede von 3 Hz, das entspricht einer Frequenzunterschiedsschwelle von etwa 0,3%, wahrnehmen kann. Ist der entsprechende Schwellenwert einmal überschritten, so wird, unabhängig von der Frequenz, mit zunehmendem Schalldruck ein Ton immer lauter empfunden. Bei kontinuierlich weiter steigendem Schalldruck wird zunächst eine Schmerzempfindung (Schmerzschwelle, Schmerzempfindungsschwelle) ausgelöst, die schließlich in Taubheit übergeht. Diese kann bei nur kurzer Schalleinwirkung reversibel sein. Mit steigender Einwirkungszeit führen über der Schmerzschwelle liegende Schalldruckpegel aber immer zu einer irreversiblen Schädigung des Gehörorgans. Diese ist im allgemeinen auf eine Verletzung der Sinneszellen und Störung der Mikrozirkulation in der Cochlea zurückzuführen. Gehörschäden können jedoch auch schon bei geringeren Schallintensitäten auftreten, sofern diese lange genug einwirken. Diese schädigenden Intensitäten sind bereits bei einer Dauerbelastung von 90 dB erreicht. Derartige Schalldruckpegel werden häufig in der Arbeitswelt, an Flughäfen und in Diskotheken weit überschritten.
Eine weitere Leistung der Gehörorgane von Insekten und Wirbeltieren besteht in der akustischen Lokalisation einer Schallquelle. Diese wird mit beiden Ohren (binaural) durchgeführt (Richtungshören). Zur „Berechnung“ der Schallrichtung in der horizontalen Ebene (rechts/links) werden folgende Kriterien herangezogen: 1) Die zeitliche Differenz zwischen dem Ankommen einer Schallwelle am linken bzw. rechten Ohr, wenn sich die Schallquelle seitlich des Hörers befindet. Diese Zeitdifferenz Δ t berechnet sich nach der Formel Δ t = d · sinα/v (d = Ohrenabstand, α = seitlicher Einfallswinkel der Schallwellen, v = Schallgeschwindigkeit). Dieses Kriterium gilt allerdings nur für Tiere mit hinreichend großem Ohrabstand. (Bei Insektenarten mit Tympanalorganen an den Tibien [z.B. Laubheuschrecken] können nur die Zeitdifferenzen zwischen beiden Tibien erfaßt werden, nicht aber die zwischen den beiden Trommelfellen eines Tympanalorgans, da diese viel zu dicht aneinander liegen.) Unter günstigen Bedingungen können Mensch und Katze noch Zeitdifferenzen von 10–5 s auswerten, was einer Winkelauflösung von 1° entspricht. 2) Die Differenz des Schalldrucks. Die von einer seitlich vom Hörer befindlichen Schallquelle ausgesandten Schallwellen werden auf dem Wege zu dem der Schallquelle abgewandten Hörorgan beim Durchtritt durch den Schädel gedämpft. 3) Unterschiede in der Klangfarbe. Diese resultieren daraus, daß beim Durchtritt durch den Schädel höhere Töne stärker gedämpft werden als tiefere. In der vertikalen Ebene (oben/unten) können Geräusche vor allem aufgrund der unsymmetrischen Form der Ohrmuscheln lokalisiert werden: Geräusche von oben werden vom Außenohr anders in das Mittelohr projiziert als Geräusche von unten und erzeugen also ein anderes Klangbild. Tiere ohne Ohrmuscheln (z.B. Vögel) bestimmen die vertikale Geräuschrichtung, indem sie ihren Kopf etwas zur Seite geneigt halten, so daß eine Ohröffnung tiefer liegt als die andere. Eine besondere Weiterentwicklung stellen hier die Gehörorgane einiger Eulenarten (z.B. Schleiereule; Eulen ) dar, bei denen sich die Ohröffnungen auf beiden Seiten des Kopfes nicht symmetrisch, sondern in verschiedenen Höhen befinden. Dies erlaubt den Tieren eine vertikale Richtungslokalisation, auch ohne den Kopf bewegen zu müssen. auditorische Efferenz, Bárány (R.), Békésy (G. von), Cochlear-Implantat, Cotugno (D.), Ewald (E.J.R.), Falloppio (G.), Geoffroy Saint-Hilaire (E.), Helmholtz (H.L.F. von), Müller (J.P.), Politzer (A.), statoakustische Organe, Valsalva (A.M.), Wollaston (W.H.); ö Gehörorgane , mechanische Sinne I–II.
H.W./Ch.S.
Lit.:Campenhausen, Ch. v.: Die Sinne des Menschen. Einführung in die Psychophysik der Wahrnehmung. Stuttgart 1993. Hellbrück, J.: Hören. Physiologie, Psychologie und Pathologie. Göttingen 1993. Horn, E.: Vergleichende Sinnesphysiologie. Stuttgart 1982. Penzlin, H.: Lehrbuch der Tierphysiologie. Stuttgart 1994. Zenner, H.-P.: Hören. Physiologie, Biochemie, Zell- und Neurobiologie. Stuttgart 1994. Zenner, H.-P., Zrenner, E. (Hrsg.): Physiologie der Sinne. Heidelberg 1995.
Gehörorgane
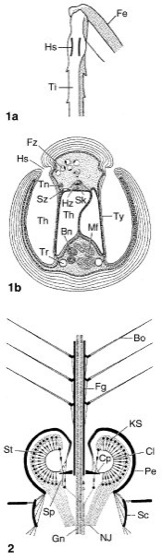
Abb. 1: 1a Lage der Tympanalorgane im Vorderbein einer Laubheuschrecke; 1b Querschnitt durch das Tympanalorgan im Vorderbein der Laubheuschrecke Decticus (Warzenbeißer). 2 Schema der Antenne einer Stechmücke (Culicidae) mit Johnstonschem Organ.
Bn Beinnerv, Bo Borsten, Cl Chitinlamelle, Cp Chitinplatte, Fe Femur, Fg Fühlergeißel, Fz Fettzelle, Gn Geißelnerv, Hs Hörspalt (Öffnungsschlitz der Tympanalhöhle), Hz Hüllzelle. KS Kerne der Sinneszellen, Mf Muskelfaser, NJ Nerven des Johnstonschen Organs, Pe Pedicellus (2. Fühlerglied), Sc Scapus (1. Fühlerglied), Sk Skolops, Sp Skolopidium, St Stift, Sz Sinneszelle, Th Tympanalhöhle, Ti Tibia, Tn Tympanalnerv, Tr Trachee, Ty Tympanum,
Gehörorgane
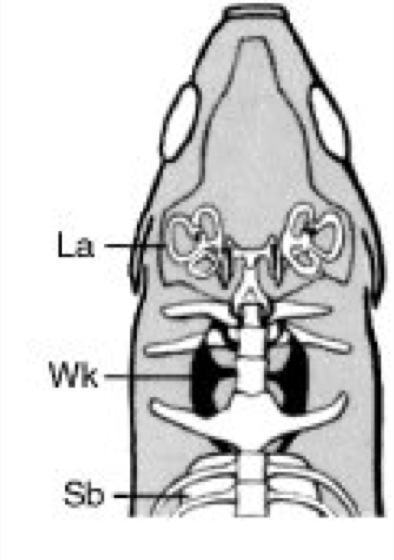
Abb. 2: Schalleitungsapparat bei Karpfenfischen.
La Lagena, Sb Schwimmblase, Wk Webersche Knöchelchen

Gehörorgane
Abb. 3: Labyrinthe verschiedener Wirbeltiere: a Fisch, b Frosch, c Vogel, d Säuger; Bo Bogengänge, CO Cortisches Organ, La Lagena, Pb Papilla basilaris, S Schnecke, Sa Sacculus, Ut Utriculus.

Gehörorgane
Abb. 4: Büschel von Haarzellen (Stereocilien) im Cortischen Organ
Gehörorgane
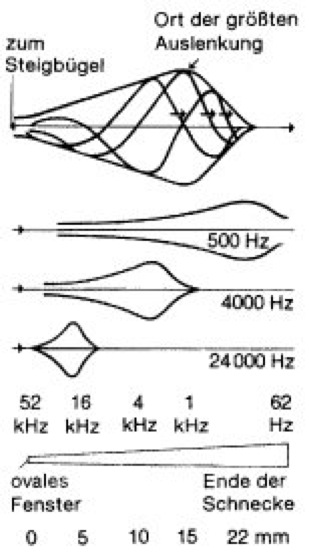
Abb. 5: Die Druckwelle (Wanderwelle) erreicht je nach Schallfrequenz ihr Schwingungsmaximum an verschiedenen Orten der Basilarmembran (Abb. oben). Abb unten: Schema der Basilarmembran mit den Regionen maximaler Schwingungsamplitude bei den eingetragenen Frequenzen.
Gehörorgane
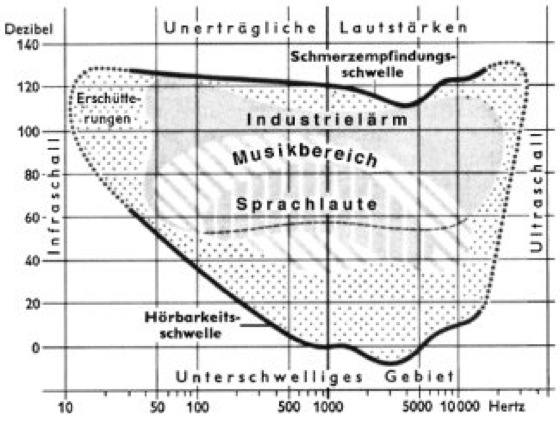
Abb. 6: Hörbereich (Hörfläche) aller hörbaren Töne des menschlichen Ohres
Wenn Sie inhaltliche Anmerkungen zu diesem Artikel haben, können Sie die Redaktion per E-Mail informieren. Wir lesen Ihre Zuschrift, bitten jedoch um Verständnis, dass wir nicht jede beantworten können.