Lexikon der Biologie: Nervensystem
Nervensystem, Systema nervosum, Abk. NS, Gesamtheit des den Metazoen-Organismus (Metazoa) durchziehenden Nervengewebes als morphologische und funktionelle Einheit mit der Fähigkeit, Reize über Rezeptoren aufzunehmen, Erregungen zu bilden, weiterzuleiten, zu verarbeiten, eventuell zu speichern und gegebenenfalls Reize über Effektoren zu beantworten. Seine funktionelle und strukturelle Einheit ist die Nervenzelle (Neuron). – Die Evolution des Nervensystems läßt sich nur theoretisch erschließen, da fossile Nachweise für das Nervensystem weitgehend fehlen (Paläoneurologie, Edinger [T.]). Ein Vergleich heute existierender, einfach organisierter Tierformen (z.B. Schwämme, Hohltiere, Plattwürmer) soll daher die diesen gemeinsamen Merkmale eines ursprünglichen Nervensystems verdeutlichen. Hierdurch lassen sich Modellvorstellungen über die theoretisch möglichen Evolutionswege des Nervensystems gewinnen. – Den Schwämmen(Porifera) als einer sehr einfach organisierten Tiergruppe wurde lange Zeit die Existenz eines Nervensystems abgesprochen, doch besitzen auch sie langgestreckte, mehrfach verzweigte (multipolare) Zellen, die Erregung in Form elektrischer Impulse (Bioelektrizität, Impuls, Nervenimpuls) weiterleiten. Die Erregungsübertragung zwischen den einzelnen Zellen erfolgt durch chemische Überträgersubstanzen (Neurotransmitter). Die Erregungsleitung ist sehr langsam und scheint bei der Kontraktion des Schwammkörpers eine Rolle zu spielen. – Ein Nervensystem in dem eingangs beschriebenen Sinne ist bei den (nicht monophyletischen) "Hohltieren" (Coelenterata) ausgebildet. Das Nervensystem dieser Tiere (Hohltiere, Nesseltiere, Rippenquallen) liegt an der Basis der äußeren, den Körper bedeckenden Zellschicht (epitheliales Nervensystem). Es besteht aus zahlreichen multipolaren Zellen, die an ihren Ausläufern miteinander in Kontakt treten und so ein netzförmiges Nervensystem (Nervennetz) aufbauen. Eine Konzentration von Nervenzellen zu einem Ring um den Schlund findet sich bei Polypen bzw. am Schirmrand der Medusen. Eine physiologische Besonderheit des diffusen Nervennetzes ist, daß die Synapsen zwischen den Nervenzellen Erregungen in beide Richtungen weiterleiten. Dadurch kann sich in dem Nervennetz eine Erregung von jedem beliebigen Punkt aus gleichmäßig in alle Richtungen ausbreiten. Bei 2 Gruppen der Nesseltiere, den Hydrozoa und den Scyphozoa, wurden 2 morphologisch getrennte Nervennetze beschrieben: eines im Zusammenhang mit der Fortbewegung, das andere im Zusammenhang mit den Fangbewegungen. Aktivität des einen Nervennetzes hemmt das andere und umgekehrt. Die Bedeutung der bilateralen Körperorganisation (bilateral, Symmetrie) und der gerichteten Fortbewegung läßt sich deutlich schon am Beispiel der Plattwürmer(Plathelminthes) darstellen. An dem Körperende, das bei der Fortbewegung als erstes mit der Umwelt in Berührung kommt, sind vermehrt Sinnesorgane ausgebildet (Cephalisation). Das Nervensystem besteht im typischen Fall aus 8 Marksträngen (enthalten Zellkörper und Fasern – also noch keine Ganglienbildung; Markstrang), die durch zahlreiche Kommissuren miteinander verbunden sind. Am Vorderende ist in bezug zu den Sinnesorganen ein Kopf-Ganglion (Gehirn) zu finden, das auch Kontakt zu den Längssträngen hat. Ein solches Nervensystem wird aufgrund der gleichmäßigen Ausrichtung der Längsstränge Orthogon genannt. – Das typische Nervensystem der Ringelwürmer(Annelida) ist ein Strickleiternervensystem, das sich aus vielen paarigen und segmental angeordneten Ganglien zusammensetzt. Die Ganglien sind durch querverlaufende Kommissuren und längsverlaufende Konnektive miteinander verbunden. Von jedem Ganglion gehen 3 "segmentale" Nerven aus (Gehirn [Abb.]). Diese innervieren aber, entsprechend der die Segmentgrenzen übergreifenden Anlage der Muskulatur, auch Gebiete, die jenseits des Segments liegen, von dessen Ganglion sie entspringen. Die Nerven fassen sensible und motorische Anteile (Afferenz, Efferenz) zusammen. Nervenimpulse werden dort über Zwischenneurone (Interneuron) auf ab- oder aufsteigende Nervenfasern umgeschaltet, so daß Impulsübertragung auch auf andere Ganglien möglich ist. Der Verlauf einzelner Fasern konnte experimentell über bis zu 30 Segmenten verfolgt werden. – Die Bauchmarkganglien (Bauchmark) erfüllen wichtige integrative Leistungen und scheinen auch für das Lernvermögen (Lernen) der Ringelwürmer von besonderer Bedeutung zu sein. Entfernung des Gehirns beeinträchtigt zumindest keine der Fähigkeiten. Das Gehirn der Ringelwürmer entsteht durch Verschmelzung der vordersten Bauchmarkganglien (Gehirn). Gehirn wie Bauchmarkganglien besitzen einen Rindenbau, d.h., eine äußere Rinde enthält die Zellkörper, während das innere Mark von auf- und absteigenden Faserbahnen erfüllt ist. – Vom Gehirn entspringen die Nerven des Eingeweidenervensystems (stomatogastrisches Nervensystem). Dieses bildet ein dichtes Nervengeflecht um Schlund und Eingeweide; es scheint von den sensiblen und motorischen Systemen des Strickleiternervensystems weitgehend unabhängig zu sein. Funktionell völlig unabhängig vom allgemeinen motorischen Nervensystem ist das Riesenfasersystem ( vgl. Infobox 1 , vgl. Abb. 1 ) des Bauchmarks (Kolossalfasern). Im ventralen Nervenstrang liegen meist 3 Nervenfasern, deren Durchmesser bis zu 75 μm beträgt und damit den Querschnitt "normaler" Fasern um das ca. 10fache übersteigt. Damit verbunden ist eine Erhöhung der Leitungsgeschwindigkeit für elektrische Impulse (Aktionspotential, Erregungsleitung). – Das Nervensystem der Gliederfüßer (Arthropoda: Spinnentiere, Krebstiere, Tausendfüßer, Insekten) stimmt in seiner Grundorganisation mit dem Strickleiternervensystem der Ringelwürmer überein (Insekten [Abb.]). In einigen ursprünglichen Gruppen zeigt es noch diesen charakteristischen Bau, während in allen abgeleiteten Gruppen eine verstärkte Zusammenlegung und Konzentrierung der Ganglien und die Herausbildung weiterer übergeordneter Zentren zu beobachten sind. So sind z.B. bei Webspinnen, vielen Insekten und einigen Krebstieren (Krabben) die Ganglien des Bauchmarks zu einem einheitlichen großen Nervenknoten (Ganglion) verschmolzen. – Auch das Gehirn der Gliederfüßer erfährt mit zunehmendem Differenzierungsgrad eine weitere Ausgestaltung (Gehirn [Abb.]; Oberschlundganglion). Die Bauchmarkganglien des Rumpfes und des Hinterleibs entsenden in jedem Segment Axone zu den Muskeln des Rumpfes, der Gliedmaßen und der Atemöffnungen, in den flügeltragenden Segmenten auch zu den Flügelmuskeln und im Hinterleib zum Herzen. Umgekehrt empfangen die Bauchmarkganglien sensible Nervenfasern von den Sinnesorganen der Beine, der Flügel, Cerci, von den inneren Streckrezeptoren usw. Zahlreiche Interneurone in den Ganglien verschalten die Neurone miteinander. Den Bauchmarkganglien kommt eine bedeutende integrierende Funktion zu. So liegen die Bewegungsmuster des motorischen Apparats (u.a. Flügel- und Beinbewegung) in den Ganglien codiert vor und werden nur durch Impulse vom Gehirn ein- bzw. ausgeschaltet. Wie auch bei den Ringelwürmern lassen sich im Bauchmark der Gliederfüßer Riesenfasern feststellen. – Das Eingeweidenervensystem (sympathisches Nervensystem, viscerales Nervensystem) versorgt unabhängig vom motorischen Nervensystem die inneren Organe. Es besteht bei Insekten ( vgl. Infobox 3 ) aus 3 Teilsystemen: dem stomatogastrischen Nervensystem (Frontalganglion, Frontalkonnektive, Hypocerebralganglion, Nervus recurrens), dem unpaaren ventralen Nervensystem (Ventralnerv mit eigenen segmentalen Ästen) und dem sympathischen caudalen Nervensystem (unpaarer Nerv des letzten Abdominalganglions). – Eine besondere Ausbildung hat bei den Gliederfüßern die Verknüpfung des Nervensystems mit dem Hormonsystem (Hormone, Insektenhormone) erfahren. Hieran sind zum einen neurosekretorische Zellen (Neurosekrete) des Nervensystems beteiligt, die z.B. in der Pars intercerebralis und in fast allen Bauchmarkganglien zu finden sind, zum anderen aber auch endokrine Drüsen außerhalb des Nervensystems. Die Koppelung der Systeme erfolgt über die Neurohämalorgane. – Die in dem Stamm Weichtiere (Mollusca: Muscheln, Schnecken, Kopffüßer) ausgeprägte Vielfalt der Lebensformen spiegelt sich in einer entsprechenden Mannigfaltigkeit in der Ausbildung des Nervensystems wider. Der gemeinsame Grundbauplan aller Weichtierklassen beschreibt 6 Paar klar definierter Ganglien: die Oberschlundganglien oder Cerebralganglien, Pedalganglien (Fußganglion), Pleuralganglien, Buccalganglien (Buccalganglion), Intestinalganglien und Visceralganglien (Visceralganglion). Alle Ganglien sind durch Kommissuren und Konnektive miteinander verbunden. In fast allen Klassen der Weichtiere wird jedoch der Lagebezug der Ganglien verändert, und (oder) es kommt zu Verschmelzungen. Bei den beiden ursprünglichsten Klassen der Weichtiere, den Amphineura (Wurmmollusken und Käferschnecken) und den Monoplacophora (Urmützenschnecken, Napfschaler), zeigen sich noch morphologische Anklänge an ein Orthogon. Bei diesen beiden Gruppen besteht das Nervensystem, ausgehend vom Oberschlundganglion, aus 2 Paar Nervensträngen, 1 Paar lateralen und 1 Paar ventralen, die durch zahlreiche Kommissuren verbunden sind. – Die Schnecken(Gastropoda) zeigen einerseits die Anlage des Grundbauplans (6 Ganglienpaare) sehr deutlich, unterliegen aber andererseits durch die Drehung des Eingeweidesacks einer Umkonstruktion, die zu einer Überkreuzung der zu den Parietal- (Parietalganglion) und Visceralganglien führenden Konnektive führt (Chiastoneurie). Eine Besonderheit ist das vom Pedalganglion (Gehirn [Abb.]) ausgehende Nervennetz des Fußes (pedaler Nervenplexus). Im Gegensatz zum primitiven Nervennetz der Hohltiere handelt es sich hier um eine hochspezialisierte Form der Innervierung (sekundäres Nervennetz). Das Nervennetz des Fußes (Podium) steht unter dem zentralnervösen Einfluß des Pedalganglions, zeigt komplizierte sensomotorische Verschaltungen (Sensomotorik), welche die Wellenbewegung des Fußes koordinieren, und scheint eigene Impulszentren zu besitzen. Ein stomatogastrisches Nervensystem ist in Form eines Magen-Darm-Plexus ausgebildet, der über die Buccal- und Visceralganglien innerviert wird. – Das Nervensystem der Kopffüßer(Cephalopoda) weist eine für Wirbellose einmalige Zentralisation (Konzentration) auf. Die in den anderen Klassen einzeln gelegenen Ganglien verschmelzen zu einem großen Komplexgehirn (Gehirn [Abb.]), das zu erstaunlichen integrativen Leistungen (einsichtiges Handeln, Lernen) befähigt ist. Auch bei Kopffüßern gibt es ein Riesenfasersystem, das als "Notsystem" unabhängig arbeitet und schnelle Fluchtreaktionen auslöst. –
Das Nervensystem der Wirbeltiere(Vertebrata) und des Menschen weist einen völlig anderen Bauplan als die bisher besprochenen Nervensysteme auf. Es läßt sich morphologisch in das Zentralnervensystem (Gehirn und Rückenmark) und das periphere Nervensystem (Hirnnerven, Rückenmarksnerven und periphere Ganglien) einteilen. Funktionell unterscheidet man das animale Nervensystem oder somatische Nervensystem – zur Regelung der Beziehung des Organismus zur Außenwelt und der willkürlichen und unwillkürlichen Motorik, und das autonome Nervensystem oder vegetative Nervensystem – zur Regelung der Vitalfunktionen (Atmung, Sekretion, Stoffwechsel, Verdauung, Wasserhaushalt und vieles andere). Das vegetative Nervensystem ist primär nicht dem Bewußtsein untergeordnet (autonom), es wird seinerseits in 3 weitere funktionell und morphologisch unterschiedliche Systeme unterteilt: 1) Sympathikus (vorwiegend verantwortlich für Energieentladung, abbauenden Stoffwechsel; ergotrope Wirkung), 2) Parasympathikus (Energiespeicherung, Erholung, aufbauender Stoffwechsel; trophotrope Wirkung), 3) intramurales System (Nervenfasern und Ganglien in Herz- [Herznerven], Magen- [Magen], Darm- [Darm], Blasen- [Harnblase] und Uteruswand [Gebärmutter], mit gewisser Selbständigkeit). – Grundelemente des Zentralnervensystems oder ZNS sind ein entlang der Längsachse des Tieres dorsal im Körper gelegenes Nervenrohr (Neuralrohr), das Rückenmark und ein Gehirn (Farbtafel) am Vorderende (Kopf). Der Wirbeltierkörper zeigt eine fundamentale Gliederung in 4 Körperregionen, die sich auch in der Zuordnung peripherer Bereiche des Nervensystems zu Abschnitten des ZNS widerspiegelt: 1) Die Leibeswand (somatisches Gebiet) wird über die Spinalnerven des Rückenmarks versorgt. 2) Deutlich getrennt von der Leibeswand ist das Eingeweidenervensystem (viscerales Gebiet), dessen Innervierung einerseits über den Grenzstrang (Truncus sympathicus) des Sympathikus erfolgt und das somit über die Rami communicantes mit den visceralen Neuronen des Rückenmarks verbunden ist (sympathisches Nervensystem). Andererseits findet eine nervöse Versorgung der inneren Organe auch über Seitenzweige der Hirnnerven, insbesondere des Vagus, statt (parasympathisches Nervensystem). 3) Der Kiemendarm(branchiales Gebiet) und seine Derivate bei landlebenden Wirbeltieren (branchiogene Organe, Kehlkopf) werden von Hirnnerven (Branchialnerven) versorgt. 4) Die großen Sinnesorgane des Vorderkopfes (Nase, Augen, statoakustisches Organ) stellen eine gesonderte "Sinnesperipherie" dar und sind über die Hirnnerven I (Olfactorius), II (Opticus) und VIII (Statoacusticus) mit den ihnen zugeordneten Gebieten im Gehirn verbunden. – Das Rückenmark durchzieht als mächtiger Strang den Wirbelkanal. Es ist nervöses Zentralorgan für zahlreiche Reflexe und Automatismen und zugleich Leitungsweg vieler Nervenfasern, welche die übergeordneten Zentren des Gehirns mit der Peripherie verbinden. Entsprechend deutlich läßt sich auch anatomisch eine Untergliederung in einen Eigenapparat und einen Verbindungsapparat feststellen. Der Eigenapparat wird von anatomisch fest verschalteten Reflexbögen aufgebaut, die über Interneurone miteinander verbunden sind. Er ist ohne Beteiligung des Gehirns zu selbsttätigen Leistungen fähig, die ein Grundmuster von Bewegungsabläufen, Stell- und Haltereaktionen (Gleichgewichtsorgane, Gravitationsbiologie, Haltungssinne, Kinästhesie) und oder Schreckreaktionen (Kampf-oder-Flucht-Reaktion) repräsentieren. Diese Schaltwege legen auf der spinalen Ebene elementare motorische Programme fest, deren Ablauf von höheren Zentren nur regulierend beeinflußt wird. Der Verbindungsapparat des Rückenmarks verknüpft sensible bzw. motorische Neurone mit den übergeordneten Zentren des Gehirns. Bei Säugetieren und Mensch tritt ein Verbindungszug, die Pyramidenbahn (Tractus corticospinalis), besonders hervor. Sie verbindet die Zentren der Willkürmotorik in der Großhirnrinde direkt, ohne Umschaltung, mit Motoneuronen im Rückenmark. Auf dieser Bahn werden bewußte, dem Willen unterliegende Bewegungssignale geleitet. Kopien dieser Signale gelangen zum Kleinhirn ( vgl. Abb. 6 ), das eine Koordination der Bewegungsmuster vornimmt und regelnde Signale entsendet. Die motorischen Kleinhirnsignale werden auf Parallelbahnen der Pyramidenbahn geleitet, zuvor aber noch mehrfach in den Kerngebieten des Rautenhirns (Rhombencephalon) umgeschaltet. Dieses System unterliegt nicht dem Willen und wird dem Pyramidenbahnsystem als extrapyramidales System an die Seite gestellt. Zwischen beiden bestehen über Nebenschlußbahnen enge Verbindungen. – Das vegetative oder autonome Nervensystem innerviert die inneren Organe, Herz und Blutgefäße sowie die Drüsen. Es arbeitet vom Willen weitgehend unabhängig (Name!) und tätigt eine Steuerung des inneren Milieus (Atmung, Verdauung, Blutkreislauf, Körpertemperatur, Hormondrüsentätigkeit). Das vegetative Nervensystem ist zentral eng mit dem somatisch-motorischen System verknüpft. Im Zentralnervensystem sind daher die Anteile der beiden Systeme morphologisch nicht zu trennen. Eine deutliche Trennung zeigt sich aber in der Peripherie: das periphere vegetative Nervensystem gliedert sich in einen sympathischen (Sympathikus, sympathisches Nervensystem) und einen parasympathischen (Parasympathikus, parasympathisches Nervensystem) Anteil. Die Zellkörper eines Teils der sympathischen Neurone liegen im Brust- und Lendenbereich des Rückenmarks. Von dort entsenden sie Axone zu den Ganglien des Grenzstrangs und den Bauchganglien, in denen die Erregungsmuster auf Neurone umgeschaltet werden, die zu den Bestimmungsorganen leiten. Die Zellkörper der parasympathischen Neurone liegen in der Beckenregion des Rückenmarks und im Hirnstamm. Ihre Fasern führen zu Ganglien nahe bei den Bestimmungsorganen. Dort werden sie auf Folgeneurone umgeschaltet, die direkt auf das Organ einwirken. Viele innere Organe werden sowohl durch den Sympathikus als auch durch den Parasympathikus innerviert. Sympathikus und Parasympathikus bilden in der Wandung zahlreicher Hohlorgane (z.B. Herz, Magen), die in ihrer Funktion eine gewisse Selbständigkeit aufweisen, ein Geflecht vegetativer Nervenfasern und Ganglien, die in der topographischen Anatomie als intramurales Nervensystem beschrieben werden. Während der Sympathikus funktionell vorwiegend auf energieverbrauchende und abbauende Prozesse einwirkt (ergotrope Wirkung), hat die parasympathische Innervation eher Beziehungen zur Erholung und Energiespeicherung (trophotrope Wirkung; vgl. Tab. ). Daraus resultiert in einigen Fällen eine antagonistische Wirkung (Antagonismus) der beiden Systeme. Durch die jedoch gleichzeitige Wirksamkeit dieser beiden Systeme entsteht unter normalen Bedingungen keine dauernde einseitige Funktionsänderung, sondern letztlich eher eine synergistische Arbeitsweise (Synergetik). – An der Zusammenarbeit der verschiedenen Teile des Nervensystems sind immer Sekrete beteiligt. Sie können als Neurotransmitter direkt auf postsynaptische Membranen wirken, aber auch, z.B. als Neurohormone, entferntere Orte im Körper erreichen. Diese Form der Neurosekretion (Neurosekrete) des Nervensystems ist phylogenetisch sicher sehr alt und zeigt, daß nervöse und humorale Koordination ursprünglich beide an das Nervensystem geknüpft waren. Auch nach der Entwicklung echter endokriner Drüsen hat das Nervensystem seine übergeordnete Funktion beibehalten und steuert die Ausschüttung der Hormone. – Das Nervensystem unterscheidet sich vom Hormonsystem dadurch, daß es eine Information oder ein Signal gezielt von einer Struktur zu einer anderen weiterleiten kann, während das Hormonsystem den Körper mit einem Stoff, dem Hormon, "überschwemmt" und alle Strukturen, die empfänglich dafür sind, gleichzeitig anspricht. Dennoch können sich beide Systeme gegenseitig beeinflussen (Hormone können durch Nervenimpulse freigesetzt werden oder können ihrerseits in neuronale Prozesse eingreifen) und stehen morphologisch in enger Verbindung, so daß eine Abgrenzung beider Systeme oft schwer fällt (ein Neurotransmitter, z.B. Adrenalin, kann gleichzeitig ein Hormon sein; Nervengewebe können Neurohormone abgeben; endokrine Organe können aus neuronalen Anlagen hervorgehen: das Nebennierenmark [Nebenniere] leitet sich z.B. von sympathischen Ganglien ab). – Zur Funktionsweise des Nervensystems vgl. Infobox 2 , zur Ontogenese vgl. Infobox 4 . Axon, Hormone (Farbtafel), Nerve growth factor, Nervenzelle (Farbtafel I-II), Neurobiologie (Geschichte der) , Neurobionik, neurodegenerative Krankheiten, neuroendokrines System, Neuroethologie, Neuroimmunologie, neuronale Netzwerke, Neuropeptide, Neuropharmakologie, Neurophysiologie, Neuropsychologie, Neurotoxine, neurotrophe Faktoren, Neurowissenschaft, Plastizität, Psychoneuroimmunologie, Synapsen, Telencephalon (Farbtafel). Nervensystem INervensystem II .
M.St./M.L.
Lit.:Brown, A.G.: Nerve Cells and Nervous Systems. An Introduction to Neuroscience, Heidelberg 2001. Eccles, J.C.: Das Gehirn des Menschen. München 61990. Hall, M., Olias, G., Robinson, D.: The Human Nervous System. An Introduction. CD-ROM. Berlin, Heidelberg 2001. Kaestner, A. (Hg.): Lehrbuch der speziellen Zoologie, Bd. I, 1; I, 2; I, 3; I, 4; II, 2; II, 5. Heidelberg 51993–95. Kahle, W.: Taschenatlas der Anatomie, Bd. 3 Nervensystem und Sinnesorgane. Stuttgart 2000. Nicholls, J.G., Martin, R., Wallace, B.G.: Vom Neuron zum Gehirn. Zum Verständnis der zellulären und molekularen Funktion des Nervensystems. Stuttgart 1995. Romer, A.S., Parsons, T.S.: Vergleichende Anatomie der Wirbeltiere. Hamburg 51991. Starck, D.: Vergleichende Anatomie der Wirbeltiere, Bd. 3. Berlin 1982. Zilles, K., Rehkämper, G.: Funktionelle Neuroanatomie. Heidelberg 1998. Wolpert, L.: Entwicklungsbiologie, S. 393–428. Heidelberg 1999.
Nervensystem
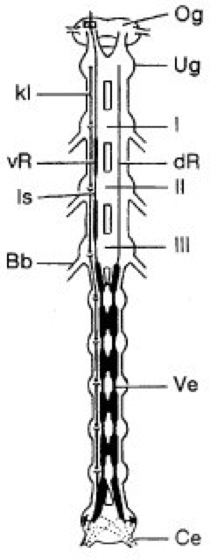
Abb. 1: Organisation der Riesenfasern im Nervensystem der Amerikanischen Schabe (Periplaneta americana). Bb Beinbasis, Ce Cercalnerven, dR dorsale Riesenfasern, Is Isthmus der ventralen Riesenfaser, kI kurzes Interneuron, Og Oberschlundganglion, Ug Unterschlundganglion, Ve Verengung der Riesenfaser, vR ventrale Riesenfaser; I, II und III Pro-, Meso- und Metathorakalganglion
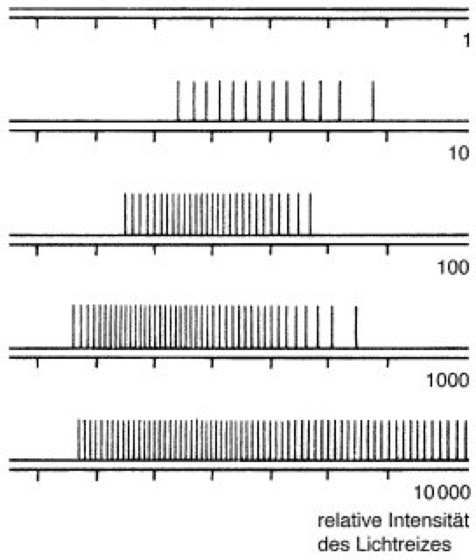
Abb. 2
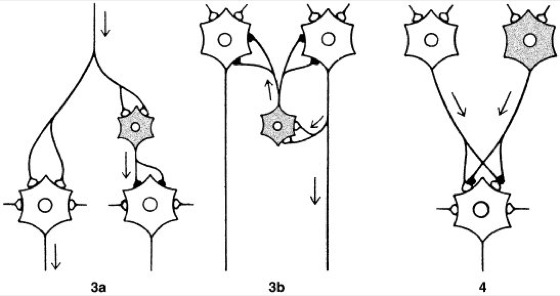
Abb. 3:postsynaptische Hemmungen:a afferente kollaterale Hemmung, b rückläufige (rekurrente) Hemmung.
Abb. 4:präsynaptische Hemmung (grau dargestellte Zellen = hemmende Interneurone)
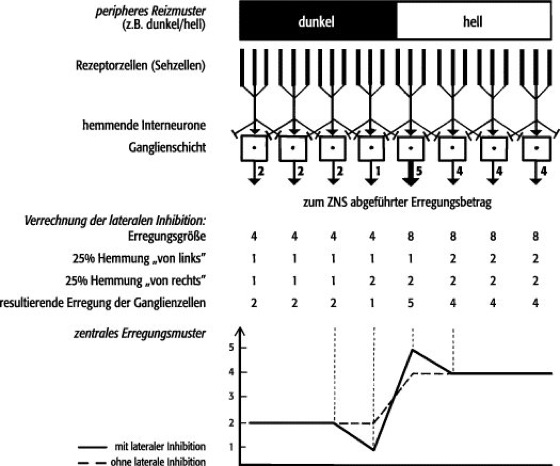
Abb. 5: Schematische Darstellung der lateralen (Vorwärts-)Inhibition. Zur Veranschaulichung des Prinzips wurde die durch diese Hemmung verursachte Kontrastüberhöhung anhand von Zahlenbeispielen dargestellt. Vereinfachend wurde eine Linearität zwischen Reizintensität und Erregungsgröße angenommen. Die von den Rezeptoren kommende Erregung wird an die Ganglienzellen weitergegeben, wobei über Kollaterale gleichzeitig hemmende Interneurone erregt werden. Diese wirken mit einer angenommenen Hemmung von 25% (bezogen auf die Erregungsgröße der Rezeptoren) auf die benachbarten Ganglien ein.
Nervensystem
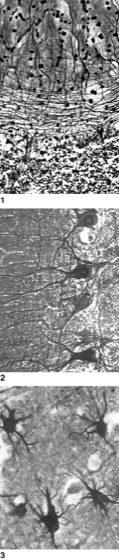
Abb. 6:
Mikroskopische Aufnahmen 1 eines Ausschnitts aus dem Kleinhirn (deutlich sichtbar die komplexe Verschaltung der verschiedensten Typen von Nervenzellen über ein inniges Geflecht zahlloser Nervenfortsätze), 2 von Neuronen (Purkinje-Zellen) des menschlichen Kleinhirns (mit sichtbaren Zellkörpern und reich verzweigtem Dendritensystem), 3 von Astrocyten

Nervensystem
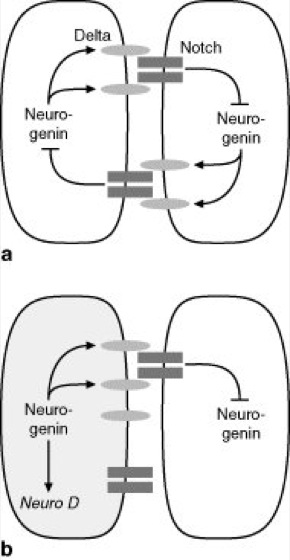
Abb. 7: In einem proneuralen Cluster beginnt eine Zelle als erste, über ein Signal ihre Nachbarzellen daran zu hindern, neuronale Vorläuferzellen zu werden (laterale Inhibition). So wird nur diese hemmende Zelle selbst zur neuronalen Vorläuferzelle und bildet über nachfolgende Zellteilungen Neurone und Gliazellen aus, während ihre Nachbarzellen sich zu Epidermiszellen differenzieren.
Nervensystem
Abb. 8: Spezifizierung von neuronalen Vorläuferzellen bei Xenopus. Zellen in der Neuralplatte synthetisieren zunächst Neurogenin, aber auch die transmembranen Moleküle Delta (als Signal) und Notch (als Rezeptor). Diejenige Zelle in einer Gruppe, die zufällig zuerst mehr Delta produziert, hemmt in benachbarten Zellen über Aktivierung des Notch-Rezeptors die Bildung von Neurogenin und damit die Differenzierung zu Neuronen. In der mehr Delta produzierenden Zelle wird die Neurogenin-Produktion nicht mehr unterdrückt, die Bildung von Neuro D wird aktiviert, und die Zelle wird zur neurogenen Vorläuferzelle.

Nervensystem
Abb. 9: Symmetrische und asymmetrische Teilung von neuronalen Stammzellen in der ventrikulären Proliferationszone im Zentralnervensystem der Wirbeltiere. Die apikale Seite der Zellen im Neuroepithel grenzt an das Lumen des Neuralrohrs. Sich teilende Zellen verlagern das intrazelluläre Numb-Protein nach apikal, das transmembrane Protein Notch-1 nach basal. Bei der symmetrischen Teilung (a, Teilungsebene senkrecht zur Epithelebene) entstehen 2 gleichartige Zellen, die ihren Stammzellcharakter beibehalten. Bei der asymmetrischen Teilung (b, Teilungsebene parallel zur Epithelebene) entsteht apikal eine Stammzelle, die in der Proliferationszone verbleibt, während der nach basal abgegebene Neuroblast später zum Neuron differenziert.
Wenn Sie inhaltliche Anmerkungen zu diesem Artikel haben, können Sie die Redaktion per E-Mail informieren. Wir lesen Ihre Zuschrift, bitten jedoch um Verständnis, dass wir nicht jede beantworten können.