Lexikon der Chemie: Alkine
Alkine, Acetylene, im engeren Sinne ungesättigte, eine C≡C-Dreifachbindung enthaltende Kohlenwasserstoffe der allg. Formel CnH2n-2. Im weiteren Sinne gehören zu dieser Stoffklasse auch Kohlenwasserstoffe mit mehreren Dreifachbindungen, die isoliert oder konjugiert sein können und im Pflanzenreich weit verbreitet sind, z. B. in Korbblütlern. Die A. bilden eine homologe Reihe von Verbindungen (Tab.), beginnend mit Ethin (Acetylen).
Erstmals beim Butin treten wegen der unterschiedlichen Lage der Dreifachbindung in der Kohlenstoffkette Konstitutionsisomere auf (But-1-in und But-2-in). Da die Dreifachbindung aus sp-hybridisierten C-Atomen aufgebaut wird, gibt es keine E,Z-Isomerie. Über die Bezeichnung der A. Nomenklatur, Abschn. C III.
Alkine. Tab.: Homologe Reihe
| ||
| Propin | HC≡C-CH3 | |
| But-1-in | HC≡C-CH2-CH3 | |
| But-2-in | CH3-C≡C-CH3 | |
| Pent-1-in | HC≡C-CH2-CH2-CH3 | |
| Pent-2-in | CH3-C≡C-CH2-CH3 | |
| Hex-1-in | HC≡C-CH2-CH2-CH2-CH3 |
Eigenschaften. Alk-1-ine haben im Vergleich zu den Alkanen höhere Siedepunkte. Das technisch bedeutsame Ethin sowie Propin und But-1-in sind bei Zimmertemperatur gasförmig, die höheren Homologen flüssig. Die relativ höheren Siedepunkte sind auf zwischenmolekulare Wechselwirkungen infolge permanenter Dipolmomente D bei Alk-1-inen von 0,75 bis 0,9 D zurückzuführen. Ethin ist im Gegensatz zu Ethan und Ethen in Wasser besser löslich und leichter zu verflüssigen, explodiert jedoch in dieser Form bei Stoß oder beim Erhitzen mit großer Brisanz. A. brennen mit rußender Flamme, Ethin bei ausreichender Luftzufuhr mit hell leuchtender Flamme. Im Gemisch mit Luft oder Sauerstoff sind Ethin und weitere Homologe, darunter auch Di- und Polyine, außerordentlich explosiv. Eine weitere Besonderheit von Ethin und Alk-1-inen besteht darin, daß sie CH-acid sind, d. h., daß die an die sp-hybridisierten C-Atome gebundenen H-Atome durch Metall-Ionen substituierbar sind. Die entstehenden Metallverbindungen heißen Acetylide.
Reaktionen. Für A. sind ebenso wie für Verbindungen mit C=C-Doppelbindungen (Alkene) Additionsreaktionen typisch. Meistens können diese Reaktionen so geführt werden, daß entweder substituierte Alkene oder die völlig ungesättigten Alkanderivate entstehen. Bei der katalytischen Hydrierung reagieren Dreifachbindungen schneller als Doppelbindungen, bei vielen anderen Additionsreaktionen ist die Reaktivität der A. geringer als die der Alkene. Weitere Reaktionen Acetylenchemie.
Analytisches. Zum chem. Nachweis von A. mit endständiger Dreifachbindung kann die Bildung von Kupfer(I)- und Silber(I)-acetyliden in ammoniakalischer Lösung herangezogen werden. Im IR-Spektrum erscheint die C≡C-Valenzschwingung im Bereich von 2080 bis 2280 cm-1, während die C-H-Valenzschwingung bei etwa 3300 cm-1 auftritt. Die UV-Absorption nichtkonjugierter C≡C-Bindungen liegt unterhalb 200 nm. In den 1H-Kernresonanzspektren erscheinen Signale acetylenischer Protonen bei Werten zwischen δ = 2 bis 3 ppm. Außerdem beobachtet man oft long-range-Kopplungen, d. h. Kopplungen über mehr als drei Bindungen.
Herstellung. Großtechnisch wird nur das wichtigste A., Ethin, erzeugt. Homologe A. oder Cycloalkine kann man durch folgende Methoden erhalten: 1) Dehydrohalogenierung von 1,2- oder 1,1-Dihalogenverbindungen bzw. Halogenvinylverbindungen mit alkoholischer Kaliumhydroxidlösung oder mittels Natriumamid:
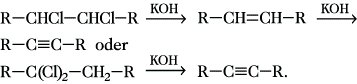
2) Oxidation von Bishydrazonen von 1,2-Diketonen mit Quecksilber(II)-oxid:
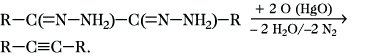
Auf diesem Weg können auch niedere Cycloalkine, wie Cyclopentin oder Cyclohexin, gebildet werden, allerdings konnten diese stark gespannten Verbindungen bisher nur durch Folgereaktionen nachgewiesen werden.
3) A. mit endständiger C≡C-Dreifachbindung können durch Erhitzen mit Kupfer(II)-Salzen in Pyridin zu Diinen gekuppelt werden (Glaser-Reaktion).
Verwendung.Ethin, Acetylenchemie. Homologe A. werden für Synthesen in wissenschaftlichen Laboratorien verwendet.
Wenn Sie inhaltliche Anmerkungen zu diesem Artikel haben, können Sie die Redaktion per E-Mail informieren. Wir lesen Ihre Zuschrift, bitten jedoch um Verständnis, dass wir nicht jede beantworten können.