Lexikon der Chemie: Aminophenole
Aminophenole, Phenole, die eine oder mehrere Aminogruppen am aromatischen Kern enthalten. A. sind amphoter, d. h., sie weisen sowohl sauren als auch basischen Charakter auf, wobei die basischen Eigenschaften dominieren. Die wichtigsten A. sind die drei isomeren 2-, 3- oder 4-A.
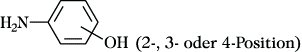
2-Aminophenol (o-Aminophenol), farblose Blättchen oder Nadeln; F. 174 °C, Sublimation bei 153 °C und 1,47·103 Pa. Es ist in kaltem Wasser wenig, in Alkohol und Ether besser löslich. Die Herstellung erfolgt durch Reduktion von 2-Nitrophenol mit Eisen in schwach saurer Lösung bzw. durch Reduktion von Nitrobenzol über das als Zwischenprodukt entstehende Phenylhydroxylamin, das sich unter den sauren Reaktionsbedingungen zu 2- und 4-A. umlagert. 2-A. wird zur Herstellung von Farbstoffen, pharmazeutischen Produkten und Haarfärbemitteln verwendet.
3-Aminophenol (m-Aminophenol), farblose, hexagonale Prismen; F. 123 °C, Kp. 164 °C bei 1,47·103 Pa. Es ist in Wasser schwer, in Alkohol und Ether leicht löslich. 3-A. wird vorwiegend aus 3-Aminobenzolsulfonsäure durch Einwirkung von Alkalihydroxiden oder aus Resorcin und Ammoniak in Gegenwart von Katalysatoren gewonnen. Es wird zur Herstellung der therapeutisch wichtigen Aminosalicylsäure sowie zur Synthese von Rhodaminfarbstoffen verwendet.
4-Aminophenol (p-Aminophenol), farblose Blättchen; F. 186 bis 187 °C, Subl. bei 180 °C und 3,6·102 Pa. Es ist schwer löslich in Wasser, etwas löslich in Alkohol, löslich in Chloroform und Benzol. Die wichtigste Methode zur Herstellung von 4-A. ist die Reduktion von 4-Nitrophenol mit Eisen in schwach saurer Lösung oder durch Reduktion von Nitrobenzol (s. o.). 4-A. wird als photographischer Entwickler eingesetzt. Außerdem wird es zur Herstellung modifizierter Photoentwickler sowie für Schwefel- und Azofarbstoffe verwendet.
Wenn Sie inhaltliche Anmerkungen zu diesem Artikel haben, können Sie die Redaktion per E-Mail informieren. Wir lesen Ihre Zuschrift, bitten jedoch um Verständnis, dass wir nicht jede beantworten können.