Lexikon der Chemie: Androgene
Androgene, eine Gruppe von Steroiden, die als männliche Sexualhormone wirken. Die natürlichen A. leiten sich vom Androstan ab, sie enthalten damit 19 C-Atome und besitzen Sauerstoffunktionen am C-Atom 3 und C-Atom 17. Hauptvertreter der natürlichen A. ist Testosteron, 4-Androsten-3,17-dion. Daneben haben aber auch andere Derivate des Androstans, wie z. B. der Testosteronmetabolit Androsteron, eine – wenn auch wesentlich geringere – androgene Wirkung. Testosteron wird in den Interstitialzellen des Hodens, den sog. Leydigschen Zellen, unter dem Einfluß des gonadotropen Hormons (Gonadotropine) gebildet. Die Biosynthese verläuft über 17α-Hydroxyprogesteron durch Abspaltung der C2-Kette am C-Atom 17 zu 4-Androsten-3,17-dion, das zu Testosteron reduziert wird.
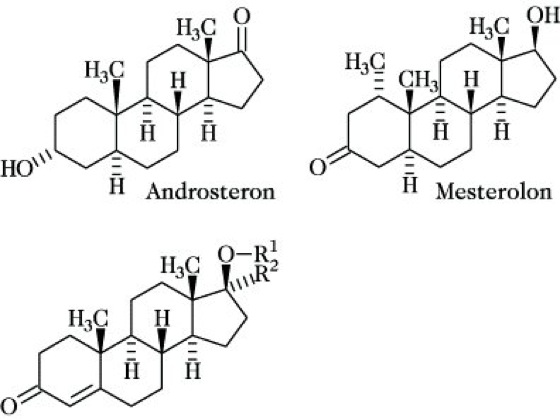
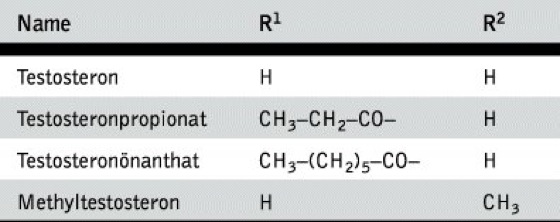
Testosteron ist partialsynthetisch aus Androstenolon (5-Androsten-3-ol-17-on) oder auf mikrobiologischem Wege aus Progesteron zugänglich. Zu den sexualspezifischen Wirkungen des Testosterons zählen die Ausbildung der sekundären männlichen Geschlechtsmerkmale, die Aufrechterhaltung der Funktion der akzessorischen Drüsen des Genitaltrakts, die Spermiogenese und die Erhaltung der Libido. Zu den sexualunspezifischen Wirkungen rechnet die anabole Wirkung (Anabolika). Testosteron wird zur Substitutionstherapie bei zu niedrigem Androgengehalt verschiedener Genese eingesetzt. Es kommt nach oraler Anwendung wegen zu schneller Metabolisierung nicht zur Wirkung und wird deshalb parenteral appliziert. Häufiger als Testosteron werden wegen deren längerer Wirkungsdauer seine Ester, wie Testosteronpropionat, eingesetzt. Ester mit längerkettigen Fettsäuren, wie z. B. das Önanthat, entfalten eine Depotwirkung. Oral wirksame Testosteronderivate sind Methyltestosteron mit einer 17α-ständigen und Mesterolon mit einer 1α-ständigen Methylgruppe. Die 17α-ständige Methylgruppe verhindert die Dehydrierung zu 17-Ketoverbindungen, die 1α-ständige Methylgruppe die Anlagerung an metabolisierende Enzyme.
Wenn Sie inhaltliche Anmerkungen zu diesem Artikel haben, können Sie die Redaktion per E-Mail informieren. Wir lesen Ihre Zuschrift, bitten jedoch um Verständnis, dass wir nicht jede beantworten können.