Lexikon der Chemie: Cellulose
Cellulose, β-D-(1→4)-Glucan, ein Homopolysaccharid, das aus 1→4-β-glucosidisch verbundenen Anhydro-D-glucose-Einheiten aufgebaut ist, häufigste an der Erdoberfläche vorkommende organische Substanz. Im gesamten Pflanzenmaterial vorkommende C.-Menge wird mit 26,5 × 1010 t angegeben. Verschiedene Pflanzen und Pflanzenteile enthalten unterschiedliche Anteile an Cellulose (Abb. 1).
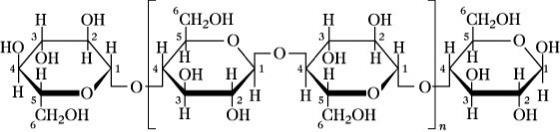
Cellulose. Abb. 1: Strukturformel der Cellulose.
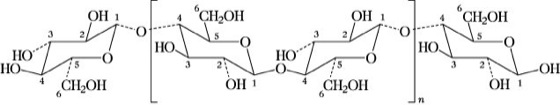
Cellulose. Abb. 2: Konformationsschema der Cellulose.
Baumwolle 95-99 %, Baumrinden 20-30%, Moose 25-30 %; am Aufbau des Holzes ist die C. mit 40-44 % beteiligt.
Auf Grund dieser Verknüpfungsart entsteht ein fadenförmiges Makromolekül mit einem reduzierenden Ende (Aldehydgruppe in Halbacetalform am Kohlenstoff 1) und ein nichtreduzierendes Ende (sekundäre Hydroxygruppe am Kohlenstoff 4). Alle Glucoseeinheiten liegen in der Sesselform vor, so daß folgendes Konformationsschema entsteht (Abb. 2).
Die Bruttoformel ist C6pH10p+1O5p+1 (p = Durchschnittspolymerisationsgrad DP).
Je Cellulosemolekül sind in der Cellulose des Holzes etwa 4000-5000 Zuckereinheiten verknüpft (DP = 4000-5000).
Auf Grund des geregelten linearen Aufbaues und des Dipolcharakters der Hydroxygruppen kommt es zur Ausbildung von intra- und intermolekularen Wasserstoff-Brückenbindungen. Es entsteht eine übermolekulare Struktur aus geordneten (kristallinen) und weniger geordneten (parakristallinen) Bereichen.
Der Anteil der kristalinen Cellulose an der Gesamtcellulose des Holzes beträgt 50-70 % (meist etwa 70 %). Diese strukturelle Besonderheiten sind wichtig für die Quell- und Reaktionseigenschaften der Cellulose.
Bei Behandlung mit starken Alkali-Lösungen entsteht aus der nativen Cellulose (Cellulose I) die sog. Hydratcellulose (Cellulose II), die trotz gleichen chemischen Aufbaues ein aufgeweitetes Gitter in den kristallinen Bereichen aufweist, wodurch eine raschere Aufnahme von Wasser, Farbstoffen oder Reaktanten erfolgen kann.
Lösung der C. C. ist in den üblichen Lösungsmitteln nicht löslich. Sie kann gelöst werden in wässrigen Lösungen, in denen Hydroxide mit einem voluminösen Basenkation enthalten sind:
· Basen von Ammonium-Komplexen z. B.
[Cu(NH3)4]2+
Schweizer Reagenz (Kupfer(II)-hydroxid),
"Cuoxam";
· Basen von Amin-Komplexen z. B. [Cu(en)2]2+ "Cuoxen", [Cd(en)3]2+ Cadoxen, [Co(en)3]2+ Cooxen etc. (en = Ethylendiamin, H2N-CH2-CH2-NH2)
· Quarternäre Ammoniumbasen [NR4]+
(R = z. B. Alkyl);
· Eisen-Natriumtartrat-Komplex (Eisen-Weinsäure-Natrium-Komplex ![]()
EWN).
Weiterhin kann Cellulose in konzentrierten starken Mineralsäuren, z. B. Schwefelsäure, Trifluoressigsäure) und einigen nichtwässrigen Zwei- (z. B. SO2 + aliphatisches Amin; DMSO + Formaldehyd) und Dreikomponentenlösungsmitteln (SO2 + aliphatisches Amin + DMSO, Triethylamin + Harnstoff + Dimethylsulfoxid) in Lösung gebracht werden.
Substitutionsreaktionen an der C. Ziel der Substitutionsreaktionen an der C. ist die Erzeugung von Produkten mit modifizierten Eigenschaften und damit die Verbreiterung der Einsatzmöglichkeiten. Meist wird die C. in eine lösliche Form überführt und in Form von Fasern, Folien etc. umgeformt oder mit Plastifikatoren verknetet und zu Formteilen verarbeitet oder aber in Kleb- und Anstrichstoffen als Lösung bzw. Dispersion eingesetzt.
Grundsätzlich kann zwischen Veresterungs-, Veretherungs- und Pfropfreaktionen an der C. unterschieden werden. Im folgenden einige wichtige Beispiele:
Veresterungsreaktionen.
- Nitrierung: Erzeugung von Nitrocellulose. (Cellulosenitrat) durch Umsetzung von C. mit Salpetersäure, Schwefelsäure, Wasser im molaren Verhältnis 1 : 2 : 2.

- Acetylierung: Erzeugung von Acetylcellulose (Celluloseacetate) durch Umsetzung von C. mit Essigsäure, Acetanhydrid und kleinen Mengen Schwefelsäure
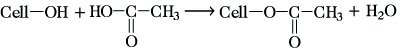
- Xanthogenierung: Erzeugung von Cellulose-xanthogenat (Natriumsalz des Dithiokohlensäureesters der C.) durch Umsetzung von C. mit Natronlauge und danach mit Schwefelkohlenstoff
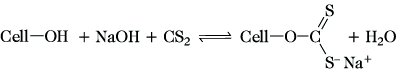
Diese reversible Veresterungsreaktion ist die Grundlage für die Herstellung von Celluloseregeneraten, die als Viskose-Fasern, -Folien, -Schwämmen umfassend verwendet werden.
Veretherungsreaktionen.
- Alkylether, z. B. Methylcellulose, entsteht durch Umsetzung von C. mit Alkylchlorid im alkalischen Medium:
Cell-OH + Cl-CH3 → Cell-O-CH3 + HCl
- Hydroxyalkylether, z. B. Hydroxyethylcellulose:
Cell-OH + Cl-CH2-CH2OH →
Cell-O-CH2-CH2-OH + HCl
- Carboxymethylcellulose erhält man durch Umsetzung von C. mit Chloressigsäure:
Cell-OH + Cl-CH2-COO- Na+ →
· Cell-O-CH2-COO- Na+ + HCl
Cyanoethylcellulose:
Cell-OH + Cl-CH2-CH2-CN →
Cell-O-CH2-CH2-CN + HCl
· Aminoethylierung, z. B. Diethylaminoethylcellulose (DEAE-Cellulose):
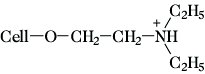
- Hydrolyse der glucosidischen Bindungen, bedeutsam z. B. bei der Holzverzuckerung, bei dem sauren Sulfitaufschluß des Holzes, enzymatische Hydrolyse z. B. im Verdauungstrakt von Wiederkäuern;
- alkalischer Abbau ("peeling"-Reaktion), bedeutsam z. B. bei den alkalischen Holzaufschlußverfahren: Alkalisch-oxidativer Abbau vom reduzierenden Ende der Polysaccharidenketten her;
- thermischer Abbau, bedeutsam z. B. bei der Erzeugung von Holzkohlen und Kohlenstoffasern;
- oxidativer Abbau, bedeutsam z. B. bei der Erzeugung modifizierter C.-Produkte (Oxocellulose etc.);
- photochemischer Abbau, bedeutsam z. B. bei der Vergilbung und Versprödung von Papieren;
- biochemischer Abbau, bedeutsam z. B. bei der Bildung von Humus aus Pflanzenmaterial;
- mechanochemischer Abbau, bedeutsam z. B. bei der mechanischen Bearbeitung des Holzes und der Cellulose.
Gewinnung von C. Zellstoff.
Verwendung. C. ist ein sehr vielseitig nutzbarer Rohstoff. Für die Textilindustrie ist C. der wichtigste Bestandteil der Faserrohstoffe, insbesondere der Baumwolle. Als Textilfaser wird auch die regenerierte C. eingesetzt (Cuprofasern, Viskosefasern). C. ist weiterhin wesentlicher Bestandteil von Papier und Pappe. Sehr reine Celluloseprodukte sind Verbandmaterialien, wie Verbandwatte, -mull und -zellstoff. Die durch Abbau von C. säurehydrolytisch erhaltenen Zucker (Holzverzuckerung) können weiter zu Ethanol verarbeitet werden. Vielseitig angewandt werden zahlreiche chemisch modifizierte C., insbesondere Ether (Ethyl-, Benzyl-, Methyl- und Carboxymethylester) und Ester (Acetate, Propionate, Acetobutyrate, Nitrate und Xanthogenate) der C.

Wenn Sie inhaltliche Anmerkungen zu diesem Artikel haben, können Sie die Redaktion per E-Mail informieren. Wir lesen Ihre Zuschrift, bitten jedoch um Verständnis, dass wir nicht jede beantworten können.