Lexikon der Chemie: chemische Kampfstoffe
chemische Kampfstoffe, industriell herstellbare chem. Substanzen oder Gemische von Substanzen, die wegen ihrer akuten Toxizität im Sinne tödlicher oder zeitweilig schädigender Wirkungen zu militärischen Zwecken verwendet werden.
C. K. wurden zuerst unter Verwendung von Abblasverfahren eingesetzt, später dominierte der artilleristische Einsatz und die Verwendung spezieller Gaswerfer. Moderne Einsatzmittel für die c. K. umfassen Artilleriegranaten, Bomben, Raketen-Gefechtsköpfe, Minen, Flugzeugabsprühgeräte sowie spezielle Einsatzmittel für Reizkampfstoffe. Der Einsatz von c. K. ist völkerrechtlich durch das Genfer Abkommen von 1925 verboten, ihre Beschaffung durch das C-Waffen-Übereinkommen von 1997 international geächtet.
Einteilung der c. K.Die "klassische" militärische Unterteilung der c. K. in Weißkreuzkampfstoffe, Grünkreuzkampfstoffe und Gelbkreuzkampfstoffe gilt heute als überholt und hat lediglich historische Bedeutung. Nach modernen militärischen Gesichtspunkten unterscheidet man: tödlich oder nicht tödlich wirkende c. K., c. K. mit langsamem oder schnellem Wirkungseintritt, c. K. mit langer oder kurzer Wirkungsdauer, bevorzugt zur Luftraum- oder zur Oberflächenvergiftung geeignete (flüchtige oder seßhafte) c. K. Die Klassifikation erfolgt dabei sowohl nach toxikologischen als auch nach physikalisch-chem. Eigenschaften. Hauptparameter sind toxische (letale oder schädigende) Dosis, Latenzzeit, Seßhaftigkeit und beabsichtigte Einsatzart.
Nach toxikologischen Aspekten und unter Berücksichtigung anderer Eigenschaften können c. K. wie folgt unterschieden werden (s. auch Tab. S. 236).
1) Reizerregende c. K.Es handelt sich um Vertreter verschiedener chem. Stoffklassen, insbesondere um halogenierte bzw. arsenorganische Verbindungen. Zu den vorwiegend augenreizend wirkenden c. K. (Augenreizstoffe) zählen als wichtigste Vertreter ω-Chloracetophenon (CN), 2-Chlor-benzylidenmalodinitril (CS) und das Dibenz-(b,f)-1,4-oxazepin (CR). Augenreizstoffe wirken auf die sensiblen Nervenendigungen der Augenschleimhäute. Als Wirkungsmechanismen werden Enzyminhibierungen durch Blockade von Thiolgruppen angesehen. Hauptsymptome sind Brennen und Stechen der Augen, Tränenfluß, Fremdkörpergefühl, Lidschluß, zeitweilige Blindheit und Bindehautentzündungen. In hohen Konzentrationen sind bleibende Augenschäden möglich. Schädigungen der oberen Atemwege können ebenfalls bei hohen Dosen auftreten, in schweren Fällen verlaufen sie unter Ausbildung eines toxischen Lungenödems tödlich. Für CS wurden darüber hinaus bei längerer Einwirkungsdauer auf der ungeschützten Haut Erythembildungen und Blasenbildung beschrieben.
C. K., die überwiegend die oberen Atemwege reizen, werden allgemein als Nasen- und Rachenreizstoffe bezeichnet. Zu ihnen zählen als die wichtigsten Vertreter arsenorganische Verbindungen wie das Diphenylchlorarsin (Clark 1), das Diphenylcyanarsin (Clark 11) und das (auch heute noch aktuelle) Diphenylaminchlorarsin (Adamsit). Weitere Vertreter findet man unter den bleiorganischen Verbindungen, meist Trialkylverbindungen. Nasen- und Rachenreizstoffe verursachen Reizungen der Schleimhäute im Nasen- und Rachenraum, daneben aber auch der Augen. Als Wirkungsmechanismus wird die Blockade von Thiolgruppen diskutiert. Die Latenzzeit kann bis zu 30 Minuten betragen, als Symptome stehen Husten- und Niesreiz im Vordergrund, hinzu kommen verstärkte Sekretion der Nasenschleimhaut und Speicheldrüsen. Weitere Wirkungen sind Atemnot, Kopfschmerz und Schmerzen im Brustbeinbereich. In hohen Dosen kann die Vergiftung tödlich verlaufen (Lungenödem).
2) Psychotoxische c. K.Hierbei handelt es sich um Substanzen, die zeitweilig psychische Anomalien (z. B. Modellpsychosen) auszulösen vermögen. Sie wirken bereits in extrem niedrigen Dosierungen, zur Vergiftung eines Menschen werden Milligramm- bis Mikrogrammmengen benötigt. Man kann differenzieren zwischen psychotomimetischen Stoffen, die Modellpsychosen auslösen, und psychotropen Stoffen, die die psychische Handlungsfähigkeit beeinträchtigen. Unter militärischen Gesichtspunkten bedeutsam sind Phenylglycolsäureester oder Benzilsäureester heterocyclischer Iminoalkohole, daneben wurden Lysergsäurederivate, Tryptaminderivate, Phenylallcylamine und Cannabinolderivate getestet. Munitioniert wurde das 3-Chinuclidinylbenzilat (BZ). Hauptsymptome einer BZ-Vergiftung sind auffallende Verwirrtheit, Desorientierung und psychomotorische Erregungen, daneben Halluzinationen verschiedener Art. Seine militärische Wirksamkeit wurde wegen der unvorhersagbaren Wirkung zweifelhaft.
3) Hautschädigende c. K.Es handelt sich um allgemein langwirkende, also seßhafte c. K., die zeitweilig oder langdauernd außergefechtsetzende oder auch tödliche Vergiftungen bewirken. Im klinischen Bild steht dabei die Schädigung der Haut und der Schleimhäute im Vordergrund. Chemisch handelt es sich um halogenierte Derivate von Thioethern, tertiären Aminen, primären Arsinen und Oximen. Militärisch bedeutsam sind das bereits im ersten Weltkrieg eingesetzte Bis-(2-chlor-ethyl)sulfid (S-Lost, Yperit, Senfgas, Mustard), die von ihm abgeleiteten N-Alkyl-bis-(2-chlorethyl)amine bzw. N-Alkyl-tris-(2-chlorethyl)amine (N-Loste), das 2-Chlorethenyldichlorarsin (Lewisit) und einige halogenierte Oxime, z. B. Dichlorformoxim. Die toxischen Eigenschaften der hautschädigenden c. K. werden auf ihre Fähigkeit zur Bildung heterocyclischer Onium-Ionen zurückgeführt, die ihrerseits zu einer Vielzahl von Reaktionen befähigt sind und mit Zellbestandteilen wie Proteinen und Aminosäuren (Hämoglobin, Serumalbumin und -globulin, Cystein, Lysin, Arginin, Histidin) in Wechselwirkung treten können. Der Wirkungseintritt erfolgt bei halogenierten Thioethern und Aminen verzögert (Latenzperiode symptomfrei), bei halogenierten Arsinen und Oximen sofort. Je nach Dosis rufen sie Hautrötungen, Blasenbildung oder nekrotische Gewebezerstörungen hervor. Daneben beobachtet man systemische toxische Wirkungen wegen der relativ hohen Resorption in die Körperflüssigkeiten verbunden mit unspezifischen alkylierenden Wirkungen, insbesondere bei den Lostderivaten. Halogenalkylamine sind besonders potente Inhibitoren enzymatischer Prozesse. Lostderivate können verschiedene Organe (Leber, Niere, Milz, Hirn, Magen-Darm-Trakt, Herz, Lunge) schädigen. Die das Vergiftungsbild bestimmenden Hautschäden zeigen eine außerordentlich schlechte Heilungstendenz bei stark reduzierter allgemeiner Widerstandsfähigkeit des Organismus (Gefahr von Sekundärinfektionen). Die toxischen Wirkungen des Lewisit ähneln denen der Loste, allerdings ist die Heilungstendenz bei überstandener Vergiftung günstiger. Halogenierte Oxime bewirken ohne Latenzzeit heftiges Brennen und starken Schmerz auf der Haut, dazu kommen Quaddelbildung und Entzündungen. Man spricht daher oft von Nesselstoffen.
Lostderivate weisen ein hohes chem. Alkylierungspotential auf. Damit erklärt man die beobachteten Spätschadeneffekte nach überstandenen akuten oder subakuten Intoxikationen bzw. der längerdauernden Exposition in kleinsten Dosen. S-Lost ist eines der potentesten Kanzerogene.
4) Lungenschädigende c. K. Sie waren militärisch während des ersten Weltkrieges von Bedeutung. Die Hauptvertreter sind Chlor und Phosgen, daneben wurden Chlorkohlensäuretrichlormethylester (Diphosgen) und Kohlensäure-bis-(trichlormethyl)-ester (Triphosgen) verwendet, die bei der Anwendung thermisch in zwei bzw. drei Mole Phosgen gespalten werden. Außerdem hatte das Chlorpikrin eine gewisse Bedeutung. Die Wirkungsdauer von lungenschädigenden c. K. ist kurz, ihr Wirkungseintritt verzögert. Lungenschädigende Kampfstoffe rufen ein toxisches Lungenödem hervor (Latenzzeit bis zu einigen Stunden).
5) Allgemeingiftige c. K.Es handelt sich meist um kurzzeitig und schnell wirkende c. K., die während des ersten Weltkrieges eine gewisse Rolle spielten. Hauptvertreter sind Cyanwasserstoff (Blausäure), Halogencyane, Arsen- und Phosphorwasserstoff sowie Kohlenmonoxid. Die toxische Wirkung der genannten c. K. beruht auf der spezifischen Beeinflussung enzymatischer Vorgänge bzw. Stoffwechselprozesse, insbesondere im Blut, Gifte. Weitere bedeutsam Stoffgruppen sind die Derivate der Fluoressigsäure, Gifte, Sabotagegifte.
6) Nervenschädigende c. K.Nervenschädigende phosphororganische c. K. sind die derzeit bedeutsamsten c. K. Der erste Vertreter dieser Gruppe wurde 1936 in Deutschland von Schrader synthetisiert und war das militärisch heute weniger relevante Dimethylaminoethylcyanophosphat (Tabun). Hauptvertreter sind das O-Isopropylfluormethylphosphonat (Sarin, GB), das O-Pinacolylfluormethylphosphonat (Soman, GD) und die V-Kampfstoffe, von denen der militärisch bedeutsamste Vertreter O-Ethyl-S-(N,N-diisopropylaminoethyl)-methylphosphonnothiolat (VX) ist. Sarin dient wegen seiner relativ hohen Flüchtigkeit vorwiegend zur Luftraumvergiftung, VX ist dagegen ein seßhafter Kampfstoff besonders zur Geländevergiftung. Phosphororganische Nervenkampfstoffe werden sowohl inhalativ als auch – vor allem im Falle der V-Stoffe – über die Haut resorbiert. Das Vergiftungsbild wird primär bestimmt durch die Blockade der Acetylcholinesterase, eines Enzyms mit einer Schlüsselfunktion im Bereich cholinerger Nerven (Synapsen) sowie an den Synapsen der motorischen Endplatten der Muskulatur (Gifte). Dadurch wird der enzymatische Abbau des Neurotransmitters Acetylcholin unterbunden, es kommt zu einer endogenen Acetylcholinvergiftung. Die Hauptsymptome von Vergiftungen mit nervenschädigenden Kampfstoffen können unterschieden werden in nicotinartige, muscarinartige und zentrale Symptome. Herzfrequenz und -kraft sind herabgesetzt, Pupillen verengt (Miosis), die Blutgefäße des Herzens und der Bronchien verengt, diejenigen von Lunge, Haut und Muskulatur erweitert. Es kommt zu unfreiwilligen Urin- und Kotabgängen. Bei den zentralen Symptomen stehen im Vordergrund Krämpfe sowie die Lähmung des Atemzentrums, die meist die Todesursache ist (Atemstillstand). Zur Therapie werden direkte Cholinolytika (Atropin) eingesetzt, die die Wirkung des endogen gebildeten Acetylcholinüberschusses durch kompetitive Konkurrenz am Acetylcholinrezeptor unterdrücken. Auch bestimmte Reaktivatoren, die den Gift-EnzymKomplex spalten, werden eingesetzt. Außerdem richtet sich die Therapie auf die Sicherung der Sauerstoffversorgung (künstliche Beatmung) und die Erhaltung der Lebensfunktionen (symptomatische Therapie).
Neben synthetischen Produkten wurden einige natürliche Toxine, insbesondere mikrobielle und tierische Produkte, als militärisch bedeutsam angesehen (Sabotagegifte). Der wohl wichtigste Vertreter war das Botulinustoxin A, ein extrem toxisches Stoffwechselprodukt des Bakteriums Clostridium botulinum. Toxine unterliegen unabhängig von der Art ihrer Herstellung dem völkerrechtlichen Verbot im Rahmen der Konvention zum Verbot biologischer Waffen (abgeschlossen 1972, in Kraft seit 1975), d. h., ihre Entwicklung, Herstellung und Lagerung zu Zwecken der chem. Kriegführung ist völkerrechtlich illegal. Toxine sind ebenfalls durch das C-Waffen-Übereinkommen erfaßt, Ricin und Saxitoxin sind spezifisch im C-W-Übereinkommen geregelt.
Identifikation und Bestimmung von c. K. Die schnelle und sichere Identifikation von c. K. sowie ihre quantitative Bestimmung sind erste notwendige Voraussetzungen zum Schutz vor ihren Wirkungen. Es wurden chem., physikalisch-chem., physikalische und biochem. Methoden zum Schnellnachweis und zur Bestimmung der c. K. entwickelt. Bei den chem. Verfahren stehen Farbreaktionen (Spürröhrchen, Tüpfelreaktionen, Spürpapiere u. dgl.) im Vordergrund, biochem. Verfahren nutzen spezifische Enzymbeeinflussungen (z. B. Blockade von Cholinesterasen) und nachgeschaltete Reaktionen (Farb-, elektrochem. oder anderer Nachweis), sie sind insbesondere für die Phosphororganika außerordentlich empfindlich. Allerdings sind enzymatische Verfahren oft für den Sofortnachweis zu langsam. Unter den physikalisch-chem. Verfahren wurden insbesondere optische, gaschromatographische, massenspektrometrische und ionenbeweglichkeitsspektroskopische Methoden sowohl für den Einsatz in Schnellanalysatoren als auch zum Nachweis und zur quantitativen Bestimmung der c. K. in Laboratorien weiterentwickelt.
Schutz vor den Wirkungen der c. K. Der Schutz vor den Einwirkungen c. K. umfaßt sowohl kollektive Schutzmittel und -einrichtungen (Filteranlagen, Raumhermetisierung) als auch individuelle Schutzmittel (Schutzmasken, Schutzanzüge). Der Schutz ist nur begrenzt erreichbar und hängt neben Ausstattungsgrad und Effektivität der Schutzmittel noch von anderen Faktoren ab (Zeitfaktor, Trainingszustand, Art und Menge des eingesetzten c. K.). Zu den Schutzfaktoren zählen ferner die medizinische Versorgung der Vergifteten, die sich insbesondere beim Massenanfall Geschädigter außerordentlich schwierig gestaltet. Universelle Antidote existieren nicht, für die meisten c. K. sind spezifische Antidote bekannt.
Entgiftung von c. K.Sie kann mit physikalischen, chem. und physikalisch-chem. Verfahren erreicht werden. Nach der Art der zu entgiftenden Objekte kann man nach Personen-, Oberflächen-, Innenraum- und Geländeentgiftung differenzieren. Die Wirksamkeit von Entgiftungsmaßnahmen hängt von verschiedenen Faktoren ab, z. B. Art und Formulierung des c. K., Art und verfügbare Menge des Entgiftungsmittels, meteorologische Faktoren, Zeitpunkt des Beginns der Entgiftungsarbeiten. Entgiftungsarbeiten erfordern geschultes und mit Schutzmitteln ausgestattetes Personal und eine straffe Organisation zur Vermeidung sekundärer Vergiftungen.
chemische Kampfstoffe. Tab.: Die wichtigsten chemischen Kampfstoffe und einige ihrer bedeutsamsten Eigenschaften.
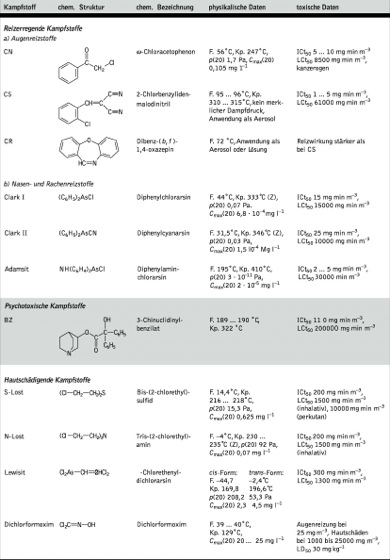
chemische Kampfstoffe. Tab. (Fortsetzung).
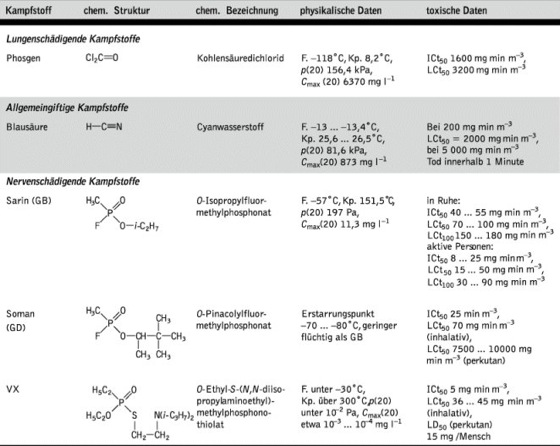
F. Schmelzpunkt, Kp. Siedepunkt bei Normaldruck, p(20) Sättigungsdampfdruck bei 20 °C, Cmax(20) Sättigungskonzentration in Luft bei 20 °C, ICt50 mittlere außergefechtsetzende Konzentration (als Konzentrations-Zeit-Produkt), LD50 mittlere tödlich wirkende Dosis (in mg kg-1), LCt50 mittlere tödlich wirkende Dosis (als Konzentrations-Zeit-Produkt), LCt100 tödliche Dosis für 100 Prozent exportierter Personen. Die angegebenen tödlichen und toxischen Dosen beziehen sich auf den Menschen, sie sind aus tierexperimentellen Daten extrapoliert.
Geschichtliches.C. K. wurden erstmals im ersten Weltkrieg in militärisch bedeutsamen Mengen eingesetzt. Als erster massiver Einsatz von c. K. wird allgemein der Abblasangriff mit Chlorgas am 22. April 1915 durch die kaiserlich-deutschen Truppen in der Schlacht bei Ypern (Belgien) angesehen, auch wenn bereits früher auf französisch-cnglischer und auf deutscher Seite weniger wirksame, reizerregende Chemikalien verwendet worden waren. In der Folgezeit eskalierte auf beiden Seiten der Einsatz von c. K. sowohl hinsichtlich der angewendeten Mengen als auch hinsichtlich der verwendeten chem. Substanzen. Neben Lungengiften (Chlor, Phosgen, Di- und Triphosgen u. a.) wurden neuartige Reizkampfstoffe (Clark I und II) und später Hautkampfstoffe (Yperit oder Lost) angewendet, andere neue c. K. (Adamsit, Lewisit) wurden bis zur Anwendungsreife entwickelt. In den Folgejahren wurden c. K. nur in seltenen Fällen eingesetzt, so während der italienischen Aggression gegen Abessinien Mitte der 30er Jahre und von japanischer Seite während des zweiten Weltkrieges in begrenztem Umfang in China.
Obwohl während des zweiten Weltkrieges kein militärisch bedeutender Einsatz c. K. erfolgte, wurden in dieser Zeit durch Entwicklungsarbeiten in Deutschland die ersten Vertreter der bis heute bedeutsamen phosphororganischen Nervenkampfstoffe (Tabun, Sarin und Soman) entwickelt und zum Teil produziert. Nach Ende des zweiten Weltkrieges verlagerte sich der Schwerpunkt der Entwicklung und Herstellung von c. K. in die damalige Sowjetunion sowie die USA, wo in den 50er Jahren die phosphororganischen V-Kampfstoffe entwickelt und Anfang der 60er Jahre in die Produktion übergeführt wurden. Daneben wurden neuartige, zeitweilig wirkende und die menschliche Psyche schädigende c. K. entwickelt (z. B. BZ). Umfangreiche Anwendungen von c. K. sowie Entlaubungsmitteln erfolgten im Vietnamkrieg durch die USA-Truppen in den Jahren 1961 bis 1971, teilweise auch noch bis 1975 (Phytogifte, insbesondere chlorierte Phenoxyessigsäurederivate, Picloram und Arsenwirkstoffe, außerdem verschiedene Reizkampfstoffe, wie CN und CS). Parallel dazu wurden, beginnend bereits in der Mitte der 50er Jahre, neue Einsatzmittel für c. K. entwickelt, die sogenannten Binärwaffen. Hierbei werden zur Reduzierung des Selbstvergiftungsrisikos die letzten beiden chem. Vorstufen des c. K. in das Einsatzmittel (Granaten, Bomben, Raketen) gefüllt und erst nach Abschuß bzw. Abwurf, d. h. auf dem Wege ins Zielgebiet, miteinander gemischt. In einer chem. Reaktion wird auf dem Wege zum Ziel der eigentliche c. K. gebildet, meist ein phosphororganischer Nervenkampfstoff. Seit den 70er Jahren verschob sich das Gewicht der C-Waffen-Beschaffung und -anwendung in Konfliktzonen der Dritten Welt. Irak setzte c. K. in den 80er Jahren gegen den Iran sowie Kurdensiedlungen im Norden Iraks ein.
Der Einsatz c. K. während des ersten Weltkrieges stellte eine Verletzung geltenden Völkerrechts dar (Haager Landkriegsordnung in der Fassung von 1907, Artikel 23). Dies wurde im Genfer "Protokoll über den chemischen und bakteriologischen Krieg" von 1925 bekräftigt, das dieses Anwendungsverbot auf die bakteriologischen (biologischen) Kampfmittel ausdehnte. Verhandlungen über ein umfassendes Verbot chem. Waffen fanden seit Ende der 60er Jahre im Rahmen des Genfer Abrüstungsausschusses (heute Abrüstungskonferenz genannt) statt. Sie mündeten in die Übergabe des C-Waffen-Übereinkommens an die Vereinten Nationen im September 1992.
Wenn Sie inhaltliche Anmerkungen zu diesem Artikel haben, können Sie die Redaktion per E-Mail informieren. Wir lesen Ihre Zuschrift, bitten jedoch um Verständnis, dass wir nicht jede beantworten können.