Lexikon der Chemie: Desaminierung
Desaminierung, die Eliminierung einer Aminogruppe aus einer organischen Verbindung. Die wichtigste synthetische Methode der D. ist die Diazotierung primärer Amine bzw. Amide und anschließende Stickstoffabspaltung. Das zurückbleibende instabile Carbenium-Ion reagiert in Abhängigkeit von den Reaktionsbedingungen unter Bildung stabiler Reaktionsprodukte. In Gegenwart von Reduktionsmitteln, z. B. Alkohol und Kupfer(I)-oxid, unterphosphoriger Säure, Formaldehyd oder Zinn(II)-Verbindungen, können aromatische primäre Amine über die Diazoniumsalze in die desaminierten unsubstituierten Kohlenwasserstoffe umgewandelt werden. Bei der Zersetzung von Diazoniumsalzen in Wasser entstehen die jeweiligen Alkohole. Durch Abspaltung eines Protons aus dem Carbenium-Ion bilden sich in einer Konkurrenzreaktion Alkene:
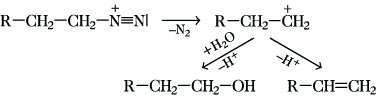
Carbonsäureamide werden unter diesen Bedingungen unter Bildung von Carbonsäuren desaminiert. Arendiazoniumsalze können in analoger Weise in Phenole umgewandelt werden. In Gegenwart von Kupfer(I)-Salzen oder Kupferpulver kann die Diazoniumgruppe auch durch andere Anionen, z. B. Chlorid, Bromid, Cyanid, Rhodanid und Nitrat, im Sinne der Sandmeyer-Reaktion substituiert werden. Bei der Umsetzung von α-Aminosäureestern und α-Aminoketonen mit salpetriger Säure bei tiefen Temperaturen entstehen mesomeriestabilisierte α-Diazoester und α-Diazoketone. Die D. tritt bei diesen Verbindungen erst bei höherer Temperatur bzw. in Gegenwart verd. Säuren ein. Biologisch wichtig ist die oxidative D. von α-Aminosäuren. Dabei bilden sich zunächst unter dem Einfluß von Flavinenzymen α-Iminocarbonsäuren, die hydrolytisch unter Abspaltung von Ammoniak in α-Ketocarbonsäuren übergeführt werden: R-CH(NH2)-COOH → R-C(=NH)-COOH → R-CO-COOH. Bezogen auf die α-Aminosäure findet bei der Transaminierung mit einer α-Ketosäure ebenfalls eine D. statt.
Der bei der D. primärer Amine oder Amide mit salpetriger Säure frei werdende Stickstoff wird nach der Methode von van Slyke zur quantitativen Bestimmung dieser Verbindungen ausgenutzt.
Wenn Sie inhaltliche Anmerkungen zu diesem Artikel haben, können Sie die Redaktion per E-Mail informieren. Wir lesen Ihre Zuschrift, bitten jedoch um Verständnis, dass wir nicht jede beantworten können.