Lexikon der Chemie: Formaldehyd
Formaldehyd, Methanal, H-CHO, der einfachste aliphatische Aldehyd; F. -92 °C, Kp. -21 °C. F. ist ein farbloses, stechend riechendes Gas, das in Wasser und zahlreichen organischen Lösungsmitteln, wie Alkohol und Ether, gut löslich ist.
|
F. geht die meisten typischen Aldehydreaktionen ein und unterscheidet sich nur durch einige spezielle Reaktionen von den übrigen Aldehyden.
F. neigt, wie die meisten aliphatischen Aldehyde, in Gegenwart von Säuren oder Basen zur Polymerisation unter Bildung langkettiger oder cyclischer Produkte, den Polyoxymethylenen. In wäßrigen Lösungen des F., in denen dieser vorwiegend als Hydrat, HO-CH2-OH, vorliegt, bildet sich bereits beim Eindampfen ein weißes, amorphes, lineares Polymerengemisch, das als Paraformaldehyd bezeichnete wird: HO-(CH2-O)n-CH2-OH. In Gegenwart von Säuren bildet sich bei der Destillation einer Formaldehydlösung ein cyclisches Trimerisat, das Trioxymethylen (1,3,5-Trioxan);
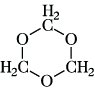
die Bildung von cyclischem Tetraoxymethylen wurde ebenfalls beobachtet. Durch Erhitzen oder durch Hydrolyse kann aus den genannten Polymeren F. zurückgewonnen werden. Da F. kein α-ständiges H-Atom enthält, unterliegt es in Gegenwart von Alkali- oder Erdalkalihydroxiden in höher konz. Lösungen der Cannizzaro-Reaktion unter Disproportionierung zu Methanol und Ameisensäure. Mit Ammoniak reagiert F. unter Bildung von Hexamethylentetramin (Urotropin). Verbindungen mit reaktiven H-Atomen reagieren mit F. unter Bildung von Hydroxymethylverbindungen. So wird z. B. aus F. und Acetaldehyd Tris(hydroxymethyl)acetaldehyd gebildet, der mit überschüssigem F. zum Pentaerythrit weiterreagiert:
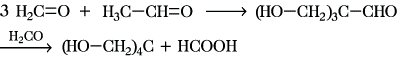
Bei der Synthese von Phenoplasten werden aromatisch gebundene H-Atome in gleicher Weise durch die Hydroxymethylgruppe ersetzt. Analog können die H-Atome im Nitromethan und im Acetylen durch Hydroxymethylgruppen substituiert werden: H-C≡C-H + H2C=O → H-C≡C-CH2-OH (Propargylalkohol).
Bei der Mannich-Reaktion sowie bei der Herstellung von Aminoplasten werden reaktive H-Atome in Aminen bzw. im Harnstoff primär durch Hydroxymethylgruppen ersetzt. Weitere präparativ wichtige Reaktionen des F. sind die Blanc-Reaktion sowie die Grignard-Reaktionen unter Bildung primärer Alkohole.
Gewinnung. F. wird vorzugsweise aus Methanol nach zwei unterschiedlichen Syntheseverfahren hergestellt: 1) durch Dehydrierung von Methanol in Gegenwart eines Silber- oder Kupferkatalysators. Primärschritt der Reaktion ist die Dehydrierung des Methanols: CH3OH → CH2O + H2, ΔRH = +84 kJ/mol. Durch Zugabe von Luft wird der Wasserstoff verbrannt: H2 + 1/2 O2 → H2O, ΔRH = -243 kJ/mol. Es resultiert folgende Gesamtgleichung: CH3OH + 1/2 O2 → CH2O + H2O, ΔRH = -159 kJ/mol. Die Herstellung einer konz. Formalinlösung (etwa 40 M-% F. in Wasser-Methanol-Lösung) erfolgt durch eine nachgeschaltete Destillationsstufe. 2) Bei dem rein oxidativen Verfahren wird Methanol in Gegenwart eines Fe2O3/MoO3-Katalysators zu F. oxidiert. Dazu werden Methanoldämpfe mit hohem Luftüberschuß bei 350 bis 450 °C in einem Röhrenofen über den Katalysator geleitet. Der Methanolumsatz erfolgt dabei vollständig. Nach Abkühlung der Reaktionsgase auf etwa 100 °C wird der F. mit Wasser aus dem Gasstrom herausgewaschen.
Verwendung. F. wird hauptsächlich zu hochpolymeren Werkstoffen, insbesondere zu Phenoplasten, Aminoplasten und Polyoxymethylen, verarbeitet. Weitere wichtige Folgeprodukte des F. sind Polyole, z. B. Pentaerythrit und Trimethylolpropan, die für die Herstellung von Polyester große Bedeutung haben. Durch Ethinylierung von F. und anschließende Hydrierung erhält man Butan-1,4-diol. Außerdem wird F. als Desinfektions- und Konservierungsmittel, als Härtungsmittel für Leim, Casein und Gelatine, als Reduktionsmittel in der Küpenfärberei, zum Desodorieren, als Ausgangsmaterial für synthetische Gerbstoffe, zum Fixieren anatomischer Präparate sowie zur Schimmelpilzbekämpfung eingesetzt. Im Labor wird F. für eine Vielzahl unterschiedlicher synthetischer Aufgaben verwendet.
Wenn Sie inhaltliche Anmerkungen zu diesem Artikel haben, können Sie die Redaktion per E-Mail informieren. Wir lesen Ihre Zuschrift, bitten jedoch um Verständnis, dass wir nicht jede beantworten können.