Lexikon der Chemie: Ionenchromatographie
Ionenchromatographie, Variante der Ionenaustauschchromatographie, bei der der die Detektion störende Elektrolytuntergrund der mobilen Phase durch eine Nachsäulenderivatisierung zurückgedrängt wird. Bei der I. werden spezifische Reagenzien (z. B. Alizarin Rot S) eingesetzt, die nur mit den Probeionen zu hochempfindlich detektierbaren Komplexen reagieren, oder es werden durch die Kombination der Trennsäule mit einer nachgeschalteten zweiten Ionenaustauschersäule (Suppressor) die Eluenten neutralisiert bzw. abgefangen. Beispielsweise kann die sehr häufig für Kationentrennungen verwendete Salzsäure mit Hilfe eines Austauschers in der OH-Form als Suppressor durch Bildung der Cl-Form und Wasser neutralisiert werden. Neuere Methoden setzen semipermeable Ionenaustauschermembranen (Hollow-Fiber) als Suppressor ein. Noch kürzere Reaktionsstrecken und höhere Austauschkapazität bietet das Anlegen eines elektrischen Feldes für den beschleunigten Ionentransport in einer elektrochemischen Suppressorkammer.
Man unterscheidet Kationen- und Anionenchromatographie (Abb. 1a und 1b). Daneben kennt man im Falle der Anionenchromatographie auch eine vereinfachte Form durch Verwendung von 10-3 bis 10-4 molaren Lösungen von Phthalsäure als Eluent im pH-Bereich von 4 bis 6. Aufgrund der geringen elektrischen Leitfähigkeit entfällt die Kombination mit einer Suppressorsäule.
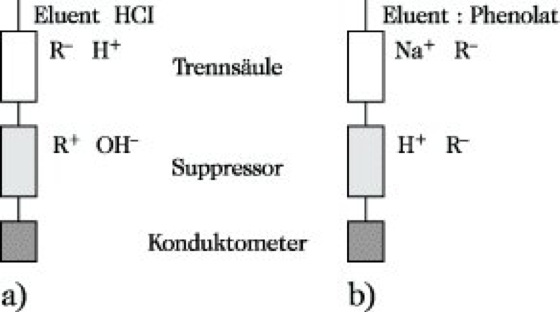
Ionenchromatographie. Abb. 1: (a) Kationenchromatographie, (b) Anionenchromatographie.
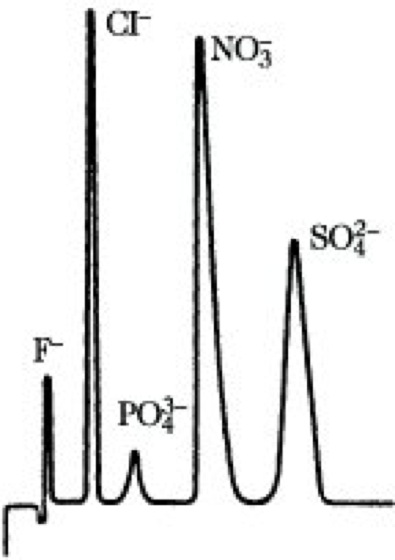
Ionenchromatographie. Abb. 2: Anionenchromatogramm einer Wasserprobe.
Der Nachweis der getrennten Ionen erfolgt durch Leitfähigkeitsmessungen oder mit Hilfe elektrochem. Detektoren. Als Apparaturen verwendet man Geräteanordnungen der Hochleistungsflüssigchromatographie.
Die I. findet Anwendung in der naßchem. Routineanalytik und variiert von Ionenbestimmungen in Trinkwasser über Abwasser bis hin zu organischen Matrizes wie Urin oder Blut (Abb. 2). Dabei sind Ionenkonzentrationen im %-Bereich (Meerwasser) genauso bestimmbar wie im mg/t-Bereich (Kesselspeisewasser).
Wenn Sie inhaltliche Anmerkungen zu diesem Artikel haben, können Sie die Redaktion per E-Mail informieren. Wir lesen Ihre Zuschrift, bitten jedoch um Verständnis, dass wir nicht jede beantworten können.