Lexikon der Chemie: Katalyse
Katalyse, die Erscheinung, daß die Geschwindigkeit einer Reaktion durch den Zusatz eines Stoffes erhöht wird, der selbst nicht in der Stoffbilanz der Reaktion auftritt. Der Stoff, der fest, flüssig (gelöst) oder gasförmig sein kann, wird als Katalysator (in der Technik im Falle von Festkörpern auch als Kontakt) bezeichnet.
I) Allgemeines. Je nachdem, ob der Katalysator in der gleichen oder in einer anderen Phase als die Reaktanten vorliegt, unterscheidet man homogene und heterogene K. (s. u.). Von Photokatalyse und Elektrokatalyse spricht man, wenn der Katalysator photo- bzw. elektrochemisch erzeugt wird. Unter Phasentransferkatalyse versteht man das Prinzip, die in unterschiedlichen Phasen, z. B. Wasser und organischem Lösungsmittel, löslichen Reaktanten durch geeignete Zusätze in die gleiche Phase zu überführen und damit die Reaktion zu ermöglichen. Bei der Biokatalyse wirken Enzyme als Katalysator. Die Erscheinung, daß durch den Zusatz eines Stoffes die Reaktionsgeschwindigkeit erniedrigt wird, bezeichnet man als Inhibierung (mitunter auch als "negative K."). Dieser Effekt kann entweder durch die Blockierung oder Veränderung des Katalysators einer katalysierten Reaktion (Katalysatorvergiftung) oder durch eine Inhibitorwirkung verursacht werden (Inhibitor).
Prinzipiell unterschiedlich wirken Katalysatoren und Initiatoren. Während durch einen Initiator kein neuer Reaktionsweg eröffnet wird, beruht die Wirkung des Katalysators auf der Ausbildung eines neuen Reaktionsmechanismus, der einen rascheren Ablauf der Reaktion ermöglicht und in dem der Katalysator ständig wieder zurückgebildet wird. Das Prinzip der K. läßt sich für eine einfache bimolekulare Reaktion A + B → AB durch die allg. Reaktionsgleichung A + B + K → AB + K beschreiben. Da der Katalysator K nicht in die Stoffbilanz eingeht, verändert er auch nicht die Gleichgewichtslage der Reaktion. Daraus ergibt sich die wichtige Schlußfolgerung: Katalysierbar sind nur thermodynamisch mögliche Reaktionen, deren freie Reaktionsenthalpie ΔRG negativ ist. Um einen neuen Reaktionsweg zu eröffnen, muß der Katalysator z. B. gemäß A + K ![]()
AK, AK + B → AB + K mit einem Reaktanten eine mehr oder weniger stabile Zwischenverbindung bilden, die für den geschwindigkeitsbestimmenden Schritt der Reaktion einen neuen Übergangszustand mit einer kleineren freien Aktivierungsenthalpie ΔGKat (Abb.) liefert (Eyringsche Theorie, Reaktionskinetik). Je größer die Erniedrigung der freien Aktivierungsenthalpie ist, um so höher ist die Geschwindigkeit der katalysierten Reaktion bzw. die Aktivität des Katalysators. Nach der Gibbs-Helmholtz-Gleichung AG = AH – TAS hängt ΔGKat von der Aktivierungsenthalpie ΔHKat und der Aktivierungsentropie ΔSKat ab, d. h. von der Bildungsenergie und der Bildungswahrscheinlichkeit des Übergangszustands mit dem Katalysator im geschwindigkeitsbestimmenden Schritt der Reaktion. Dementsprechend ist für die Funktion des Katalysators die Art seiner Wechselwirkung mit den Reaktanten von entscheidender Bedeutung. Dadurch kann die Reaktivität der Reaktanten erhöht (Aktivierung) und/oder ihre optimale räumliche Zusammenführung begünstigt werden.
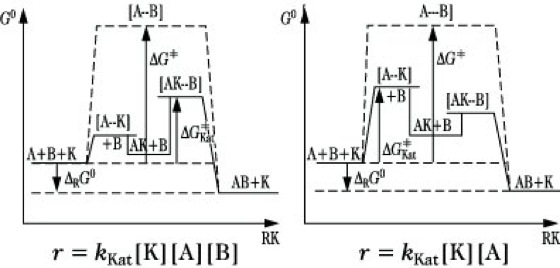
Katalyse. Abb.: Reaktionsdiagramm und Geschwindigkeitsgesetz für eine katalysierte bimolekulare Reaktion A + B →K AB. a) mit einer Arrhenius-Zwischenverbindung AK, b) mit einer Van't-Hoff-Zwischenverbindung AK. ΔRG0 = freie Standardreaktionsenthalpie, ΔG|Kat freie Aktivierungsenthalpie der katalysierten und ΔG=| der unkatalysierten Reaktion. Mit =| werden Übergangszustände bezeichnet, RK bedeutet Reaktionskoordinate.
Kenngrößen eines Katalysators. Die Umsatzzahl gibt die je Zeiteinheit erreichbare Anzahl der Umsätze in mol Reaktionsprodukt je mol Katalysator oder Aktivzentrum an, charakterisiert die Katalysatorleistung und kann auch als Maß der katalytischen Aktivität dienen. Die durch Nebenreaktionen unter den Reaktionsbedingungen stets begrenzte Lebensdauer des Katalysators bestimmt die Katalysatorausbeute oder -produktivität, das ist die insgesamt je mol Katalysator rationell gewinnbare Produktmenge. Die Katalysatorbelastung ist die Reaktantdosiergeschwindigkeit je Katalysatormenge, angegeben in Volumen Reaktant je Katalysatorvolumen und Zeiteinheit. Die Selektivität eines Katalysators äußert sich in der Begünstigung einer Reaktion, wenn zwischen den Reaktanten mehrere möglich sind, und unter Spezifität eines Katalysators versteht man die Eigenschaft, eine bestimmte Reaktion nur für ein Substrat in Abhängigkeit von dessen Struktur zu katalysieren.
Bedeutung und Verwendung. Durch K. können kinetische Reaktionshemmungen, die generell bei einer zu geringen anziehenden Wechselwirkung zwischen den Reaktanten resultieren, umgangen und Reaktionen gezielt in eine bestimmte Richtung gelenkt werden. Etwa 80% der derzeitigen technischen Verfahren in der chem. Industrie beruhen auf katalytischen Reaktionen. Rascherer Ablauf, Einsparung von Prozeßstufen, höhere Ausbeuten am gewünschten Produkt und geringerer Energieaufwand durch mögliche Temperatur- oder Druckerniedrigung sind wesentliche ökonomische Aspekte der K. Vielfach werden bisher nicht oder nur schwer erhältliche Stoffe überhaupt erst in rationeller Weise und in großem Maßstab zugänglich. Wesentlich ist die K. auch für die biochem. Prozesse im lebenden Organismus. Spezielle Anwendungen der K. gibt es in der analytischen Chemie. Die gesetzmäßige Abhängigkeit der Reaktionsgeschwindigkeit katalysierter Reaktionen von der Natur und der Konzentration des Katalysators kann zum qualitativen Stoffnachweis, zur Endpunktanzeige in der Maßanalyse (katalytische Titration) sowie zur quantitativen Stoffbestimmung (Katalymetrie) ausgenutzt werden, wobei im Prinzip eine hohe Empfindlichkeit (Spurenanalyse) erreichbar ist.
II) Homogene K. Im Ablauf homogener katalytischer Reaktionen lassen sich zwei Grenzfälle unterscheiden: a) Die Bildung der Zwischenverbindung AK erfolgt rascher als die Weiterreaktion, die geschwindigkeitsbestimmend ist. Man spricht dann von einer Arrhenius-Zwischenverbindung (Abb. a). Diese ist prinzipiell nachweisbar, und die katalytische Aktivität hängt von der Konzentration und der Reaktivität dieser Zwischenverbindung ab. b) Die Bildung von AK ist geschwindigkeitsbestimmend und erfolgt langsamer als die Weiterreaktion. Hierbei bezeichnet man AK als Van't-Hoff-Zwischenverbindung (Abb. b). Diese ist direkt nicht nachweisbar, und die katalytische Aktivität wird durch ihre Bildungsgeschwindigkeit bestimmt. In jedem Fall ist der Katalysator an der Ausbildung des Übergangszustands im geschwindigkeitsbestimmenden Reaktionsschritt beteiligt und geht konzentrationsmäßig in das Geschwindigkeitsgesetz der Reaktion ein. Da auch ein Reaktionsprodukt katalytisch wirken kann (Autokatalyse), läßt sich ein Katalysator kinetisch als ein zugesetzter oder in der Reaktion gebildeter Stoff definieren, der im Geschwindigkeitsgesetz der Reaktion in einer höheren Potenz auftritt, als es nach der Reaktionsgleichung möglich erscheint. Durch die Messung der Abhängigkeit der Reaktionsgeschwindigkeit von der Katalysatorkonzentration kann eine K. kinetisch bewiesen und ein erster Anhaltspunkt für den Mechanismus der katalytischen Reaktion gewonnen werden.
Ausgehend von der chem. Natur des Katalysators unterscheidet man:
1) Brönstedsche Säure-Base-K. Als Katalysatoren fungieren Protonendonoren oder/und Protonenakzeptoren. Hängt die Reaktionsgeschwindigkeit der katalysierten Reaktion nur von der H3O+- oder OH--Konzentration ab, spricht man von spezieller (spezifischer) Säure- oder Base-K. Bei der allgemeinen Säureoder Base-K. wirken außerdem noch andere im System vorhandene Säuren oder Basen katalytisch. Zahlreiche organisch-chem. Reaktionen, insbesondere Additionen an die C=0- und die C=C-Doppelbindung, die Hydrolyse von Estern, Kondensations- und Polymerisationsreaktionen, Eliminierungen sowie eine ganze Reihe von Umlagerungen (Isomerisierungen), lassen sich durch Protonierung oder Deprotonierung des betreffenden Reaktanten katalysieren. Protonenübertragungen können über Wasserstoffbrückenbindungen sehr rasch erfolgen (1011 mol/l s), und mit der Anlagerung oder Abspaltung eines Protons ist im allg. eine beträchtliche Reaktivitätssteigerung verbunden. Diese resultiert aus der extrem stark polarisierenden Wirkung des Protons. Mit den stärksten Brönsted-Säuren, z. B. der Kombination FSO3H/SbF5 (magische Säure), lassen sich in flüssigem Schwefeldioxid auch gesättigte Kohlenwasserstoffe unter Bildung von hochreaktiven Carbonium-Ionen protonieren. In anderen Fällen reicht bereits die Ausbildung einer Wasserstoffbrückenbindung mit der Katalysatorsäure oder -base für die erforderliche Polarisierung des Substrats aus. Häufig ist die katalytische Wirkung dem pK-Wert der Katalysatorsäure oder -base proportional (Brönstedsche Katalyse -Beziehung). Aus der kombinierten Säure- und Base-Einwirkung (bifunktionelle K.) kann eine stärkere Aktivierung resultieren.
2) Elektrophile und nucleophile K. basieren auf der Aktivierung eines Substrats mit Elektronenpaardonor oder Elektronenpaarakzeptoreigenschaften durch koordinative Wechselwirkung mit einem anderen Akzeptor- bzw. Donormolekül. Typische Beispiele für elektrophile K. sind die Friedel-Crafts-Alkylierungen (Friedel-Crafts-Reaktionen) und die Meerwein-Ponndorf-Verley-Reduktion. Nucleophile K. sind z. B. die Acylierung von Aminen, Alkoholen und Phenolen mit Acetylchlorid durch Pyridin und die durch Cyanid-Ionen katalysierte Benzoinkondensation. Generell eröffnet die elektrophile und nucleophile K. aufgrund der strukturellen Variabilität des Katalysators größere und spezifischere Aktivierungsmöglichkeiten als die Brönstedsche Säure-Base-K.
3) Die Metallkomplexkatalyse umfaßt die katalytischen Möglichkeiten, die auf der chem. Reaktivität von komplexgebundenen Metall-Ionen und -Atomen in Lösung basieren. Metallkomplexe können über unbesetzte Valenzorbitale des Zentralatoms als elektrophile und über besetzte innere D-Orbitale als nucleophile Reagenzien wirken. Außerdem sind vor allem bei Übergangsmetallkomplexen auch Redoxreaktionen relativ leicht möglich. Ähnlich wie durch Protonenaddition lassen sich Lewisbasische Moleküle durch Komplexbildung mit einem Metall-Ion für eine heterolytische Bindungsspaltung oder eine nucleophile Addition aktivieren. Aus diesem Grund sind Metall-Ionen wie Mg2+, Zn2+ und Mn2+ wichtige Aktivatoren in der Biokatalyse. Ein Beispiel für Metallkomplexkatalyse durch koordinative Wechselwirkung mit Metall(II)-Ionen ist die Spaltung der Oxalylessigsäure zu Brenztraubensäure und CO2 in wäßriger Lösung. Die K. von Redoxreaktionen (Redoxkatalyse) kann entweder über eine Redoxreaktion oder eine koordinative Wechselwirkung des Reaktanten mit dem Katalysator erfolgen. Beispiele hierfür sind die katalytische Zersetzung von Alkylhydroperoxiden durch Co(II)- oder Mn(II)-Verbindungen, die für die Autoxidation von Kohlenwasserstoffen wichtig ist, und die durch Mo(VI)Verbindungen katalysierte Epoxidierung von Alkenen durch Alkylhydroperoxide (Halcon-Verfahren). Aber auch Substitutionsreaktionen lassen sich über eine Redoxreaktion mit dem Katalysator beschleunigen. Komplexkatalysatoren ermöglichen über die Art des Zentralatoms, d. h. seine Valenzorbitalcharakteristik und seine Oxidationsstufe, und die Koordinationssphäre, die durch die Donor-Akzeptor-Eigenschaften, die geometrische Struktur, Raumerfüllung und Anordnung sowie die gegenseitige Beeinflussung der Liganden bestimmt wird, eine erhebliche chem. Modifizierung, die zur Katalysatoroptimierung und gegebenenfalls zur katalytischen Reaktionssteuerung genutzt werden kann.
Katalyse. Tab.1: Technisch wichtige Verfahren zur Erzeugung organischer Zwischenprodukte und Hochpolymere aus den einfachen Grundstoffen Aceylen, Ethylen, Propylen, Butadien, Kohlenmonoxid und Wasserstoff durch metallorganische Komplexkatalyse (Ph = C6H5, Ar = Aryl, R = Alkyl, acac = Acetylacetonat)
| |||
| Reppe-Synthesen mit Acetylen | |||
| Vinylierung mit Essigsäure Ethinylierung mit Formaldehyd Carbonylierung mit CO/H2O Cyclooligomerisation | Hg2+ Cu2C2 Ni(CO)4/HBr Ni(CN)2 | Vinylacetat (70%) But-2-in-1,4-diol (90%) Acrylsäure (90%) Cyclooctatetraen (70%) | |
| Funktionalisierungsreaktionen | |||
| Hydrosilylierung von Olefinen Hydrocyanierung von Butadien Ethylenoxidation Carbonylierung von Methanol Oxosynthese mit 1-Olefinen | H2PtCl6 Ni(P(OPh)3)4 O2/PdCl2/CuCl2 Co2(C0)8/HI HCo(C0)4/PR3 | Alkylsilan Adipinsäuredinitril Acetaldehyd (95%) Essigsäure (90%) Aldehyd (80%) oder Alkohol (80%) | |
| C-C-Verknüpfungsreaktionen | |||
| Polymerisation des Ethylens Oligomerisation des Ethylens (Shell-Verfahren) Polymerisation des Propylens Polymerisation des Butadiens Cyclotrimerisation des Butadiens Cyclodimerisation des Butadiens | TiCl4/Al2(C2H5)6 PhNi(PhC(O)CHPPh2)PPh3 TiCl3/MgCl2/Al(C2H5)2Cl Ni(O2CR)2/Al2(C2H5)6/BF3 · O(C2H5)2 TiCl4/Al2Cl3(C2H3)3 Ni(acac)2/Al2(C2H5)6/P(OAr)3 | Polyethylen (97%) 1-Olefine C10... C30 (98%) Isotakt. Polypropylen (95%) 1,4-cis-Polybutadien (96%) Cyclododeca-1,5,9-trien (90%) Cycloocta-1,5-dien (96%) |
4) Metallorganische Komplexkatalyseist die K. organisch-chem. Reaktionen unter Bildung von Verbindungen mit einer Metall-Kohlenstoff-Bindung. 1953 fand K. Ziegler die K. der Ethylenpolymerisation unter Normalbedingungen mit einem metallorganischen Mischkatalysator aus TiCl4 und Al2(C2H5)6 (aluminiumorganische Verbindungen). Wenig später gelang G. Natta mit ähnlichen Katalysatoren die stereoreguläre Polymerisation von Propen und Butadien. Generell bezeichnet man Katalysatoren aus einer Übergangsmetallverbindung und einer Hauptgruppenmetallorganylverbindung als Ziegler-Natta-Katalysatoren. Die eigentlichen Katalysatoren in diesen Systemen sind besonders reaktive σ- oder π-Organoübergangsmetallkomplexe, die durch Reaktion mit der Organylkomponente gegebenenfalls unter Einbeziehung der jeweiligen Reaktanten entstehen. Als metallorganische Komponente (Cokatalysator) haben sich die in Kohlenwasserstoffen gut löslichen Aluminiumorganyle besonders bewährt, die, im Überschuß angewendet, die gebildeten katalytisch aktiven Komplexe zusätzlich gegen eine Zerstörung (Vergiftung) durch O2- und H2O-Spuren schützen können.
Die auf der metallorganischen Komplexkatalyse basierenden technischen Synthesen bestimmen wesentlich das Profil der modernen Petrol- und Hochpolymerenchemie (Tab. 1). Metallorganische Komplexkatalysatoren zeichnen sich vielfach durch hohe Aktivität, Selektivität und Spezifität aus.
Bei der Ethylenpolymerisation ergeben die durch Trägerfixierung und Behandlung mit Lewis-Basen verbesserten Ziegler-Natta-Katalysatoren der 2. Generation über 10000 kg Polyethylen/mol Titan, so daß die Verfahrensstufe der Katalysatorentfernung in der Aufarbeitung entfallen kann. Die Anwendung wesentlich aktiverer Rhodiumkomplexkatalysatoren ermöglicht bei der Essigsäuresynthese aus Methanol und Kohlenmonoxid und der Oxosynthese von Olefinen eine Steigerung der Selektivität und den Übergang vom Hochdruck- zum energetisch erheblich günstigeren Mitteldruckverfahren. Eine hohe Katalysatorspezifität zeigt z. B. die Katalyse der Hydrierung olefinischer Doppelbindungen mit dem Wilkinson-Komplex Rh(PPh3)3Cl (Ph = Phenylrest), wobei andere ungesättigte Gruppen, wie -CHO, -CN, -NO2 -CO2H und -C6H5 nicht angegriffen werden. Durch die Einführung chiraler Phosphinliganden gelang es, α-Acetylaminozimtsäuren mit einer Enantioselektivität von bis zu 99% asymmetrisch zu hydrieren und auf diese Weise eine direkte Synthese des Arzneimittels L-Dopa (3,4-Dihydroxyphenylalanin) technisch zu realisieren. Für eine ganze Reihe metallorganischer Komplexkatalysatoren ist der Wirkungsmechanismus in den Grundzügen aufgeklärt.
Die durch kinetische, spektroskopische und präparative Untersuchungen erreichten Einblicke in die Wirkungsweise metallorganischer Komplexkatalysatoren sind auch für die Entwicklung der chem. Theorie der K. von wesentlicher Bedeutung. Generell läßt sich der Mechanismus homogen katalysierter Reaktionen leichter aufklären und liefert in vielen Fällen eine Modellvorstellung für den Ablauf vergleichbarer heterogen katalysierter Reaktionen. Ein bedeutender verfahrenstechnischer Nachteil metallorganischer Komplexkatalysatoren ist oft ihre nicht sehr hohe thermische und chem. Beständigkeit und ihre schwierige Abtrennbarkeit. Man versucht dieses Problem durch Trägerfixierung, d. h. durch chem. Bindung des katalytisch aktiven Komplexes auf einem organischen oder anorganischen Feststoff (Heterogenisierung), zu lösen.
III) Heterogene K. (Kontaktkatalyse, Oberflächenkatalyse). Der Katalysator liegt in der Regel als amorpher oder kristalliner Festkörper vor, an dessen Oberfläche die katalysierte Umsetzung der gasförmigen oder flüssigen Reaktanten erfolgt.
Der Ablauf einer heterogen katalysierten Reaktion schließt die folgenden Schritte ein: Äußere Diffusion der Reaktanten zur Oberfläche des Katalysatorkorns, innere Diffusion oder Porendiffusion, d. h. Diffusion zur inneren Oberfläche in den Poren, Adsorption, Oberflächenreaktion, Desorption der Reaktionsprodukte, Rückdiffusion durch die Poren zum Rand des Katalysatorkornes und Diffusion in die umgebende Gasphase. Neben dem Massetransport erfolgt ein Wärmeübergang zum Ausgleich der durch die Reaktionswärme verursachten Temperaturgradienten innerhalb des Katalysatorkornes und zwischen Katalysator und Gasphase. Ausschlaggebend für die Reaktionsbeschleunigung in der heterogen katalysierten Reaktion ist die erhöhte Reaktivität des adsorbierten Reaktanten, die – im Vergleich zur nichtkatalysierten Reaktion – zu einer Erniedrigung des Wertes der Aktivierungsenergie in der Arrhenius-Beziehung führt. Grundsätzlich besteht die Möglichkeit, daß die Aktivierungsenergie der Oberflächenreaktion kleiner ist als die der Adsorption oder Desorption. In diesem Fall werden Adsorption bzw. Desorption geschwindigkeitsbestimmend für den katalytischen Reaktionsablauf.
Wesentlich für eine hohe Aktivität fester Katalysatoren ist eine große, gut zugängliche Oberfläche sowie eine der Reaktion angepaßte Porosität und Textur (Form, Größe und Volumen der Poren). Die Oberflächengröße wird üblicherweise durch Auswertung der Tieftemperaturadsorptionsisotherme von Stickstoff mit der BET-Gleichung (Adsorption) bestimmt.
Nicht immer sind Katalysatoren mit hoher innerer Oberflächengröße vorteilhaft. So werden für Selektivoxidationen wenig poröse, kompakte Katalysatoren eingesetzt, da an stark porösen Katalysatoren Wärme und Stofftransport nicht schnell genug erfolgen und unerwünschte Folgereaktionen (Totaloxidation!) dann verstärkt ablaufen.
Die Wechselwirkung zwischen Katalysator und Reaktant kann entsprechend der Natur der chem. Bindung sehr vielfältig sein. Ausgehend davon lassen sich die festen Katalysatoren nach Stoffklassen untergliedern.
Stoffliche Einteilung fester Katalysatoren. 1) Metall- und Halbleiterkatalysatoren. Die zu Einelektronenübergängen befähigten Halbleiter (Halbleiteroxide und -sulfide) und Metalle können als Elektronendonatoren oder -akzeptoren wirken und Redoxreaktionen katalysieren: In Hydrierungen oder Dehydrierungen sind Metalle, z. B. Platin, Palladium, Nickel, Cobalt und Eisen, sowie Oxide und Sulfide von Zink, Nickel, Eisen, Chrom, Molybdän, Wolfram und Vanadium katalytisch aktiv, wobei in der Praxis für die bei niedrigen Reaktionstemperaturen ablaufenden Hydrierreaktionen im allg. die aktiveren, aber teureren Metalle bevorzugt eingesetzt werden; für Oxidationen werden häufig Vanadium(V)-oxid, Silber, Kupfer und Platin verwendet.
Bevorzugter Ort der Reaktionen sind aktive Zentren an der Oberfläche, z. B. koordinativ nicht abgesättigte Atome oder Ionen, insbesondere an Störstellen, Kristallkanten und -ecken oder auch ganze Atomgruppierungen (Ensemble, Multiplett) an der Festkörperoberfläche. Energiereiche Störstellen werden in Legierungsskelettkatalysatoren, den RaneyKatalysatoren, in hoher Konzentration durch Auslaugen einer Legierungskomponente, z. B. Aluminium aus einer Aluminium-Nickel-Legierung, erzeugt.
2) Säure-Base-Katalysatoren.Festkörper mit aciden OH-Oberflächengruppen (Brönsted-Zentren) eignen sich als Katalysatoren für Reaktionen, die nach einem Säure-Base-Mechanismus verlaufen, wie Alkylierung, Isomerisierung, Oligomerisierung, Hydratisierung, Dehydratisierung sowie das Cracken von Kohlenwasserstoffen. Die hohe thermische Beständigkeit einiger Festkörpersäuren ermöglicht wesentlich höhere Reaktionstemperaturen als dies bei homogenen Säuresystemen im allg. möglich ist. Zu dieser Gruppe von Katalysatoren gehören γ-Al2O3, Al2O3/SiO2, MgO/SiO2 sowie modifizierte Zeolithe. Zeolithe vom Typ Y, in die Kationen der Seltenerdmetalle eingetauscht sind, werden großtechnisch zum katalytischen Cracken eingesetzt. In Reaktionen an Zeolithen können Molekularsiebeffekte auftreten: Nur solche Moleküle werden adsorbiert und umgesetzt, bzw. können nach erfolgter Reaktion wieder in die Gasphase diffundieren, die aufgrund ihres hinreichend kleinen Moleküldurchmessers die Porenöffnungen passieren können (Reaktantselektivität, Produktselektivität). Auch die Ausbildung sperriger Übergangszustände kann durch die Porengeometrie eingeschränkt sein (Transition-State-Selektivität). Ein Beispiel für Reaktantselektivität ist das formselektive Spalten unverzweigter Alkane an engporigen Zeolithen in Anwesenheit verzweigter und cyclischer Kohlenwasserstoffe.
Die unterschiedliche katalytische Wirkung verschiedener Festkörper kann in bifunktionellen (polyfunktionellen) Katalysatoren gekoppelt werden; so laufen an dem zum Reformieren von Schwerbenzin eingesetzten Pt/γ-Al2O3-Katalysator gleichzeitig säurekatalysierte Isomerisierungsreaktionen (z. B. Methylcyclopentan zu Cyclohexan) am γ- Al2O3 und Dehydrierreaktionen (Cyclohexan zu Benzol) am Platin ab.
3) Salzartige und komplexanaloge Katalysatoren.Salzartige Katalysatoren benutzt man zur Addition und Eliminierung von HX (X = Halogen, Acetat), wobei das Anion der Katalysatorsubstanz der einzuführenden Gruppe entspricht, z. B. in der Hydrochlorierung von Acetylen an HgCl2/Aktivkohle, der Umsetzung von Essigsäure mit Acetylen an Zn(CH3COO)2/Aktivkohle, der Dehydrochlorierung von Tetrachlorethan an BaCl2 und der Reppe-Synthese (Acetylenchemie) mit CuC2 als Katalysator. Diese sowie einige weitere heterogen katalysierte Reaktionen, (Olefindisproportionierung an MoO3 oder WO3, Mitteldruckpolymerisation von Ethen an Cr2O3, oxidative Hydroxylierung von Aromaten mit H2O2 an Ti-Silicalit) ähneln in ihrem Ablauf analogen homogen komplexkatalysierten Reaktionen.
Aufbau, Eigenschaften und Anwendung technischer Feststoffkatalysatoren. Technisch eingesetzte heterogene Katalysatoren sind in der Regel zusammengesetzte Misch- oder Mehrstoffkatalysatoren. Eine Übersicht über technisch wichtige heterogen katalysierte Reaktionen gibt Tab. 2. Die Wirksamkeit (Aktivität; Selektivität, Lebensdauer) mancher Katalysatoren kann durch Zusatz geringer Mengen weiterer Stoffe, den Promotoren (Aktivatoren), noch erhöht werden. Ein Promotor, der die Tendenz der aktiven Phase zum Sintern und damit zur Verringerung der Oberflächengröße unterdrückt, wird als Texturpromotor (struktureller Verstärker) bezeichnet. Texturpromotoren sind z. B. Al2O3 in dem doppelt promotierten Eisenkatalysator für die Ammoniaksynthese und Rhenium im Pt, Re/Al2O3-Reformierkatalysator. In Bimetall- und Multimetallkatalysatoren (Legierungskatalysatoren) können beide möglichen Funktionen eines Promotors – Aktivator, Texturpromotor – durch zusätzliche Metallkomponenten ausgeübt werden.
In Trägerkatalysatoren ist die wirksame Komponente auf einem oberflächenreichen Träger (γ-Al2O3, Silicagel, Silicate, Bimsstein, Aktivkohle) aufgebracht. Im einfachsten Fall erhält man solche Katalysatoren durch Auftränken löslicher Verbindungen der aktiven Substanzen und durch anschließendes oxidatives, reduktives und/oder thermisches Aktivieren. Der Träger gewährleistet neben einer gleichmäßigen Verteilung eine hohe Dispersität der Aktivkomponente und verleiht dem Katalysator die notwendige Festigkeit sowie das für den An- und Abtransport der Reaktanten und Reaktionsprodukte zur Aktivkomponente erforderliche Porensystem. Darüber hinaus kann der Träger auch durch eine elektronische Wechselwirkung mit der Aktivkomponente deren katalytische Eigenschaften beeinflussen; auch eine Beeinflussung der kristallographischen Orientierung der Metallkristallite ist möglich. Im Extremfall – in bifunktionellen Katalysatoren – greift der Träger selbst aktiv in die Reaktion ein.
Die Form des technischen Feststoffkatalysators wird dem Verwendungszweck angepaßt. Durch die Formgebung werden neben Druckabfall und Strömungsbedingungen im Reaktor auch die Schüttdichte und die mechanische Festigkeit (Druckfestigkeit, Abriebfestigkeit) des Katalysators beeinflußt. Die wichtigsten Typen der oftmals unter Zusatz spezieller Bindemittel erhaltenen Katalysatorformlinge sind Granulate, Tabletten, Strangpreßlinge und kugelförmige (sphäroidale) Katalysatoren. Für katalytische Wirbelschichtverfahren, wie die Ammoxidation von Propen zu Acrylnitril an Bi2O3/MoO3/P2O5 und das Cracken von Gasöl an zeolithischen Katalysatoren im FCC-Prozeß, werden mikrospäroidale Katalysatoren durch Sprühtrocknen hergestellt.
Für Autokatalysatoren werden hauptsächlich metallische oder keramische Monolithe (Wabenkörper) als Träger eingesetzt, wobei sich Cordierit, ein Magnesium-Alumosilicat, als Material für keramische Monolithträger bewährt hat. Der Träger wird mit einer Zwischenschicht (wash coat) aus γ-Al2O3 belegt, die eine hohe Dispersität und gute Haftung der Edelmetallkomponente (Pt, Rh, Pd; 1-2 g pro Auto) gewährleistet. Zusätzlich eingeführte Oxide der Seltenen Erden, i. allg. Ce2O3/CeO2, wirken als Aktivatoren und Texturpromotoren. Durch den Dreiwegekatalysator werden in einem engen Bereich der Abgaszusammensetzung ("λ-Fenster") alle Schadstoffkomponenten gleichzeitig durch Totaloxidation (CO, CmHn) bzw. durch Reduktion (NOx zu Stickstoff) abgebaut.
Katalyse. Tab. 2: Heterogen katalysierte industrielle Verfahren.
| ||
| Ammoniaksynthese (Haber-Bosch-Verfahren) | Fe/Al2O3/K2O | |
| Oxidation von Schwefeldioxid zu Schwefelsäure (Kontaktverfahren) | V2O5/SiO2 | |
| Oxidation von Ammoniak zu Stickoxiden zur Herstellung von Salpetersäure | Pt/Rh | |
| Fischer-Tropsch-Synthese | Fe, Co/ThO2/MgO | |
| Synthese von Methanol Hochdruckverfahren Niederdruckverfahren | ZnO/Cr203 CuO/Cr2O3 | |
| Konvertierung von Kohlenmonoxid Hochtemperaturkonvertierung Tieftemperaturkonvertierung | Fe2O3/Cr2O3 ZnO/CuO/Cr2O3 | |
| Dampfreformieren von Kohlenwasserstoffen | Ni/CaCO3 | |
| Katalytisches Cracken von Kohlenwasserstoffen | Al2O3/SiO2 (Zeolithe) | |
| Hydrospalten von Kohlenwasserstoffen | Ni/Pd/Al2O3/SiO2 (Zeolithe) | |
| Reformieren von Schwerbenzin | Pt/γ-Al2O3 | |
| Isomerisierung der C8-Aromaten | Pt/Al2O3/SiO2 (Zeolith) | |
| Hydroraffination | NiS/WS2/Al2O3 oder CoS/MoS2/Al2O3 | |
| Selektivhydrierung von Phenol zu Cyclohexanon | Pd/Al2O3 | |
| Dehydrierung von Ethylbenzol zu Styrol | Fe3O4/Cr2O3/K2O | |
| Oxidation von Ethylen zu Ethylenoxid | Ag/α-Al2O3 | |
| Oxidation von Benzol zu Maleinsäureanhydrid sowie von o-Xylol zu Phthalsäureanhydrid | V2O5/SiO2 | |
| Abgasnachverbrennung | Pt, Rh, Pd auf Al2O3 | |
| Addition von Methanol an Isobuten zu tert.-Butylmethylether | Saure Ionenaustauscherharze | |
| Olefin-Oligomerisierung zu Benzin bzw. Kerosin | Zeolithe |
Desaktivierung, Regenerieren, Reaktivieren. Mit zunehmender Betriebsdauer nimmt meist die Wirksamkeit der Katalysatoren ab. Ursache für diese Desaktivierung sind vor allem Vergiftung, Alterung und Verkokung. Als Katalysatorgifte (Kontaktgifte) wirken bei Metallkatalysatoren häufig schon Spuren von Schwefel, Phosphor, Arsen aber auch Kohlenmonoxid, Halogenverbindungen und Wasser. Die Vergiftung kann irreversibel oder reversibel sein. Durch selektive Vergiftung können unerwünschte Nebenreaktionen unterdrückt werden, z. B. wird in der Selektivhydrierung durch Zusatz von Kohlenmonoxid die Hydrierung von Olefinen stärker als die der Acetylene und Diene zurückgedrängt. Auch eine Selbstvergiftung des Katalysators durch eines der Reaktionsprodukte kann auftreten. Die Alterung fester Katalysatoren ist mit Änderungen in der Struktur und/oder Textur verbunden und kann hervorgerufen werden durch Sintern, Rekristallisation (Kristallwachstum, Sammelkristallisation der Aktivkomponente in Trägerkatalysatoren, Ausheilung von Gitterdefekten) und durch chem. Umwandlung der Aktivkomponente (Änderung der Oxidationsstufe, Verbindungsbildung durch Festkörperreaktion). Unter Verkokung versteht man die Ablagerung hochkondensierter Folgeprodukte ("Koks") in organischen Reaktionen auf dem Katalysator. Beim Regenerieren wird der Koks durch Abbrennen entfernt.
Die vorteilhafterweise in situ durchgeführte Wiederbelebung eines desaktivierten Katalysators wird als Reaktivieren bezeichnet und kann neben dem Regenerieren weitere Maßnahmen umfassen, wie die Redispergierung der Aktivkomponente Platin in Reformierkatalysatoren.
Wenn Sie inhaltliche Anmerkungen zu diesem Artikel haben, können Sie die Redaktion per E-Mail informieren. Wir lesen Ihre Zuschrift, bitten jedoch um Verständnis, dass wir nicht jede beantworten können.