Lexikon der Chemie: Koordinationschemie
Koordinationschemie, Komplexchemie, Chemie der Komplexverbindungen. Komplexe sind Verbindungen höherer Ordnung, in denen ein neutrales oder geladenes Zentralatom von Liganden (geladene oder ungeladene, ein- oder mehratomige, meist für sich bereits existenzfähige Gruppen) umgeben ist; die Anzahl der an das Zentralatom gebundenen Liganden wird als Koordinationszahl (Abk. Kz, in der Regel 2 bis 9; bei Lanthanoiden und Actinoiden auch 10 bis 12) bzw. Zähligkeit des Zentralatoms bezeichnet. Für.jede Koordinationszahl werden ein oder mehrere charakteristische Koordinationspolyeder beobachtet, wobei ein Zusammenhang zwischen Typ, Elektronenbesetzung des Zentralatoms, den sterischen und elektronischen Ansprüchen der Liganden und der ausgebildeten räumlichen Ligandenanordnung besteht. Koordinationszahl und Koordinationsgeometrie bilden eine wichtige Klassifikationsmöglichkeit der Komplexverbindungen, weitere Ordnungsprinzipien der K. sind durch Ligandentypen, therrnodynamische und kinetische Stabilitäten bzw. Reaktivitäten der Komplexe, ihre magnetischen und optischen Eigenschaften sowie durch die vorherrschenden Bindungsverhältnisse gegeben.
Koordinationszahlen und -geometrien. In Abb. 1 sind mögliche ideale Koordinationspolyeder von Komplexen des allgemeinen Typs MLn (n = 2-12) angegeben.

Koordinationschemie. Abb. 1: Koordinationspolyeder von Komplexen der Koordinationszahlen drei bis zwölf. Gestrichelte Linien: Polyeder-Kanten, ausgezogene Linien: Metall-Ligand-Bindungen; aus Gründen der Übersichtlichkeit werden Polyeder-Kanten und Metall-Ligand-Bindungen nicht immer vollständig wiedergegeben.
Die realen Komplexgeometrien können davon, bedingt durch Einflüsse nichtbindender Valenzelektronen des Zentralmetalls sowie durch sterische Erfordernisse bei der Koordination unterschiedlicher oder mehrzähniger Liganden, mehr oder weniger deutlich abweichen. Komplexe der Kz 2 sind linear gemäß L-M-L; Komplexe der Kz 3 sind meist trigonal-planar (a) strukturiert. Beide sind relativ selten und werden vor allem mit d10-Systemen, wie Kupfer(I), Silber(I), Gold(I) und Quecksilber(II) sowie, bei Koordination sperriger Liganden, auch Palladium(0), Platin(0), Zink(II) und Cadmium(II) gebildet. Beispiele: [CuCl2]-, [Ag(NH3)2]+, [Au(CN)2]-, HgCl2, [Pt{P(c-C6H11)3}2] bzw. [Cu{SP(C6H5)3}3]+, [HgI3]-, [Pd{P(C6H5)3}3]. Komplexe der Kz 4 sind recht weit verbreitet und treten in den beiden möglichen Strukturtypen quadratisch-planar (b) und tetraedrisch (c) auf. Quadratisch-planare Komplexe sind für d8-Ionen, wie Palladium(II), Platin(II), Gold(III), Iridium(I) und Rhodium(I), typisch. Beispiele: [PdCl4]2-, [PtCl2(NH3)2], [Au2Cl6], [IrCl(CO){P(C6H5)3}2], [RhCl(CO)2]2. Sie werden auch für Nickel(II) sowie bei d7- und d9- Systemen, wie Cobalt(II) und Kupfer(II), beobachtet. Beispiele: [Ni(CN)4]2-, [Co(CN)4]2-, (NH4)2[CuCl4], [Cu(NH3)4]2+. Jedoch weisen Nickel(II) und Kupfer(II) vergleichbare Tendenz zur Ausbildung quadratisch-planarer oder tetraedrischer Strukturen auf. So sind die Komplex-Anionen [NiX4]2- (X- = Cl-, Br-, I-) und [CuBr4]2- tetraedrisch gebaut, bei Gemischtligandkomplexen [NiX2(PR3)2] werden sowohl tetraedrische als auch quadratisch-planare Strukturen gefunden. Insgesamt sind tetraedrische Komplexe nach denen der Kz 6 am häufigsten anzutreffen. Diese Koordinationsgeometrie wird besonders durch große und/oder hochgeladene Liganden. wie Cl-, Br-, I-, O2- und S2- begünstigt und tritt hauptsächlich bei Metallzentren mit d0-, d5-, d7- und d10-Konfiguration auf. Beispiele sind etwa die Halogeno- und Cyanokomplexe TiCl4. [MnCl4]2-, [FeCl4]-, [CoBr4]2- sowie, besonders typisch, Oxo- und Thiokomplexe, wie [VO4]3-, [MO4]2- (M = Cr, Mo, W), [MnO4]n- (n = 1-3), [FeO4]2-, [VS4]3-, [ReS4]- und [HgS4]6-. Für die weiter als zunächst angenommen verbreitete Kz 5 sind trigonal-bipyramidale (d), z. B. [Fe(CO)5], [HgCl5]3- und quadratisch-pyramidale Komplexe (e), z. B. [MnCl5]2-, [Co(CN)5]3-, erhalten worden. Bei [Ni(CN)5]3- wird, in Abhängigkeit vom Gegenkation, sowohl quadratisch-pyramidaler als auch trigonal-bipyramidaler Bau gefunden. Komplexe der Kz 5 sind durch nicht-starre, fluktuierende Molekülgerüste charakterisiert, beide Koordinationspolyeder sind leicht ineinander überführbar (Berry-Pseudorotation), Zwischenformen sind möglich. Die sehr häufige Kz 6 ist nahezu ausschließlich mit einer regulär-oktaedrischen (f) oder tetragonal, trigonal bzw. rhombisch verzerrt-oktaedrischen Ligandenanordnung verbunden. Tetragonale Verzerrungen der oktaedrischen Ligandenanordnung in Richtung einer gestreckten oder gestauchten quadratischen Bipyramide lassen sich bei einzelnen dn-Konfigurationen (high spind4, low spin d7 und insbesondere d9) des Übergangsmetallzentrums als Auswirkung des Jahn-Teller-Theorems erwarten und wurden auch bei high-spin-Komplexen der d4-Ionen Chrom(II) und Mangan(III) und vor allem des d9-Systems Kupfer(II) durch Kristallstrukturanalysen nachgewiesen. Komplexe mit einer trigonal-prismatischen Ligandenanordnung (g) sind sehr selten, z. B. MoS2, [Re{S2C2(C6H5)2}3], [Zr(CH3)6]2-. Komplexe der 3d-Metalle sind meist durch die genannten Kz 2 bis 6 charakterisiert, bei Übergangsmetallen der 4d- und 5d- sowie der 4f- und 5f-Reihen treten vielfach Kz > 6 auf. Ähnlich den Komplexen der Kz 5 sind Koordinationsverbindungen der Kz 7 nicht starr: die möglichen Polyeder, die pentagonale Bipyramide (h), z. B. [ZrF7]3-, [V(CN)7]4-, [UF7]3-, das überkappte Oktaeder (i), z. B. [MoF7]-, [NbOF6]3-, und das überkappte trigonale Prisma (j), z. B. [TaF7]2-, lassen sich leicht ineinander überführen. Unter den wichtigsten Polyedern von Komplexen der Kz 8, dem Würfel (k), dem quadratischen Antiprisma (l) und dem Dodekaeder (m), wird der Würfel an diskreten Komplexen höchst selten beobachtet, z. B. [UF8]3- und die beiden letztgenannten Koordinationspolyeder sind relativ leicht ineinander überführbar, wie dies z. B. an Oktacyanometallaten [M(CN)8]n- (M = Mo, W, n = 3, 4) gezeigt werden konnte. In Komplexen der Koordinationszahl 9 herrscht die dreifach-überkappte trigonal-prismatische Ligandenanordnung (n), z. B. [ReH9]2-, [M(H2O)9]3+ (M z. B. Y, Pr, Sm, Yb) vor. In Komplexen der Lanthanoide und Actinoide mit mehrzähnigen Liganden, wie NO3-, CO32- oder BH4-, treten Kz von 10 bis 12 auf. Aus den bei diesen Kz möglichen räumlichen Anordnungen werden hauptsächlich zweifach-überkappt quadratisch-antiprismatische (o) Strukturen, z. B. [Ce(NO3)5]2-, [Th(CO3)5]6-, sowie oktadekaedrische (p), z.B. [La(NO3)3(H2O)5], und ikosaedrische (q) Strukturen, z. B. [Ce(NO3)6]3- und [Zr(BH4)4], gefunden.
Liganden. Komplexliganden lassen sich nach der Art der zur Bindung an das Metallzentrum verwendeten Orbitale verschiedenen Klassen zuordnen. σ-Donorliganden, wie Ammoniak, Amine, Ethylendiamin u. a., koordinieren über freie Elektronenpaare unter Ausbildung von ausschließlichen L→M-σ-Donorbindungen, wobei das Atom, an dem das freie Elektronenpaar lokalisiert ist, als Donoratom oder Ligatoratom bezeichnet wird. Liganden, deren Donoratome mehr als ein freies Elektronenpaar besitzen, wie X- (X = Halogen), RO-, O2-, S2-, R2N-, RN2-, N3- können mit Übergangsmetallen zusätzlich zur σ-Donorbindung durch Übertragung von Elektronen aus besetzten Ligandenorbitalen in leere D-Orbitale des Metalls π-Hinbindungen ausbilden, wodurch die Metall-Ligand-Bindung Mehrfachbindungscharakter gemäß M←←L erhält (σ-Donor/π-Donor-Liganden). Weiterhin können Liganden Metall-Ligand-Mehrfachbindungen entsprechend M→←>L dadurch ausbilden, daß zusätzlich zur σ-Donorbindung Elektronen aus besetzten D-Orbitalen des Metalls in freie, antibindende π*- (oder σ*-) Orbitale des Liganden durch eine π-Rückbindung ("π-back donation") übertragen werden (σ-Donor/π-Akzeptor-Liganden). Zu dieser wichtigen Klasse zählen Moleküle oder Molekül-Ionen mit Dreifachbindungen, wie die isoelektronischen Spezies Kohlenmonoxid CO, Distickstoff N2, Cyanid CN- und das Nitrosyl-Kation NO+ sowie Verbindungen mit Donoratomen aus der V. Hauptgruppe, wie Phosphane PR3 und Arsane AsR3, u. a.. Eine große Gruppe von organischen Liganden, wie die ungesättigten (Alkene, Di- und Oligoolefine, Alkine) und aromatischen Kohlenwasserstoffe, bildet mit Übergangsmetallen π-Komplexe, in denen diese Liganden sowohl für die Ausbildung von L→M-σ- (und evtl. π-) Donorbindungen als auch für die zusätzlich stets vorhandenen M→L-π-Akzeptorbindungen Orbitale verwenden, die bezüglich der intra-Ligand-Bindung π-Symmetrie aufweisen. Kohlenmonoxid und diese Liganden spielen eine große Rolle in der Organochemie der Übergangsmetalle (elementorganische Verbindungen) sowie in der homogenen Katalyse (Katalyse).
Koordiniert ein Ligand über ein Donoratom, wird er als einzähnig bezeichnet, verfügt er über mehrere polentielle Ligatoratome, als mehrzähnig (zwei-, drei-, vier-, fünf-, sechszähnig), wobei die Zähnigkeit die Anzahl der am selben Zentralatom haftenden σ-Elektronenpaar-Donorgruppen angibt. Bei Koordination mehrzähniger Liganden mit mehr als einer solchen Donorgruppe an ein Zentralatom resultieren ringförmige Verbindungen (Metallacyclen), die Chelatkomplexe (oder Metallchelate), wobei besonders häufig Fünf- und Sechsringsysteme ausgebildet werden. Ein typischer zweizähniger Chelatbildner ist Ethylendiamin (Ethan-1,2-diamin) NH2(CH2)2NH2, während Diethylentriamin (N-(2-aminoethyl)-1,2-ethandiamin) HN(CH2CH2NH2)2, der "Tripodligand (Dreifußligand)" Tris(2-aminoethyl)amin N(CH2CH2NH2)3 und das in der Komplexometrie genutzte Ethylendiamintetraacetat [(OOCCH2)2N(CH2)2N(CH2COO)2]4- Beispiele für mehrere Chelatringe ausbildende, über flexible Molekülgerüste verfügende drei-, vier- und sechszähnige Liganden bilden. Neutrale Chelatkomplexe, bei denen die anionischen Chelatliganden die Ladung des Zentralatoms gerade kompensieren, werden auch als Innerkomplexe bezeichnet. Mehrzähnige cyclische Liganden, wie sie etwa in den Phthalocyaninen, ferner in den für die Biosphäre außerordentlich bedeutungsvollen Porphyrinen wie Häm oder Chlorophyll vorliegen, werden als makrocyclische Liganden bezeichnet. Vielzähnige Liganden liegen in makrocyclischen Polyethern (Kronenether) und in bicyclischen Aminopolyethern (Kryptanden) vor.
Einatomige Liganden, die wie die Halogenide |X--|- über mehrere freie Elektronenpaare verfügen, mehratomige Liganden, deren Donoratom über mehrere freie Elektronenpaare verfügt, z. B. Hydroxid -|O---H, ferner mehratomige Liganden mit mehreren potentiellen Donoratomen, z. B. Cyanid CN-, Thiocyanat SCN-, Azid N3- oder Nitrit NO2-, können als Brückenliganden mehrere Metallatome verbinden.
Unterschiedliche Donoratome aufweisende, einzähnige Liganden, z. B. Nitrit NO2- oder Thiocyanat SCN-, werden als ambidente (ambidentate) Liganden, Chelatliganden, die über mehr als einen Satz von Donoratomen binden können, als flexidentate Liganden bezeichnet. Zur Bezeichnung der Bindungsweise dieser Liganden in Komplexen werden im Anschluß an den Namen die (kursiven) Symbole der an das Zentralatom gebundenen Donoratome angegeben, z. B. Thiocyanato-S, Dithiooxalato-O,O. Für die bei der Entwicklung der Komplexchemie wichtigen Liganden NO2- und SCN- werden die historischen Bezeichnungsweisen Nitro- bzw. Nitritokomplexe (M-NO2 bzw. M-ONO), Isothiocyanato-(M-NCS) und Thiocyanato-(M-SCN)Komplexe verwendet.
Komplexisomerien. Bei Komplexverbindungen können vielfältige Isomerieerscheinungen auftreten, die sich der Konstitutionsisomerie (Isomerie) oder der Stereoisomerie zuordnen lassen. Konstitutionsisomerie ergibt sich bei Komplexen meist dadurch, daß einzelne Liganden gegenseitig ihre Pätze vertauschen. So beschreibt die Ionisationsisomerie Komplexpaare, bei denen ein Anion einmal ionogen und einmal als Ligand gebunden ist: [CoBr(NH3)5]SO4 bzw. [Co(SO4)(NH3)5]Br. Hiervon einen Spezialfall stellt die Hydratisomerie dar, die darauf zurückgeht, daß H2O-Moleküle entweder als Aqualiganden oder als Kristallwasser gebunden sind, z. B. in den Chrom(III)-Komplexen [CrCl2(H2O)4]Cl·2 H2O (dunkelgrün), [CrCl(H2O)5]Cl2 ·H2O (hellgrün) und [Cr(H2O)6]Cl3 (violett). Weiterhin tritt in Salzen. die aus zwei komplexen Ionen bestehen Koordinationsisomerie dadurch auf, daß Liganden ihre Plätze zwischen Kation und Anion tauschen. z. B in den Komplexen [Cu(NH3)4][PtCl4] und [Pt(NH3)4][CuCl4]. Einen besonders interessanten Fall von Konstitutionsisomerie stellt die Bindungsisomerie (früher Salzisomerie) dar, die auf der unterschiedlichen Koordination ambidenter oder flexidentater Liganden beruht. So bindet das Nitrit-Ion, NO2-, oder das Thiocyanat-Ion, SCN-, entweder über das N- oder O-Donoratom bzw. das S- oder N-Donoratom, z. B. in den Isomerenpaaren [Co(NO2)(NH3)5]Cl2 und [Co(ONO)(NH3)5]Cl2 bzw. [Pd(SCN)2{P(C6H5)3}2] und [Pd(NCS)2{P(C6H5)3}2]. Besonders wichtig sind Komplexisomerien, die als Stereoisomerien klassifiziert und in Fälle von Komplex-Diastereomerie oder Komplex-Enantiomerie unterteilt werden können. Erstere gehen entweder auf eine unterschiedliche Ligandenanordnung bei gegebener Komplexgeometrie oder die Ausbildung verschiedener Koordinationspolyeder bei gegebener Koordinationszahl zurück. Hierzu gehören etwa die cis-trans-Isomerie, die bei quadratisch-planaren oder oktaedrischen Komplexen des Typs [MA2B2] (Abb. 2), z. B. [PtCl2(NH3)2], bzw. [MA4B2] (Abb. 3a). z. B. [CoCl2(NH3)4]+, und die fac-mer-Isomerie, die bei oktaedrischen Komplexen des Typs [MA3B3] (Abb. 3b), z.B. [PtCl3(NH3)3]+, gefunden wird, sowie die Allogon-Isomerie, für die die Existenz des Gemischt ligandkomplexes [NiBr2{P(C2H5)(C6H5)2}2] sowohl

Koordinationschemie. Abb. 2: Cis-trans-Isomerie bei quadratisch-planaren Komplexen des Typs [MA2B2].
in einer tetraedrischen als auch in einer planar-quadratischen Form ein Beispiel darstellt.

Koordinationschemie. Abb. 3: Cis-trans- (a) und fac-mer- (b) Isomerie bei oktaedrischen Komplexen des Typs [MA2B4] bzw. [MA3B3].
Optische Isomerie (Spiegelbildisomerie) als Komplex-Enantiomerie wird entweder durch die Chiralität (Stereoisomerie) des Zentralatoms oder evtl. der Liganden verursacht. So treten oktaedrische Chelatkomplexe des allgemeinen Typs [M(A∩A)3] (Abb. 4; A∩A = zweizähniger Ligand) oder cis-[M(A∩A)2B2] als Enantiomerenpaare auf, die als Λ- oder Δ-Isomer bezeichnet werden. Beispiele sind etwa die Tris(oxalato)-Komplexe [M(C2O4)3]3- (M = Cr, Co) oder das Komplexkation cis-[CoCl2(H2NCH2CH2NH2)2]+.
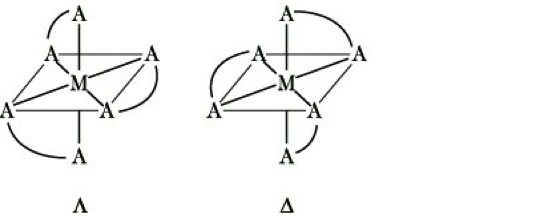
Koordinationschemie. Abb. 4: Optische Isomerie oktaedrischer Tris(chelat)-Komplexe des Typs [M(A∩A)3].
Nomenklatur. Bei der Benennung von Koordinationsverbindungen folgt auf den Namen des Kations jener des Anions. Die Bestandteile des Komplexes (Neutralkomplex, komplexes Kation oder komplexes Anion) werden in der Reihenfolge Anzahl der Liganden, Liganden (bei Gemischtligandkomplexen in alphabetischer Reihenfolge, wobei die die Anzahl der Liganden angebenden Zahlwörter nicht berücksichtigt werden), Zentralatom (unter Hinzufügung der Oxidationsstufe in römischen Ziffern) angeführt. Ist das Zentralatom Bestandteil eines komplexen Anions, erhält der Stamm des lateinischen Namens des Zentralatoms die Endung -at (Ausnahmen z. B. -antimonat, -nickelat) mit nachgestellter Oxidationsstufe. Anionische Liganden erhalten die Endung -o, z. B. Cl- Chloro, OH- Hydroxo, CN- Cyano, O2- Oxo; für wichtige Neutralliganden wie Wasser oder Ammoniak werden Bezeichnungen wie Aqua oder Ammin verwendet, Brückenliganden werden durch ein vorgestelltes μn gekennzeichnet, wobei der Brückenindex n die Anzahl der verbrückten Zentren angibt
(n = 2 wird meist weggelassen). Die Formel einer Komplexverbindung beginnt mit dem Symbol des Zentralatoms, danach folgen die Formeln der anionischen Liganden, dann der Neutralliganden und evtl. der kationischen Liganden. Die gesamte Koordinationseinheit wird in eckige Klammern gesetzt und gegebenenfalls deren Ladung angegeben. Zur Nomenklatur von Organometallkomplexen elementorganische Verbindungen. Beispiele für die rationelle Benennung klassischer Koordinationsverbindungen: Kaliumhexacyanoferrat(II), K4[Fe(CN)6]; Hexaamminnickel(II)sulfat, [Ni(NH3)6]SO4; Diammindichloroplatin(II), [PtCl2(NH4)2]; μ-Hydroxobis[pentaamminchrom(III)]chlorid, [(NH3)5Cr(OH)Cr(NH3)5]Cl5.
Komplexbildung in Lösung. Komplexbildungsreaktionen in Lösung stellen, da hier das Metall-Ion stets solvatisiert vorliegt, durchwegs Ligandenaustauschreaktionen dar. Dieser Ligandenaustausch verläuft stufenweise, wie dies für die besonders wichtige Komplexbildung in wäßriger Lösung durch folgende H2O Gleichungen angedeutet wird:
[M(H2O)6] + L ![]()
[M(H2O)5L] + H2O
[M(H2O)5L] + L ![]()
[M(H2O)4L2] + H2O
... ... ... . ..
[M(H2O)L5] + L ![]()
[ML6] + H2O
Die Konzentrationen der in Lösung nebeneinander vorliegenden Komplexspezies werden durch die individuellen Bildungskonstanten k1 = c [M(H2O)5L]/ c [M(H2O)6]·cL, k2 = c [M(H2O)4L2]/c [M(H2O)5L]·cL, ... k6 = c [ML6]/c [M(H2O)L5]·cL bestimmt; die Bruttobildungskonstante des Endkomplexes ML6, die ein Maß für die thermodynamische Stabilität dieser Verbindung ist, entspricht K= k1·k2 ... k6 = c [ML6]/c [M(H2O)6]·cL6. Durch statistische, elektrostatische und sterische Effekte bedingt, nehmen die individuellen Bildungskonstanten in der Regel stetig ab: k1> k2 > ... k6. Generell zeichnen sich Chelatkomplexe gegenüber Komplexen mit homologen einzähnigen Liganden durch signifikant erhöhte thcrmodynamische Stabilität aus, eine Erscheinung, die als Chelateffekt bezeichnet wird und im wesentlichen durch Entropiezunahme bei Chelatkomplexbildung bedingt ist. Dieser Chelateffekt sei durch einen Vergleich der Stabilitätskonstanten K für die Nickel(II)-Komplexe [Ni(NH3)6]2+ (K = 108,61) und [Ni{NH2(CH2)2NH2}3]2+ (K = 1018,28) verdeutlicht. Makrocyclische Liganden, wie z. B. Phthalocyanine, bilden wesentlich stabilere Komplexe als vergleichbare offenkettige Liganden. Dieser als makrocyclischer Effekt bezeichnete Befund führt dazu, daß die Bildungstendenz von Makrocyclen in Gegenwart geeigneter, der Ringgröße angepaßte Metall-Ionen deutlich erhöht wird (Templat-Effekt). Dies kann präparativ günstig bei vielfältigen Templatsynthesen ausgenützt werden. Für homologe oktaedrische 3d-Metallkomplexe des Typs ML6 folgt die thermodynamische Stabilität der Irving-Williams-Reihe Mn2+< Fe2+< Co2+< Ni2+< Cu2+ > Zn2+. In einem gegebenen Metall-Ligand-System nimmt die Komplexstabilität beim Übergang von M2+- zu M3+-Komplexen zu. Ein Vergleich der thermodynamischen Stabilitäten von Komplexverbindungen mit breiter Variation von Liganden und Zentralatomen zeigt, daß hier eine Klassifizierung unter Anwendung des HSAB-Konzeptes (Säure-Base-Konzepte) sinnvoll ist. Stabile Komplexe resultieren durch Kombination "weicher" Metalle, z. B. Hg(II), Pd(II), Pt(II), mit "weichen" Liganden (I-, Br-; P-, S-Donorliganden), sowie durch Kombination "harter" Metalle, z. B. D-Metalle der III. bis VI. Nebengruppe (in hohen Oxidationszahen), f-Metalle, mit "harten" Liganden (F-; O-, N-Donorliganden).
Reaktivität. Komplexverbindungen zeigen in Ligandenaustauschreaktionen (nucleophilen Substitutionen), hauptsächlich abhängig von der Art des Metalls, einen weiten Bereich unterschiedlicher Reaktivitäten, auf deren Basis sich die Verbindungen grob entweder als inert oder labil einteilen lassen. Feinere Details dieser Reaktivitätsunterschiede können mit Hilfe der Ligandenfeldtheorie erklärt werden. Hierzu werden Ligandenfeldaktivierungsenergien als Differenzen zwischen der Ligandenfeldstabilisierungsenergie des Ausgangskomplexes und derjenigen verschiedener möglicher Übergangszustände (mit idealisierten Geometrien) berechnet und die Reaktivitätsunterschiede auf die bei den einzelnen dn-Konfigurationen und angenommenen Geometrien unterschiedlichen Werte dieser Aktivierungsenergie zurückgeführt. Inertes Verhalten zeigen in der 3d-Reihe vor allem oktaedrische Chrom(III)- sowie low-spin-Cobalt(III)- und Eisen(II,III)-Komplexe, weiterhin Verbindungen der 4d- und 5d-Metalle mit mehr als zwei D-Elektronen (in der Valenzschale), wobei hier quadratisch-planare Platin(II)-Komplexe besonders eingehend untersucht wurden. Generell kann man nucleophile Ligandensubstitutionen an Komplexverbindungen unterteilen in dissoziative bzw. assoziative Prozesse, bei denen ein Zwischenprodukt mit einer um 1 verringerten bzw. um 1 erhöhten Koordinationszahl nachweisbar ist (D- bzw. A-Mechanismen,. sowie dissoziativ oder assoziativ aktivierte Auswechsel ("interchange")-Prozesse mit synchronem Reaktionsverlauf ohne Nachweis eines Zwischenprodukts
(Id- bzw. Ia-Mechanismen). Substitutionsreaktionen oktaedrischer Komplexe verlaufen meist stereospezifisch unter Erhalt der Konfiguration nach Id- oder Ia-Mechanismen über fünffach-koordinierte, quadratisch-pyramidale bzw. siebenfach-koordinierte, pentagonal-bipyramidale Übergangszustände. Seltener werden D-Mechanismen beobachtet, wobei das fünffach-koordinierte Zwischenprodukt hier meist trigonal-bipyramidalen Bau aufweist und der Ligandenaustausch dann stereounspezifisch verläuft. Dagegen sind für Substitutionsreaktionen quadratisch-planarer Platin(II)-Komplexe assoziative (Ia- oder evtl. A-) Mechanismen typisch, wobei fünffach-koordinierte, trigonal-bipyramidale Übergangszustände bzw. Zwischenprodukte auftreten und der Ligandenaustausch meist unter Retention der Konfiguration verläuft. Bei diesen Reaktionen konnte ein ausgeprägter trans-dirigierender Einfluß der Liganden ermittelt werden, der auch als trans-Effekt bezeichnet wird. Der trans-Effekt ist ein kinetischer Effekt, er beschreibt den Ligandeneinfluß auf die Substitutionsgeschwindigkeit in trans-Position. Nach Stärke des ausgeübten trans-Effektes lassen sich die gebräuchlichen Liganden wie folgt anordnen: H2O, OH-, NH3, C5H5N < Cl-, Br-, SCN-, I-, NO2-< CH3< H-, PR3< C2H4, CN-, CO. Für die Erklärung dieser Reihenfolge müssen σ- und π-Bindungseffekte berücksichtigt werden, wobei als Ursachen des trans-Effektes sowohl thermodynamische als auch kinetische Faktoren eine Rolle spielen. Zu den ersteren zählt vor allem die Schwächung der Bindung des Austrittsliganden zum Metall im Ausgangskomplex (trans-Einfluß), besonders durch trans-Liganden, die starke σ-Donoren sind, wie H- oder CH3-, aber auch durch solche mit π-Akzeptorfähigkeit. Die kinetischen Faktoren beruhen hauptsächlich auf der Stabilisierung des Übergangszustands bzw. Zwischenprodukts, die vor allem auf eine Verstärkung der Bindung des trans-Liganden zum Metall zurückgeht, und zu einer Verringerung der Aktivierungsenergie führt. Hierzu sind gute σ-Donoren, aber vor allem starke π-Akzeptoren, wie CO oder Ethylen in der Lage, deren hohe trans-Effekte weitgehend darauf zurückgeführt werden können. Der trans-Effekt wird vielfach in der Syntheseplanung für Platin(II)-Komplexe genutzt, wie dies am Beispiel der Synthesewege für cis- und trans-Diammindichloroplatin(II) demonstriert sei (Abb. 5).
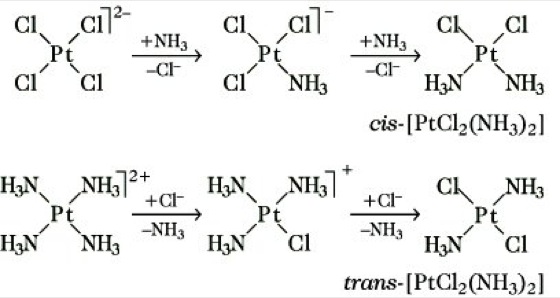
Koordinationschemie. Abb. 5: Synthesewege für cis- und trans-Diammindichloroplatin(II).
Auch in Redoxreaktionen zeigen Komplexverbindungen sehr unterschiedliche Reaktivitäten. Eine wichtige Gruppe solcher Redoxprozesse erfolgt unter Übertragung (Transfer) von Elektronen eines Komplexzentrums auf das Zentrum einer anderen Komplexverbindung. Hierbei kann sowohl Erhalt als auch Umwandlung der Ligandensphäre beider Komplexe, die dabei im allgemeinen ihre Koordinationszahlen beibehalten, beobachtet werden. Mechanistisch unterteilt man in Elektronentransfer-Prozesse, bei denen während des Elektronenübergangs die Koordinationssphären beider Komplexe intakt bleiben (Außensphären ("outer sphere")-Mechanismen) und solche, bei denen der Elektronenübergang erst nach Bildung eines zweikernigen Komplexes mit mindestens einem gemeinsamen Brückenliganden erfolgt (Innensphären ("innersphere")-Mechanismen). Nach ersterem Mechanismus verläuft etwa die Reaktion:
[FeII(CN)6]4- + [IrIVCl6]2- → [FeIII(CN)6]3- + [IrIIICl6]3-, während das klassische Beispiel eines inner sphere-Prozesses die von Taube untersuchte Reduktion des Cobalt(III)-Komplexes [CoCl(NH3)5]2+ durch das Chrom(II)-Ion [Cr(H2O)6]2+ darstellt, die folgendermaßen abläuft:
[CrII(H2O)6]2+ + [CoIIICl(NH3)5]2+ → [(H2O)5CrII-Cl-CoIII(NH3)5]4+ + H2O (Brückenbildung)
[(H2O)5CrII-Cl-CoIII(NH3)5]4+ → [(H2O)5CrIII-Cl-CoII(NH3)5]4+ (Elektronentransfer)
[(H2O)5CrIII-Cl-CoII(NH3)5]4+ + 6 H2O + 5 H+ → [CrIIICl(H2O)5]2+ + [CoII(H2O)6]2+ + 5 NH4+.
Magnetische Eigenschaften. Magnetische Untersuchungen sind eine wichtige Methode zur Klassifizierung von Übergangsmetallkomplexen. Entsprechen die ermittelten magnetischen Momente der Übergangsmetallverbindungen weitgehend jenen der freien Übergangsmetall-Ionen, so bezeichnet man diese Komplexe als high-spin-Komplexe, findet man dagegen deutlich reduzierten Paramagnetismus oder Diamagnetismus, so werden sie als low-spin-Komplexe charakterisiert. Für high-spin-Komplexe lassen sich die magnetischen Momente näherungsweise durch das Spinrnoment
(Landé-Faktor g= 2,0003, S Gesamtspinquantenzahl, μB Bohrsches Magneton) beschreiben; das bei den Ionen der ersten Übergangsperiode durch Berücksichtigung auch der Bahnbewegung der Elektronen resultierende Gesamtmoment
(L Gesamtbahndrehimpulsquantenzahl) wird meist nicht erreicht. Die Spinmomente betragen bei den freien Ionen für dn-Systeme 1,73(d1, d9), 2,83(d2, d8), 3,87(d3, d7), 4,90(d4, d6) und 5,92(d5) μB. Die 3d-Übergangsmetalle in den Oxidationsstufen +2 und +3 bilden bevorzugt, bei tetraedrischer Ligandenanordnung ausschließlich, high-spin-Komplexe, low-spin-Komplexe werden hier vor allem durch d6-Systeme wie Eisen(II), Cobalt(III) sowie Nickel(IV) in oktaedrischer und Nickel(II) in planarer Ligandenumgebung gebildet, sowie durch oktaedrische Cyanokomplexe der 3d4-, d5- und d6-Ionen repräsentiert. Low-spin-Komplexe sind ferner unter den 4d- und 5d-Übergangsmetallkomplexen häufig, so sind quadratisch planare Palladium(II)- und Platin(II)-Komplexe durchweg diamagnetisch. Das magnetische Verhalten der Übergangsmetallkomplexe läßt sich unter Anwendung der Ligandenfeldtheorie durch einen Vergleich der Spinpaarungsenergie P, d. i. die zur Paarung zweier Elektronen in einem Orbital aufzuwendende Energie, mit dem Ligandenfeldstärkeparameter 10 Dq deuten: Ist für einen gegebenen Komplex 10 Dq > P, weist dieser low-spin-Charakter auf, für P >10 Dq ist er vom high-spin-Typ. Weisen Spinpaarungsenergie und Ligandenfeldstärkeparameter etwa die gleiche Größe auf, liegen Komplexe des high- und low-spin-Typs nebeneinander in einem temperaturabhängigen Gleichgewicht (Spinüberschneidung, Spin-Crossover) vor, lassen sich also Kornplexisomere nachweisen.
Optisches Verha1ten. Eine der auff'älligsten Eigenschaften vieler Komplexe der Übergangsmetalle ist ihre Farbe, die darauf beruht, daß diese Verbindungen sichtbares Licht zu absorbieren vermögen. Entsprechend den Ursachen dieser Lichtabsorption kann man die im Elektronenspektrum eines Komplexes auftretenden Absorptionsbanden einteilen in D-D-Übergänge, bei denen ein Elektron des Zentralmetalls aus einem energieärmeren in einen energiereicheren D-Zustand übergeht, charge-transfer-Übergänge (CT), bei denen ein Elektron aus einem Orbital des Liganden in eines des Metalls (Metallreduktionsbanden) bzw. aus einem Metall- in ein Ligandenorbital (Metalloxidationsbanden) übertragen wird, Innerligand-Übergänge, bei denen ein Elektron innerhalb des Liganden aus einem energieärmeren in einen energiereicheren Zustand wechselt sowie Intervalenzübergänge, bei denen ein Elektron zwischen zwei Komplexzentren wechselt. Die D-D-Übergänge liegen häufig im sichtbaren Bereich des Spektrums und weisen aufgrund von Einschränkungen durch verschiedene Auswahlregeln (Spin-Auswahlregel, Laporte-Verbot) nur geringe Intensitäten auf. Damit zusammenhängend sind die D-D-Übergänge bei tetraedrischen Komplexen im Vergleich zu denen oktaedrischer Komplexe meist deutlich intensiver, z.B. [Co(H2O)6]2+ (schwach rosa), [CoCl4]2- (tiefblau). Zur Interpretation der Anzahl, Energie und Intensität der D-D-Banden wird zweckmäßig die Ligandenfeldtheorie herangezogen. Die charge-transfer-Banden liegen meist im UV-Bereich und zeigen deutlich höhere Intensitäten, da die ihnen zugrundeliegenden Übergänge entsprechend den Auswahlregeln erlaubt sind. Sie können aber auch in den sichtbaren Bereich hereinreichen und sind dann die Ursache für die kräftigen Farben vieler Komplexverbindungen. Beispiele für Komplexe, deren Farbigkeit auf das Auftreten von Metallreduktionsbanden im sichtbaren Bereich zurückgeht, sind etwa [CrO4]2- (gelb), [MnO4]- (violett), [VS4]3- (rotviolett). Metalloxidationsbanden werden z. B. bei Pyridinkomplexen des Typs [MX2py2] (M = Cu, Pt; py = Pyridin) und [M'X3py3] (M' = Mo, Ir) beobachtet. Ein typisches Beispiel für eine Komplexverbindung, deren Farbe auf einen Intervalenzübergang zwischen den beiden Komplexzentren Eisen(II) und Eisen(III) zurückgeht, stellt das Berliner Blau dar.
Bindungsverhältnisse. Die in Koordinationsverbindungen vorliegenden koordinativen Bindungen lassen sich vielfach alternativ auf der Grundlage sowohl elektrostatischer als auch kovalenter Bindungsmodelle interpretieren. Die Mehrzahl der Komplexe ist durch eine Überlagerung elektro- und kovalenter Bindungsanteile geprägt, typisch kovalente Komplexe stellen die Verbindungen elektronenreicher D-Metalle mit π-Akzeptor-Liganden dar. Zur theoretischen Behandlung sowohl elektrostatisch bestimmter Komplexe als auch des weiten Feldes der durch Überlagerung elektro- und kovalenter Bindungsanteile geprägten Komplexe bedient man sich heute vorzugsweise der Ligandenfeldtheorie, welche die UV/VIS-Spektren der Übergangsmetallkomplexe relativ einfach interpretieren kann und mit den daraus erhaltenen Parametern dann quantitative Aussagen auch zum magnetischen, thermodynamischen und kinetischen Verhalten der Komplexe zu liefern vermag.
Kovalente Bindungsmodelle. Bereits in den dreißiger Jahren wurde ein erstes kovalentes Bindungsmodell auf der Grundlage der Valenzstrukturtheorie (VB-Methode) entwickelt. Dabei nimmt man die Bildung koordinativer Metall-Ligand-Bindungen durch Überlappung besetzer Ligand-Orbitale mit leeren Metall-Orbitalen geeigneter Symmetrie, die durch Hybridisierung gebildet werden, an. Man unterscheidet die magnetisch normalen (high-spin) outer-orbital-Komplexe (veraltet: Anlagerungskomplexe), die den gleichen Paramagnetismus wie die freien Ionen aufweisen, von den durch reduzierten Paramagnetismus oder Diamagnetismus gekennzeichneten magnetisch anomalen (low-spin) inner-orbital-Komplexen (veraltet: Durchdringungskomplexe). Bei den ersteren werden zur Hybridisierung Metallorbitale gleicher Hauptquantenzahl n verwendet (bei tetraedrischer oder oktaedrischer Ligandenanordnung sind dies die Orbitale n s, n px, n py, n pz (sp3) bzw. n s, n px, n py, n pz, n dx2-y2, n dz2 (sp3d2)) und darin die Elektronenpaare der Liganden eingelagert, wobei die (n-1) D-Schale die gleiche Anordnung der Metallelektronen wie bei den freien Ionen aufweist. Beispiele: [NiCl4]2-, [Fe(H2O)6]2+, [CoF6]3-, [Ni(H2O)6]2+. Für die inner-orbital-Komplexe wird eine durch die Komplexbildung bewirkte weitgehende Elektronenpaarung innerhalb der partiell besetzten (n-1) D-Schale angenommen und es werden zur Hybridisierung geeignete Metallorbitale dieser (n-1) D-Schale sowie der n s-und n p-Schale verwendet. Bei quadratisch-planarer, trigonal-bipyramidaler oder oktaedrischer Ligandenanordnung sind dies die Orbitale (n-1) dx2-y2, n s, n px und n py (dsp2), bzw. (n-1) dx2-y2, n s, n px, n py und n pz (dsp3) sowie (n-1) dx2-y2, (n-1) dz2, n s, n px, n py und n pz (d2sp3). Der Diamagnetismus und Bau oktaedrischer d6-Komplexe, wie [Fe(CN)6]4- oder [Co(NH3)6]3+ sowie trigonal-bipyramidaler und quadratisch-planarer d8-Komplexe, wie [Ni(CN)5]3- bzw. [Ni(CN)4]2-, [PdCl4]2- oder [AuCl4]- lassen sich zwanglos durch den Einbau der Metallelektronen in drei bzw. vier (n-1) D-Orbitale und der Elektronenpaare der Liganden in die angegebenen Hybridorbitale erklären.
Gegenüber dem auf qualitative Aussagen beschränkten VB-Modell der Koordinationsverbindungen liefert die Molekülorbitaltheorie (MO-Theorie) der Komplexe auch quantitative lnformationen; sie findet vor allem im Bereich der kovalenten Komplexe elektronenreicher Übergangsmetalle Anwendung, da hier naturgemäß das durch die Ligandenfeldtheorie gegebene elektrostatische Bindungsmodell versagt. Die MO-Theorie der Komplexe geht von einer Kombination von Zentralatomorbitalen mit geeigneten Ligandbahnfunktionen zu bindenden bzw. antibindenden Molekülorbitalen aus und bestimmt deren Position auf der Energieskala. Unter den Metallorbitalen weisen die Orbitale dz2, dx2-y2 (Eg), s(A1g), px, py und pz (T1u) maximale Elektronendichten in Richtung Oktaederpositionen besetzender Liganden auf und sind damit zur Ausbildung von σ-Bindungen in oktaedrischen Komplexen geeignet. Die verbleibenden D-Orbitale dxy, dxz, dyz (T2g) sind hier allein zur π-Bindung befähigt, bilden daher in oktaedrischen Komplexen mit reinen σ-Donor-Liganden nichtbindende Molekülorbitale. Die sechs bindenden σ-Molekülzustände weisen stärker den Charakter von Ligand-Bahn-Funktionen auf, während die sechs T2g-Elektronen reine Metallelektronen repräsentieren (Abb. 6).
Einen wesentlich komplizierteren Charakter besitzt das MO-Schema eines oktaedrischen Komplexes mit π-bindenden Liganden. Eine qualitative Beschreibung der D-Übergangsmetall-Wechselwirkung mit π-Akzeptor-Liganden wie Kohlenmonoxid (bzw. isoelektronischen Liganden wie CN-, N2 oder NO+) kann wie folgt vorgenommen werden: Die koordinative Metall-Kohlenstoff-Bindung in Carbonylen, ähnlich auch in Cyanokomplexen, entsprechend die Metall-Stickstoff-Bindung in Distickstoff- oder Nitrosylkomplexen weist partiellen Doppelbindungscharakter durch eine Überlagerung von σ- und π-Bindungsanteilen auf. Eine Überlappung besetzter Ligand-Orbitale mit leeren Metall-Orbitalen geeigneter Symmetrie (σ-Bindung) wird durch eine Elektronenrückgabe ("back-donation") aus besetzten Metall-D-Orbitalen mit π-Symmetrie in leere, antibindende π*-Orbitale der Liganden (π-Bindung) ergänzt (Abb. 7).

Koordinationschemie. Abb. 6: MO-Diagramm oktaedrischer Komplexe [ML6] (bei ausschließlicher Metall-Ligand-σ-Wechselwirkung).

Koordinationschemie. Abb. 7: Synergetischer Bindungsmechanismus – Überlagerung von Ligand→Metall-σ- und Metall→Ligand-π-Bindungen in Matallcarbonylen.
Bei Liganden, die außer als σ-Donoren zusätzlich als π-Akzeptoren oder π-Donoren fungieren können, gehen dadurch die bei ausschließlicher σ-Wechselwirkung nichtbindenden T2g-Metallorbitale in antibindende bzw. bindende T2g* bzw. T2g-Molekülorbitale über, deren Energie gegenüber der der nichtbindenden T2g-Orbitale erniedrigt bzw. erhöht ist. Dies führt zu einer Vergrößerung bzw. Verringerung der (in der Ligandenfeldtheorie als Ligandenfeldstärkeparameter bezeichneten) Energiedifferenz Δ0 zwischen den T2g*- bzw. T2g- und den Eg*-Zuständen, und erklärt die Beobachtung, daß π-Akzeptoren, wie CO, CN-, PR3 oder Olefine starke Ligandenfelder aufbauen, dagegen π-Donoren, wie z.B. Cl-, Br-, O2- oder N3-, als schwache Liganden einzuordnen sind.
Wenn Sie inhaltliche Anmerkungen zu diesem Artikel haben, können Sie die Redaktion per E-Mail informieren. Wir lesen Ihre Zuschrift, bitten jedoch um Verständnis, dass wir nicht jede beantworten können.