Lexikon der Chemie: Madelung-Konstante
Madelung-Konstante, ein Zahlenfaktor, der die energetische Stabilisierung ausdrückt, die eine gegebene Zahl voneinander isolierter Ionenpaare bei ihrem Zusammentritt zu einem Ionengitter bestimmter Struktur erfährt. Die M. hat für jeden Strukturtyp einen charakteristischen Wert, sie hängt also nur von der Gittersymmetrie und nicht von der chem. Zusammensetzung des Ionenkristalls ab. Bei der Berechnung der M. mit Hilfe eines Reihenansatzes werden alle geometrischen Beziehungen, in denen ein herausgegriffenes Ion zu den anderen Ionen des Gitters steht, berücksichtigt. Die M. A wird bei der Berechnung der molaren GitterenergieEG nach Born in folgender Weise berücksichtigt:
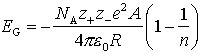
dabei bedeutet NA
Avogadro-Konstante, z+, z- Ladungszahl des Kations bzw. Anions, e Elementarladung, ε0 elektrische Feldkonstante, R0 Gleichgewichtsabstand benachbarter ungleich geladener Ionen im Kristall, n Bornscher Abstoßungsexponent. Die M. für die wichtigsten Strukturtypen von Verbindungen der allgemeinen Zusammensetzung AB und AB2 sind in der reduzierten Form in der Tabelle zusammengestellt.
Madelung-Konstante. Tab.: Madelung-Konstanten (reduzierte Form) für verschiedene Strukturtypen.
| ||
| isolierte Ionenpaare AB | 1,000 | |
| Cäsiumchlorid CsCl | 1,763 | |
| Natriumchlorid NaCl | 1,748 | |
| Wurtzit ZnS | 1,641 | |
| Zinkblende ZnS | 1,638 | |
| Fluorit CaF2 | 1,679 | |
| Rutil TiO2 | 1,605 |
Im Gegensatz zu anderen in der Literatur oft angeführten Zahlenwerten für die M., die in schwer überschaubarer Form auch die Ladungszahlen und die stöchiometrischen Koeffizienten der Ionen enthalten, sind die Ared-Werte einzig und allein geometrieabhängig. Ihr Vergleich ermöglicht deshalb eine Aussage über die energetische Effektivität bei der Ausbildung der verschiedenen Kristallstrukturen. In welchem Strukturtyp eine bestimmte Ionensubstanz wirklich kristallisiert, hängt allerdings noch entscheidend von den Radienquotienten ihrer Komponenten ab. Die Ared-Werte können nach Multiplikation mit m/2 (wobei m die Zahl der Ionen je Formeleinheit ist, also z. B. m = 2 für NaCl, m = 3 für CaF2) in die angegebene Gleichung zur Berechnung der molaren Gitterenergie eingesetzt werden.
Wenn Sie inhaltliche Anmerkungen zu diesem Artikel haben, können Sie die Redaktion per E-Mail informieren. Wir lesen Ihre Zuschrift, bitten jedoch um Verständnis, dass wir nicht jede beantworten können.