Lexikon der Chemie: Milchsäure
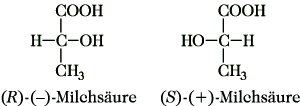
Milchsäure, α-Hydroxypropionsäure, 2-Hydroxypropansäure, CH3-CH(OH)-COOH, eine α-Hydroxycarbonsäure. M. enthält ein asymmetrisches C-Atom und ist somit chiral. Sie existiert in einer RS-Form (früher DL-Form) und den zwei optisch aktiven R- bzw. S-Formen. Den verschiedenen Formen der M. kommen als Stoffwechselprodukte pflanzlicher und tierischer Organismen besondere Bedeutung zu. M. ist in Wasser und Alkohol leicht, in Chloroform und Benzol schwer löslich. (RS)-M. oder Gärungsmilchsäure ist eine farblose bis gelbliche, hygroskopische, sirupöse Flüssigkeit; F. 18 °C, Kp. 122 °C bei 2·103 Pa. (S)-(+)-M. oder Fleischmilchsäure und die (R)-(-)-M. bilden farblose Kristalle; F. 26 °C (auch 53 °C angegeben). Die Salze und Ester der M. werden als Lactate bezeichnet.
Bei der Einwirkung von Fentons Reagens auf M. entsteht Brenztraubensäure. Durch stärkere Oxidationsmittel wird M. in Abhängigkeit von den Reaktionsbedingungen zu Oxalsäure und Kohlendioxid bzw. Essigsäure und Kohlendioxid abgebaut. M. geht beim längeren Stehen oder beim Erhitzen unter Wasserabspaltung über die Lactoylmilchsäure in Polymilchsäure über. Das Vorkommen der M. in Wein, Sauerkraut, saurer Milch, Gurken, Käse, Silage u. a. ist auf die Zersetzung von Zuckern durch Milchsäurebakterien zurückzuführen. Fleischmilchsäure wird als Zwischenprodukt der Glycolyse im Muskelgewebe gebildet. Die Herstellung der M. erfolgt hauptsächlich durch Milchsäuregärung von Lactose, Maltose oder Glucose: C12H22O11 + H2O → 4 CH3-CH(OH)-COOH. Neben diesem klassischen Verfahren wird M. auch auf synthetischem Wege hergestellt, z. B. durch Hydrolyse von Milchsäurenitril. M. und einige ihrer Derivate, besonders die Lactate, finden in der Industrie und anderen Bereichen vielfältige Verwendung, z. B. in der Woll- und Lederfärberei als Beiz- und Entkalkungsmittel, als Zusatz zu Textilhilfsmitteln und galvanischen Bädern, als Genußmilchsäure bei der Herstellung alkoholischer Getränke, als Konservierungsmittel, als Desinfektionsmittel sowie als Zusatz zu Salben und Mundwässern.
Wenn Sie inhaltliche Anmerkungen zu diesem Artikel haben, können Sie die Redaktion per E-Mail informieren. Wir lesen Ihre Zuschrift, bitten jedoch um Verständnis, dass wir nicht jede beantworten können.