Lexikon der Chemie: Molekülsymmetrie
Molekülsymmetrie, die in der räumlichen Anordnung der Atome oder Atomgruppen eines Moleküls zum Ausdruck kommende Symmetrie. Zur Beschreibung der M. benutzt man die Symmetrieelemente Drehachse Cn, Spiegelebene σ, Symmetriezentrum i und Drehspiegelachse Sn. Ihr Auftreten ist in Abb. 1 an einigen Beispielen illustriert. Die M. ergibt sich aus dem Zusammenwirken aller vorhandenen Symmetrieelemente und kann eindeutig durch die Angabe der entsprechenden Molekülsymmetriepunktgruppe bzw. deren Symbol (nach Schoenflies) charakterisiert werden. Da die M. in ei-
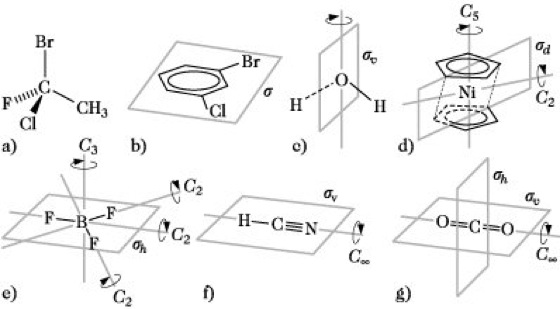
Molekülsymmetrie. Abb. 1: Moleküle mit Symmetrieelementen (es sind nur die für die Bestimmung der Symmetriepunktgruppe relevanten Symmetrieelemente dargestellt).
ner Reihe physikalischer und chem. Eigenschaften, z. B. dem Dipolmoment, der optischen Aktivität, dem spektroskopischen Verhalten oder den optischen und magnetischen Eigenschaften von Komplexverbindungen (Ligandenfeldtheorie), zum Ausdruck kommt und für deren Interpretation unerläßlich ist, besitzt ihre Bestimmung große praktische Bedeutung. Die Zuordnung eines Moleküls bekannter Geometrie zur entsprechenden Symmetriepunktgruppe gelingt ohne Schwierigkeiten, wenn man systematisch nach einem Bestimmungsalgorithmus vorgeht (Abb. 2). Man sucht dabei zunächst die Drehachse(n) höchster Zähligkeit, sofern es solche überhaupt gibt, und berücksichtigt das Vorhandensein bzw. Fehlen weiterer Symmetrieelemente entsprechend den Verzweigungen des Algorithmus.
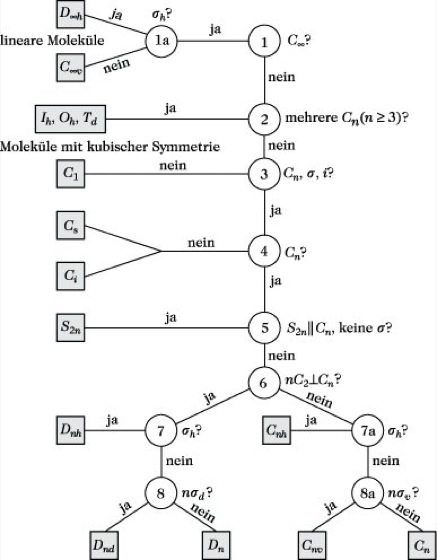
Molekülsymmetrie. Abb. 2: Algorithmus zur Bestimmung der Symmetriepunktgruppe eines Moleküls.
Auf diese Weise lassen sich die in Abb. 1 dargestellten Moleküle a bis g folgenden Punktgruppen zuordnen (in Klammern sind die für die Zuordnung relevanten Symmetrieelemente in der Reihenfolge ihres Auftretens im Algorithmus angegeben):
a) C1, b) Cs (σ), c) C2v (C2, σv), d) D5d (C5, C2 ⊥ C5, σd), e) D3h (C3, C2 ⊥ C3, σh), f) C∞v (C∞), g) D∞h (C∞, σh).
Im Zusammenhang mit der Erscheinung der optischen Aktivität spielt die M. eine entscheidende Rolle. Man bezeichnet ein Kohlenstoffatom als asymmetrisch, wenn es mit vier verschiedenen Atomen oder Atomgruppen verknüpft ist. Optisch aktive Verbindungen brauchen aber nicht asymmetrisch zu sein, was "ohne Symmetrie" bedeutet und allein der Punktgruppe C1 entspricht. Die notwendige und hinreichende Bedingung für optische Aktivität ist vielmehr die Zugehörigkeit zu den Punktgruppen C1, Cn oder Dn. Derartige Moleküle, die also kein Symmetriezentrum, keine Spiegelebene und keine Drehspiegelachse enthalten dürfen, werden als dissymmetrisch oder chiral bezeichnete (Stereoisomerie 1).
Wenn Sie inhaltliche Anmerkungen zu diesem Artikel haben, können Sie die Redaktion per E-Mail informieren. Wir lesen Ihre Zuschrift, bitten jedoch um Verständnis, dass wir nicht jede beantworten können.