Lexikon der Chemie: Nomenklatur
Nomenklatur, Nomenklatur chemischer Elemente und Verbindungen, die von den Nomenklaturkommissionen der Internationalen Union für Reine und Angewandte Chemie (IUPAC) für die Benennung chem. Elemente und Verbindungen veröff. Regeln oder Regelvorschläge. Der Artikel ist wie folgt untergliedert:
A Allgemeines
B Nomenklatur der anorganischen Chemie
I Elemente
1 Namen der Elemente
2 Sammelnamen für Gruppen und Untergruppen
II Namen von Verbindungen
1 Trivialnamen
2 Systematische Namen
3 Hydride
III Namen für Ionen und Reste
1 Kationen
2 Anionen
3 Substituenten, Radikale, Liganden
IV Homo- und Heteropolyanionen
1 Homopolyanionen
2 Heteropolyanionen mit Ketten- und Ringstruktur
3 Kondensierte Heteropolyanionen
V Säuren
1 Binäre und pseudobinäre Säuren
2 Säuren, die sich von mehratomigen Anionen ableiten
3 Funktionelle Säurederivate
VI Salze und salzartige Verbindungen
1 Einfache Salze
2 Salze, die Säurewasserstoff enthalten
3 Doppelsalze, Tripelsalze usw.
4 Oxid- und Hydroxidsalze
5 Doppeloxide und -hydroxide
VII Koordinationsverbindungen und Komplexe
1 Allgemeines über Namen für Koordinationsverbindungen
2 Namen für Liganden
3 Verbindungen mit brückenbildenden Gruppen
4 Verbindungen mit Metall-Metall-Bindung
5 Cyclopentadienyl-Komplexe
6 Bezeichnung der geometrischen Gestalt
VIII Additionsverbindungen
IX Kristalline Phasen veränderlicher Zusammensetzung
X Polymorphie
C Nomenklatur der organischen Chemie
I Unterscheidung der Namen nach dem Bildungsprinzip
1 Substitutionsnamen
2 Austauschnamen
3 Subtraktionsnamen
4 Additionsnamen
5 Konjunktionsnamen
6 Radikofunktionelle Namen
7 Anellierungsnamen
8 Hantzsch-Widman-Namen
9 Spezielle Nomenklaturen
II Prinzip der Namensbildung
1 Ermittlung der Hauptgruppe
2 Bestimmung des Verbindungsstamms
3 Benennung von Verbindungsstamm und Hauptgruppe
4 Benennung der Substituenten
5 Festlegung der Numerierung
6 Bildung des Gesamtnamens
III Aliphatische Kohlenwasserstoffe (Aliphaten)
IV Monocyclische Kohlenwasserstoffe
V Polycyclische Kohlenwasserstoffe
1 Ringsequenzen
2 Spiro-Systeme (Spirane)
3 Ortho- sowie ortho- und perianellierte Systeme
4 Brücken-Kohlenwasserstoffe
VI Heterocyclen
1 Trivialnamen
2 Heteromonocyclen
3 Heteropolycyclen
4 Behandlung der variablen Wertigkeit (Lambda-Konvention)
VII Funktionelle Derivate
1 Halogenderivate
2 Alkohole und Phenole
3 Ether
4 Aldehyde
5 Ketone
6 Carbonsäuren
7 Nitrile
8 Amine
9 Azo-Verbindungen
10 Hydrazine
11 Diazonium- und verwandte Verbindungen
12 Organoschwefelverbindungen
13 Organoselen- und -tellurverbindungen
14 Sonstige Organoelementverbindungen
VIII Spezielles
1 Ketten und Ringe
2 Radikale
3 Kationen
4 Anionen
5 Verbindungen mit zwei oder mehr ionischen Zentren gleicher Ladung
6 Verbindungen mit zwei oder mehr ionischen Zentren verschiedener Ladung
7 Isotopmodifizierte Verbindungen
D Geschichtliches
A) Allgemeines. Die ältesten Benennungen sind Trivialnamen, deren weitere Verwendung von den IUPAC-Regeln begrenzt wird.
Die eindeutige Beschreibung der Struktur einer chem. Verbindung ist durch die Formel sowie den systematischen bzw. semisystematischen Namen möglich. Der systematische Name ist die alphanumerische Beschreibung der durch die Strukturformel darstellbaren dreidimensionalen Struktur des Moleküls. Für die Benennung wird die Strukturformel in bestimmte Struktureinheiten zerlegt, die durch Namenssegmente bezeichnet und dann unter Verwendung von Stellen- und Konfigurationsangaben nach dem Baukastenprinzip zusammengesetzt werden (Abb. 1). Um Eindeutigkeit und größtmögliche Einfachheit zu erreichen, sind wie bei der Formel auch beim Namen Konventionen für die Verwendung, Schreibung und Anordnung von Namensteilen, Symbolen und Zeichen getroffen worden. Beispielsweise werden Bidestriche in Namen meist dort verwendet, wo in der englischen Sprache Leerräume stehen, so zwischen den Namen für Ionen bzw. zwischen Lokanten und den folgenden Namensteilen. Indizes zur Angabe der Ionenladung und der Anzahl gleichartiger Atome oder Atomgruppen werden in Formeln nach den IUPAC-Regeln übereinander versetzt geschrieben, z. B. SO42-. Die regelrechte Benennung einer chem. Verbindung ist nach mehreren Nomenklatursystemen möglich, von denen einige noch Alternativen zulassen. Daher gibt es für die gleiche Verbindung verschiedene IUPAC-Namen, deren Anzahl mit der Komplexität der Struktur zunimmt. Im vorliegenden Lexikon werden weitgehend neben vorhandenen Trivialnamen für anorganische Verbindungen die entsprechend den Empfehlungen der IUPAC-Nomenklaturkommissionen nach dem binären bzw. koordinativen Prinzip, für organische Verbindungen die nach dem substitutiven Prinzip gebildeten Namen aufgeführt.
B) N. der anorganischen Chemie. Für die Benennung der chem. Elemente und anorganischen Verbindungen gelten z. Z. die von der IUPAC-Kommission herausgegebenen Regeln für die N. der anorganischen Chemie 1990. Nachfolgend sind die wichtigsten Regeln angeführt.

Nomenklatur. Abb. 1: Konstruktion des Namens nach der Strukturformel.
B I) Elemente. 1) Namen der Elemente. Nach dem Wunsch der IUPAC sollten sich die Namen der Elemente in den verschiedenen Sprachen so wenig wie möglich unterscheiden. Dieses Ziel ist noch nicht erreicht. Dagegen werden die Elementsymbole in allen Sprachen einheitlich verwendet (Symbole). Die Bezeichnungen für bisher bekannte natürliche und einige künstlich hergestellte Elemente sind Trivialnamen (Periodensystem). Namen für neu entdeckte oder hergestellte Elemente werden, bis ihre Existenz eindeutig gesichert ist, systematisch aus Silben gebildet, die sich von der Ordnungszahl ableiten (0 = nil, 1 = un, 2 = bi, 3 = tri, 4 = quad, 5 = pent, 6 = hex, 7 = sept, 8 = oct, 9 = enn) und denen die Endung -ium angehängt wird, z. B. Element 123 Unbitrium (Symbol Ubt). Wegen der geringen Akzeptanz dieser Namen wird als Übergangslösung die Ordnungszahl mit der Massenzahl als linkem Exponent angegeben. Alle Isotope eines Elements sollen die gleichen Namen tragen, lediglich für die Wasserstoffisotope können die Namen Protium, Deuterium und Tritium beibehalten werden. Bei anderen Elementen erfolgt die Unterscheidung von Isotopen durch Massenzahlen, z. B. Sauerstoff-18 (Symbol: 18O). Werden Bezeichnungen vom Namen des Elements abgeleitet, so soll der lat. Name zugrunde gelegt werden; es sollen also Namen wie Aurat, Ferrat verwendet werden anstatt Goldat, Eisenat. Die Namen einiger Verbindungen des Schwefels, Stickstoffs und Antimons werden nicht von ihren lat. Namen Sulfur, Nitrogenium und Antimonium abgeleitet, sondern von Theion (griech., ›Schwefel‹), Azote (franz., ›Stickstoff‹) und Stibium (andere lat. Bezeichnung für Antimon). Quecksilberverbindungen benennt man nicht nach dem lat. Namen Hydrargyrum, sondern nach dem lat. Namen Mercurium.
B I 2) Sammelnamen für Gruppen und Untergruppen. Folgende Sammelnamen werden von der IUPAC vorgeschlagen: Actinoide oder Actinide (Ac, Th, Pa, U, Np, Pu, Am, Cm, Bk, Cf, Es, Fm, Md, No, Lr), Lanthanoide oder Lanthanide (La, Ce, Pr, Nd, Pm, Sm, Eu, Gd, Tb, Dy, Ho, Er, Tm, Yb, Lu. In den Regeln bis 1970 wurde Lanthan unter diesem Sammelnamen nicht erfaßt), Erdalkalimetalle (Ca, Sr, Ba, Ra), Chalkogene (O, S, Se, Te, Po), Halogene (F, Cl, Br, I, At), Edelgase (He, Ne, Ar, Kr, Xe, Rn), Alkalimetalle (Li, Na, K, Rb, Cs, Fr), Seltenerdmetalle (Sc, Y und die Lanthanoide), Transfermiumelemente (Md, No, Lr bis einschließlich Z 112). Weitere gebräuchliche Sammelnamen sind Transactinoide (Z 104 bis 109), Transurane (Np bis Mt). Die bis 1970 üblichen Sammelnamen Curoide (Cm, Bk, Cf, Es, Fm, Md, No, Lr) und Uranoide (U, Np, Pu, Am, Cm, Bk, Cf, Es, Fm, Md, No, Lr) werden in den Regeln von 1990 nicht erwähnt. Die Sammelnamen Triele (B, Al, Ga, In, Tl), Tetrele (C, Si, Ge, Sn, Pb), Pentele (N, P, As, Sb, Bi) sind vorgeschlagen worden, werden aber von der IUPAC nicht mehr empfohlen. Die Bezeichnung Pnicogene (anstelle von Pentele) wurde von der IUPAC nicht gebilligt. Die erste Reihe der Übergangselemente (Periodensystem) sind Sc, Ti, V, Cr, Mn, Fe, Co, Ni, Cu. Die Bezeichnung Metalloid soll nicht mehr verwendet werden; Elemente werden als Metalle, Halbmetalle und Nichtmetalle klassifiziert.
B II) Namen von Verbindungen. 1) Trivialnamen, die nicht zu falschen Deutungen führen, wie Soda, Chilesalpeter, Ätzkalk, können in der technischen und volkstümlichen Literatur ohne Bedenken verwendet werden. Dagegen sollen Namen wie schwefelsaure Magnesia, kohlensaurer Kalk, übermangansaures Kali, essigsaure Tonerde vermieden werden. Bezeichnungen wie Wasser, Ammoniak, Hydrazin, Ozon, weißer Phosphor sowie für viele Oxosäuren gehören zu den Trivialnamen. Die Verwendung von Bezeichnungen wie Salzsäure für die wäßrige Lösung von Hydrogenchlorid sowie entsprechend Flußsäure und Blausäure, ferner Natronlauge für die wäßrige Lösung von Natriumhydroxid und entsprechend Kalilauge wird sich z. Z. nicht vermeiden lassen.
B II 2) Systematische Namen werden durch Angabe der Verbindungsbestandteile, ihrer Mengenverhältnisse und deren Verknüpfung gebildet. Sehr viele Verbindungen sind binär, d. h., sie bestehen aus zwei Bestandteilen, oder sie können als binär betrachtet werden.
a) Angabe der Verbindungsbestandteile. Der Name des elektropositiven Bestandteils, also der Name des in der Formel zuerst angeführten Atoms oder der Gruppe, wird nicht verändert. Wenn zwei oder mehr elektropositive Bestandteile vorkommen, werden diese mit Ausnahme von Wasserstoff, der zuletzt genannt wird, in alphabetischer Reihenfolge aufgeführt, z. B. Ammoniumnatrium-hydrogenphosphat-tetrahydrat. Ist der elektronegative Bestandteil einatomig oder homopolyatomig, so wird sein vom (ggf. lat.) Wortstamm abgeleiteter Name mit der Endung -id versehen und an den Namen des elektropositiven Bestandteils angefügt, z. B. NaCl Natriumchlorid statt Chlornatrium, CCl4 Kohlenstofftetrachlorid statt Tetrachlorkohlenstoff. Ist der elektronegative Bestandteil heteropolyatomig, so erhält er die Endung -at, z. B. Na2CO3 Natriumcarbonat. Der Name für ein komplexes Anion wird aus dem Namen des charakteristischen Atoms oder des Zentralatoms und der Endung -at gebildet, vor dem die Namen der Liganden genannt werden, z. B. Dinatrium-tetraoxosulfat Na2SO4, Dinatrium-trioxosulfat Na2SO3. In einigen Fällen können noch Kurz- bzw. Trivialnamen verwendet werden, z. B. Natriumsulfat, Natriumsulfit. [In Ausnahmefällen werden auch die Endungen -id und -it verwendet (vgl. B III 2 b)]. Liegen zwei oder mehr elektronegative Bestandteile vor, so werden sie in alphabetischer Reihenfolge genannt.
b) Angabe der Mengenverhältnisse der Bestandteile. Die stöchiometrischen Mengenverhältnisse werden durch griech., z. T. auch lat. Zahlwörter (mono, di, tri, tetra, penta, hexa, hepta, octa, ennea oder nona, deca, hendeca oder undeca, dodeca usw.) angegeben, die den Namen der betreffenden Elemente ohne Bindestrich vorangestellt werden, z. B. PCl5 Phosphorpentachlorid. Dabei sollten die Endvokale der Zahlwörter auch bei nachfolgendem Vokal nicht weggelassen werden (Ausnahme: Monoxid). Das Zahlwort mono wird meist fortgelassen. Bei Atomgruppen, in deren Namen bereits Zahlwörter vorkommen, drückt man die Anzahl der Gruppen durch Multiplikativzahlwörter aus (lat. bis, griech. tris, tetrakis usw.). Die Gruppe, auf die sich die Multiplikativzahl bezieht, wird in Klammern gesetzt, z. B. Ca[PCl6]2 Calcium-bis(hexachlorophosphat). Das Mengenverhältnis der Bestandteile kann auch durch Angabe der Oxidationsstufe eines Elements mittels röm. Ziffern (Kapitälchen) in Klammern unmittelbar hinter dem Elementnamen gekennzeichnet werden (Stocksche Bezeichnungsweise), z. B. FeCl3 Eisen(III)-chlorid. Für Null wird die arabische Ziffer 0 benutzt. Diese Bezeichnungsweise kann sowohl auf Kationen als auch auf Anionen angewendet werden. Neben der Stockschen Bezeichnungsweise wird das Ewens-Bassett-System angewendet, bei dem die Ladung eines Ions durch eine in runde Klammern gesetzte arabische Ziffer, der das Zeichen der Ionenladung folgt, unmittelbar hinter dem Namen des Ions genannt wird, z. B. FeCl2 Eisen(2+)-chlorid.
B II 3) Hydride. Namen für binäre Wasserstoffverbindungen können systematisch gebildet werden, z. B. Hydrogensulfid.
a) Die Namen für Wasserstoffverbindungen (Hydride) folgender Atome: B, C, Si, Ge, Sn, Pb, N, P, As, Sb, Bi, O, S, Se, Te, Po (diese Elementfolge kann auf Halogenderivate ausgedehnt werden) werden aus dem Wortstamm des lat. Elementnamens und der Endung -an gebildet (Tab. 1). Bei Fehlen eines λ-Symbols gibt die Endung -an an, daß das charakteristische Element in seiner Standardbindungszahl vorliegt (s. Tab. 11), ansonsten muß die Bindungszahl nach der Lambda-Konvention (siehe C VI 4) angezeigt werden, z. B. PH5 λ5-Phosphan; SH6 λ6-Sulfan. Die an-Namen eignen sich zur Benennung von mehrkernigen Hydriden, Substitutionsprodukten und Substituenten, z. B. Tetrasilan, 1-Brom-2,2-dichlor-3-propyltriazan, 4-Disilanylheptasilan. Die Verwendung von Namen wie Phosphoran, Arsoran, Sulfuran und Persulfuran wird nicht empfohlen.
Nomenklatur. Tab. 1: Einkernige Stammhydride
|
b) Die Namen für gesättigte und ungesättigte lineare homogene mehrkernige Hydride werden aus dem entsprechenden vervielfachenden Präfix und dem a-Namen gebildet. Für die Numerierung erhalten Mehrfachbindungen die niedrigstmöglichen Lokanten, z. B. HSe-Se-SeH Triselan, H2N-N=N-NH-NH2 Pentaaz-2-en.
c1) Lineare heterogene Hydride werden auf Basis des entsprechenden Kohlenwasserstoffs mit der gleichen Anzahl der Kettenatome nach der Austauschnomenklatur (C I 2) benannt; neuerdings können die Namen auch auf Basis des homogenen Hydrids, von dem in der Kette die meisten Atome vorkommen, abgeleitet werden. c2) Alternativ ist die Benennung nach der Nomenklatur für Ketten und Ringe mit regelmäßigen Folgen von Heteroatomen (C VIII 1) möglich. Trivialnamen wie Wasser, Ammoniak, Hydrazin werden beibehalten, ebenfalls Phosphin, Arsin, Stibin, Bismutin für unsubstituierte einkernige Hydride. Vorsicht ist geboten, um Verwechslungen z. B. mit Hantzsch-Widman-Namen (vgl. C I 8 und C VI 2a) für sechsgliedrige gesättigte Heterocyclen (Dioxan, Trioxan, Diselenan) oder erlaubten Trivialnamen für andere Strukturen (Indan) zu vermeiden.
B III) Namen für Ionen und Reste. 1) Kationen. a) Einatomige Kationen werden durch den unveränderten Elementnamen benannt, deren Ladungs- bzw. Oxidationszahl (siehe B II 2 b) direkt hinter dem Namen angegeben werden kann, z. B. Cu+, Kupfer(1+)-Ion oder Kupfer(I)-Kation. Der allgemeine Name für das Gemisch der Wasserstoffisotop-Kationen ist Hydron (Elementarteilchen). Die traditionellen Namen für 1H+, 2H+ bzw. 3H+ sind Proton, Deuteron bzw. Triton. b) Mehratomige Kationen. Man unterscheidet homopolyatomige und heteropolyatomige Kationen. Eingeführte Namen für spezielle Gruppen (insbesondere sauerstoffhaltige Spezies wie Nitrosyl- und Phosphoryl-) sind weiterhin erlaubt. b1) Ein homopolyatomiges Kation kann durch Anfügen der Ladungszahl, evtl. auch der Oxidationszahl an den Namen der neutralen Einheit gebildet werden. Die Verwendung von Klammern um Formeln ist unter bestimmten Umständen zweckmäßig, z. B. (O2)+ Disauerstoff(1+)- oder Dioxygen(1+)-Ion. b2) Namen für heteropolyatomige Kationen, die formal durch Anlagerung von Hydronen an binäre Hydride entstehen, werden durch Anfügen von -ium, -diium, -triium usw. an den systematischen Namen oder Trivialnamen des Stammhydrids gebildet, z. B. N2H62+ Diazandiium-Ion oder Hydrazinium(2+)-Ion oder Hydrazindiium-Ion. Alternativ können die Namen auch durch Anfügen von -onium an den Stamm des Elementnamens (für N gilt Amm) gebildet werden. Der Name für das H3O+-Ion ist Oxonium-Ion und ist allein dieser Spezies vorbehalten. Ist der Grad der Hydratisierung des H+-Ions nicht bekannt oder spielt dieser keine Rolle, kann der einfachere Terminus Hydron oder Hydrogen- bzw. Wasserstoff-Ion verwendet werden. b3) Die Namen von kationischen Koordinationsverbindungen werden nach der Koordinationsnomenklatur (B VII) gebildet, z. B. [ICl2]+ Dichloroiod(1+)-Ion; [Al(POCl3)6]3+ Hexakis(phosphoryltrichlorid)aluminium(3+)-Ion; [H(H2O)2]+ Diaquahydrogen(1+)-Ion. b4) Kationen, die formal durch Anlagerung von Hydronen an Oxosäuren oder organische Säuren entstehen, können nach zwei allgemeinen Methoden benannt werden: (a) Behandlung der Säure als Substitutionsprodukt des Oxonium-Ions, z. B. (CH3CO2H2)+ Ethanoyloxonium- oder Acetyloxonium-Ion; (b) Verwendung der Koordinationsnomenklatur, z. B. (H4SO4)2+ Tetrahydroxoschwefel(VI)- oder Tetrahydroxosulfur(VI)-Kation. Die Endung -acidium am Namen des Anions ist im Deutschen nicht mehr gebräuchlich. b5) Kationen, die formal durch Abgabe eines Hydrid-Ions aus einem neutralen Molekül entstehen, können durch Anfügen von -ylium an den Stammnamen benannt werden. In den Namen neutraler gesättigter, acyclischer oder monocyclischer Kohlenwasserstoffe sowie einkerniger Derivate von Silan, German, Stannan, Plumban und Boran wird die Endung -an durch -ylium ersetzt. b6) Beispiele für weiterhin erlaubte triviale, nichtsystematische oder halbsystematische Namen sind: NO+ Nitrosyl-Kation, NO2+ Nitryl-Kation, UO22+ Uranyl(2+)-Kation oder Dioxouran(2+)-Ion, OH+ Hydroxylium-Ion, [HOC(NH2)2]+ Uronium-Ion. b7) Namen von kationischen Radikalen oder Substituenten werden durch Anfügen von -yl, -yliden und -diyl mit gegebenenfalls notwendigen Lokanten an die Endung -ium des Namens für das Kation erhalten. Als Alternative wird die Endung -onium für einwertige Kationen in die Endung -onio umgewandelt, z. B. H3N+- Ammoniumyl- oder Azaniumyl- oder Ammonio-, (CH3)2S+- Dimethylsulfoniumyl- oder Dimethylsulfaniumyl- oder Dimethylsulfonio-, N≡N+- Diazin-1-ium-1-yl- oder Diazonio-.
B III 2) Anionen. a) Einatomige Anionen werden benannt, indem die Endung -id an den gegebenenfalls abgekürzten lat. Namen des Elements angehängt wird, z. B. Cl- Chlorid-Ion; K- Kalid-Ion; H- Hydrid-Ion, 1H- Protid-Ion, 2H- Deuterid-Ion, C4- Carbid-Ion, Ge4- Germid-Ion. Wenn die Verbindung mehrere elektronegative Bestandteile enthält, werden deren Namen ohne Berücksichtigung etwaiger vervielfachender Präfixe alphabetisch geordnet, z. B. Na6ClF(SO4)2 Hexanatrium-chlorid-fluorid-bis(sulfat). b) Mehratomige Anionen. Es werden homopolyatomige und heteropolyatomige Anionen unterschieden. Die Ladung kann als Ladungszahl dem Namen in Klammern nachgestellt oder durch die Oxidationszahl ausgedrückt werden. b1) Homopolyatomige Anionen tragen den Namen des einatomige Stammanions, ergänzt durch das entsprechende vervielfachende Präfix und die Ladungszahl, z. B. S22- Disulfid(2-)-Ion. Müssen Strukturunterschiede betont werden, kann man runde Klammern verwenden, z. B. TlI3 Thallium-triiodid oder Thallium(3+)-triiodid, aber Tl(I3) Thallium(triiodid) oder Thallium(1+)-(triiodid). Neben den systematischen Namen sind z. B. folgende Trivialnamen erlaubt: O2- Hyperoxid- oder Superoxid-Ion, O22- Peroxid-Ion, O3- Ozonid-Ion, C22- Acetylid-Ion, N3- Azid-Ion. b2) Die Namen heteropolyatomiger Anionen bestehen in der Regel aus dem gegebenenfalls abgekürzten lat. Namen des Zentralatoms und der Endung -at; Atome und Gruppen, die an das Zentralatom gebunden sind, werden als Liganden behandelt (B VII 2), z. B. [Fe(CO)4]2- Tetracarbonylferrat(2-) oder Tetracarbonylferrat(-II). Folgende Ausnahmen mit den Suffixen -id oder -it sind noch erlaubt: H3C- Methanid, CN- Cyanid, NHNH2- Hydrazid, NH2- Amid, NH2- Imid, HO- Hydroxid, HF2- Hydrogendifluorid(1-)-Ion, PO33- Phosphit, AsO33- Arsenit, ClO2- Chlorit, ClO- Hypochlorit, NO2- Nitrit, SO32- Sulfit, S2O42- Dithionit. Das Suffix -it in den Namen vorstehender Oxosäure-Anionen gibt einen niedrigeren als den maximalen Oxidationsgrad an (B V 2a). Die Namen Sulfat, Phosphat, Nitrat usw. sind allgemein gebräuchlich für Oxoanionen, in denen Schwefel, Phosphor bzw. Stickstoff von Liganden – einschließlich Sauerstoff – umgeben sind, unabhängig von deren Anzahl und Art, z. B. SO32- Trioxosulfat oder Sulfit, SO42- Tetraoxosulfat oder Sulfat. Die noch erlaubten Präfixe Ortho-, Pyro- und Meta- sollen durch die systematischen Bezeichnungen Mono-, Di- und Cyclo- bzw. Poly- ersetzt werden. Die Verwendung der bisher üblichen Präfixe Hypo- (früher Unter-), Per- (früher Über-) o. dgl. ist auf einige Anionen beschränkt (s. B V 2a). b3) Die Namen von Anionen, die bei Verlust aller Hydronen aus charakteristischen Gruppen wie einer sauren Hydroxygruppe entstehen, werden aus den Säurenamen durch Ersatz von -säure durch -at gebildet, gegebenenfalls unter Einschub von -o-, z. B. HPO22- Phosphinat-Ion. b4) Namen von Anionen, die sich formal durch Abgabe eines oder mehrerer Hydronen aus Hydroxygruppen von Alkoholen, Phenolen und deren Chalkogen-Analoga ableiten, werden durch Anfügen von -at an den entsprechenden Namen gebildet, z. B. H3CO- Methanolat- oder Methoxid-Ion, C6H5S- Benzenthiolat- oder Benzolthiolat-Ion. b5) Namen für Anionen, die sich formal durch Abspaltung eines oder mehrerer Hydronen von Nicht-Sauerstoff-Atomen eines Hydrids ableiten, werden durch Anfügen von -id (oder -diid usw.) an den Namen der Stammverbindung gebildet, z. B. H3C- Methanid oder Methyl-Anion, PH2- Phosphandiid- oder Hydrogenphosphid(2-)-Ion, SiH3- Silanid-Ion. b6) Anionen, die sich formal durch Addition eines Hydrid-Ions an ein Stammhydrid ableiten, sollen das Suffix -uid erhalten, z. B. BH4- Boranuid. b7) Namen von anionischen Radikalen oder Substituenten, die formal durch Abgabe von Hydronen aus einem Stammhydrid entstehen, werden durch Anfügen von Suffixen wie -yl, -yliden und -diyl mit gegebenenfalls notwendigen Lokanten an den Namen für das Anion gebildet, z. B. (N≡)- Azanidyliden- oder Amidyliden-. b8) Namen für anionische Zentren, die formal durch Abgabe sämtlicher Hydronen von Chalkogenatomen in Säuren entstehen, werden durch Anfügen von -o an das Suffix -at gebildet. Die Endung -ido entsteht aus dem Suffix -id, z. B. -SO(O)2- Sulfonato-, (O-)- Oxido- oder Oxidanidyl-, (SS)- Disulfido- oder Disulfanidyl-.
B III 3) Substituenten, Radikale, Liganden. Atome und Atomgruppen (Reste) werden in Molekülen chemischer Verbindungen als Substituenten, Liganden (siehe B VII 2), die an eine Stammstruktur oder ein Zentralatom gebunden sind, sowie Radikale unterschieden. Radikale können neutral (CH3·, NO·) bzw. negativ (O2·-) oder positiv (UO2·+) geladen sein, z. B. UO22+ Uranyl(VI) oder Uranyl(2+), UO2+ Uranyl(V) oder Uranyl(1+). Substituenten und Radikale tragen oft die gleichen Namen. Um die Art der beschriebenen Spezies zu definieren, kann man das Wort Radikal oder Radikalion (Radikalkation bzw. Radikalanion) bzw. Gruppe oder Rest an den Namen der Spezies anfügen. Mit Ausnahme einiger Trivialnamen enden die Namen ungeladener Gruppen oder Radikale auf yl. So steht der Ausdruck Hydroxyl-Radikal für das Radikal HO·, Hydroxy-Verbindung für eine Verbindung, die HO-Gruppen enthält, Hydroxy-Gruppe für die Gruppe HO- selbst. Die Präfixe Thio-, Seleno- und Telluro- bezeichnen auch weiterhin den Ersatz von Sauerstoff in solchen Gruppen durch Schwefel, Selen bzw. Tellur. Die Nomenklatur anorganischer Radikale wird z. Z. aktualisiert. Diskutiert wird die Verwendung des Bindestrichs vor dem Suffix -yl in additiven Namen im Unterschied zu Substitutionsnamen, z. B. HSe· Hydridoselen-yl bzw. Selanyl. a) Systematische Namen für Radikale oder Substituenten, unterscheiden sich nicht. In den folgenden Beispielen ist daher nur die Formel für das Radikal angegeben worden. Radikalen oder Substituenten, die formal durch Abgabe von einem oder mehr Wasserstoffatomen aus jeder beliebigen Position eines Stammhydrids entstehen, werden durch Anfügen der Endung yl, diyl, yliden usw. an den Hydridnamen benannt, z. B. (CH3)· Methanyl (s. Ausnahmen), (NH)2· Azandiyl, (NH2-NH)· Diazanyl, ·OO· Dioxidan-1,2-diyl. Ausnahmen: In Namen, die sich von neutralen gesättigten acyclischen und monocyclischen Kohlenwasserstoffen sowie von Boran, Silan, German, Stannan und Plumban ableiten, wird das Suffix an durch yl ersetzt, z. B. (CH3)· Methyl, (SnCl3)· Trichlorstannyl, (BH2)· Boryl. b) Radikale und Substituenten mit Trivialnamen. Einige neutrale und kationische sauerstoff- (oder chalkogen-)haltige Radikale haben unabhängig von der Ladung, spezielle auf yl endende Namen (Tab. 2). Über O gebundene Substituenten tragen die Endung oxy-. Namen wie Bismutyl und Antimonyl sind nicht mehr erlaubt, da die Verbindungen keine abgegrenzten BiO- bzw. SbO-Gruppen enthalten; solche Verbindungen sind als Oxide zu benennen.
Diese Gruppen werden in Verbindungen als positive Bestandteile behandelt, z. B. COCl2 Carbonyl-dichlorid. c) Geladene Radikale oder Substituenten siehe B III 1 b bzw. B III 2 b. d) Verwendung von Namen anorganischer und organischer Substituenten als Präfixe. Restnamen für Elemente werden durch Anfügen der Endung io an den Namensstamm des Elements gebildet z. B. Fe- Ferrio-, S- Sulfurio-. Für Cl, Br und I sollen diese io-Namen nur verwendet werden, wenn die Wertigkeit des Radikals oder des Restes größer als 1 ist. Ist die Wertigkeit 1, so werden die Namen Chloro-, Bromo- bzw. Iodo- benutzt. Radikale oder Gruppen, die sich von einem charakteristischen Element (mit oder ohne Liganden) ableiten, haben Namen mit der Endung io-. Die Namen werden nach den Regeln der Koordinationsnomenklatur zusammengesetzt, z. B. Cl2I- Dichloroiodio-, ClHg- Chloromercurio-.
Nomenklatur. Tab. 2: Trivialnamen für Radikale und Substituenten.
|
B IV) Homo- und Heteropolyanionen. 1) Homopolyanionen. Die nach B II 2a gebildeten stöchiometrischen Namen für Salze mit Polyanionen enthalten keine strukturellen Informationen. Entstehen die Anionen durch Kondensation von Molekülen einer Monosäure, die das charakteristische Element in dem positiven Oxidationszustand enthält, der der Gruppennummer des Elements im Periodensystem entspricht, so genügt die Angabe der Anzahl der Atome dieser Elemente durch ein griech. Zahlwort. Die Nennung der Anzahl der Sauerstoffatome erübrigt sich bei Angabe der Ionenladung, z. B. S2O72- Disulfat(2-)-Ion. Bei abweichender Oxidationszahl wird diese nach der Stockschen Bezeichnungsweise angegeben (vgl. B II 2b), z. B. [O2HAs-O-AsO3H]2- Dihydrogendiarsenat(III,V)(2-)-Ion.
Ringförmige und geradkettige Strukturen können durch die Präfixe cyclo- und catena- unterschieden werden. Ist der Brückensauerstoff durch eine andere Gruppe ersetzt, so wird diese durch μ lokalisiert und mit dem entsprechenden Präfix benannt, z. B. [O3P-S-PO2-O-PO3]5- 1,2-μ-Thiotriphosphat(5-)-Ion.
B IV 2) Heteropolyanionen mit Ketten- oder Ringstruktur werden nach der Nomenklatur für Koordinationsverbindungen (B VII) oder der Nomenklatur für Ketten und Ringe benannt. Nach B VII werden hinter den Namen für Brücken und/oder Liganden die Namen der charakteristischen Elemente in alphabetischer Reihenfolge zitiert. Der Name endet mit at und der Ewens-Bassett-Zahl, z. B. [O3Cr-O-AsO2-O-PO3]4- Di-μ-oxo-octaoxo(2-arsen-1-chrom-3-phosphor)at(4-)-Ion.
B IV 3) Kondensierte Heteropolyanionen, bei denen ein Netzwerk mit vielen Zentralatomen, die tetraedrisch oder oktaedrisch von Sauerstoffatomen umgeben sind, das charakteristische Element (Hauptgruppenelement) umgibt, werden durch Angabe der Anzahl der den Tetraedern bzw. Oktaedern zugehörigen Sauerstoffliganden, dem Ligandennamen für das Hauptgruppenelement einschließlich der Sauerstoffliganden vor Anzahl und Anionnamen der Tetraeder- bzw. Oktaeder-Zentralatome, der Endung at und der Ewens-Bassett-Zahl bezeichnet, z. B. [SiW12O40]4- Hexatriacontaoxo(tetraoxosilicato)dodecawolframat-(4-)-Ion.
B V) Säuren. Die gebräuchliche N. der Säuren ist das Ergebnis einer langen Entwicklung, so daß es schwer möglich ist, die Bezeichnungen der Säuren in ein strenges System zu fassen. Nach den vorliegenden Regeln werden brauchbare Namen beibehalten; es sollte jedoch versucht werden, neue Verbindungen systematisch zu benennen.
B V 1) Binäre und pseudobinäre Säuren. Säuren, deren Anionennamen auf -id enden (vgl. B III 2), werden als binäre und pseudobinäre Wasserstoffverbindungen benannt, z. B. Hydrogenchlorid, Hydrogensulfid, Hydrogenazid.
B V 2) Säuren, die sich von mehratomigen Anionen ableiten, können analog den binären bzw. pseudobinären Säuren benannt werden, die Anionen werden als Komplexe aufgefaßt. Häufiger werden Namen so gebildet, daß bei auf -at endenden Anionennamen das Wort -säure an den Namen des charakteristischen Elements angehängt wird, z. B. Schwefelsäure, entsprechend wird die Endung -it durch -igsäure ersetzt, z. B. Schwefligsäure. Die adjektivische Bildung von Säurenamen (Zweiwortnamen, z. B. schweflige Säure) sollte aufgegeben werden.
a) Oxosäuren. Systematisch werden diese als Homopolysäuren (B IV 1) benannt. Die Verwendung der in Tab. 3 angegebenen traditionellen Namen ist weiter erlaubt, wobei das Infix -ig- zur Angabe einer niedrigeren Oxidationsstufe, das Präfix Hypo- für eine noch niedrigere und das Präfix Per- für eine höhere Oxidationsstufe dient. Oxosäuren mit verschiedenem "Wassergehalt" werden durch die Präfixe Ortho- und Meta- unterschieden, wobei das Präfix Meta- nur dann benutzt werden sollte, wenn die Struktur nicht bekannt ist. Für das Präfix Pyro- wird Di- verwendet (s. a. B III 2 b).
b) Peroxosäuren. Das Präfix Peroxo- zeigt in Verbindung mit dem Trivialnamen einer Säure den Ersatz von -O- durch -O-O- an, z. B. H2SO5 Peroxomonoschwefelsäure, H2S2O8 Peroxodischwefelsäure. c) Thiosäuren. Das Präfix Thio- zeigt an, daß ein Sauerstoffatom der Oxosäuren durch Schwefel ersetzt ist, z. B. H2S2O3 Thioschwefelsäure. Kann mehr als ein Sauerstoffatom durch Schwefel ersetzt werden, muß die Anzahl der Schwefelatome angegeben werden, z. B. H2CS3 Trithiokohlensäure. Entsprechend werden die Präfixe Seleno- und Telluro- verwendet. d) Säuren mit anderen Liganden als Sauerstoff oder Schwefel werden als Koordinationsverbindungen (vgl. B VII) benannt, z. B. H2SiF6 Hexafluorokieselsäure. Für viele Säuren mit Trivialnamen sind systematisch gebildete Namen vorzuziehen, z. B. H2MnO4 Tetraoxomangan(VI)-säure, zum Unterschied von H3MnO4 Tetraoxomangan(V)-säure.
B V 3) Funktionelle Säurederivate sind Verbindungen, die sich durch Substitution von OH oder manchmal O durch andere Atome oder Gruppen ableiten. Für sie sind noch funktionelle Namen im Gebrauch, die jedoch von der IUPAC nicht empfohlen werden. Die Namen der Säurehalogenide werden von dem entsprechenden Säurerest abgeleitet, wenn dieser einen eigenen Namen hat, z. B. SO2Cl2 Sulfurylchlorid. In anderen Fällen werden die Verbindungen systematisch nach der Koordinationsnomenklatur (B VII) oder als Halogenidoxid bezeichnet, z. B. MoCl2O2 Dichlorodioxomolybdän, Molybdän-dichlorid-dioxid. Anhydride anorganischer Säuren werden als Oxide bezeichnet, z. B. N2O5 Distickstoffpentaoxid statt Salpetersäureanhydrid. Ester anorganischer Säuren können wie die Salze benannt werden, z. B. (H3C)2SO4 Dimethyl-sulfat. Säureamide können in der Weise benannt werden, daß die Endung -amid entweder an den Namen der Säure oder an den des Säurerestes angehängt wird, z. B. PO(NH2)3 Phosphorsäuretriamid oder Phosphoryltriamid. Werden nicht alle Hydroxygruppen der Säure durch H2N-Gruppen ersetzt, so werden die Namen nach der Koordinationsnomenklatur (B VII) gebildet, z. B. NH2SO3H Hydrogen-amidotrioxosulfat. Namen wie Sulfamidsäure werden nicht mehr empfohlen.
B VI) Salze und salzartige Verbindungen. 1) Einfache Salze fallen in das Gebiet der binären Verbindungen und sollen gemäß den schon dort behandelten Regeln benannt werden (vgl. B II 2a; B III 1; B III 2), z. B. KCl Kalium-chlorid, NaClO Natrium-chlorit, (NH4)2SO4 Ammonium-sulfat, KClO4 Kalium-perchlorat.
B VI 2) Salze, die Säurewasserstoff enthalten, werden durch Zufügen des Wortes hydrogen unmittelbar vor dem Namen des Anions benannt (vgl. B II 2a), z. B. NaHCO3 Natrium-hydrogencarbonat, LiH2PO4 Lithium-dihydrogenphosphat.
B VI 3) Doppelsalze, Tripelsalze usw. In den Namen sollen alle Kationen vor den Anionen stehen, die Namen werden nach den Regeln einfacher Salze gebildet. Mit Ausnahme von Wasserstoff (vgl. B II 2a; B VI 2) werden die Kationen sowie die Anionen in alphabetischer Reihenfolge genannt. Die Mengenverhältnisse der Bestandteile werden durch Zahlwörter angegeben. Für die Anzahl der komplexen Anionen werden die Präfixe bis, tris usw. benutzt, da di, tri usw. in Namen für kondensierte Anionen verwendet werden, z. B. Na6ClF(SO4)2 Hexanatrium-chlorid-fluorid-bis(sulfat).
Nomenklatur. Tab. 3: Erlaubte Namen für gängige Oxosäuren und deren Anionen, alphabetisch geordnet nach dem charakteristischen Element.
|
Nomenklatur. Tab. 3: (Fortsetzung)
|
B VI 4) Die Namen der Oxid und Hydroxidsalze sollen wie die Namen von Doppelsalzen gebildet werden, in denen O2-- und HO--Anionen vorliegen, z. B. BiClO Bismut-chlorid-oxid, CuCl2·3Cu(OH)2 oder Cu2Cl(OH)3 Dikupfer-chlorid-trihydroxid.
B VI 5) Doppeloxide und -hydroxide. Ausdrücke wie ›gemischte Oxide‹ oder ›gemischte Hydroxide‹ werden nicht mehr empfohlen, die Verbindungen sollen vielmehr als Doppel-, Tripeloxide usw. bezeichnet werden, z. B. Cr2CuO4 Chrom(III)-tipfer(II)-oxid. Gegebenenfalls wird der Strukturtyp in Klammern hinter dem Namen angegeben, z. B. NaNbO3 Na-
triumniob-trioxid (Perowskit-Typ); ist der Typenname gleichzeitig der Mineralname, so entfällt der Zusatz -Typ, z. B. FeTiO3 Eisen(II)-titan-trioxid (Ilmenit).
B VII) Koordinationsverbindungen und Komplexe. Jede Verbindung, die durch Anlagerung von einem oder mehreren Molekülen, Resten oder Ionen an ein oder mehrere Zentralatome gebildet wird, kann als Komplexverbindung behandelt werden. Somit können viele einfache und bekannte Verbindungen als Koordinationsverbindungen benannt werden.
B VII 1) Allgemeines über Namen für Koordinationsverbindungen. Das charakteristische Atom des Komplexes wird als Zentralatom, die an dieses gebundenen Atome, Reste oder Moleküle werden als Liganden bezeichnet. Im Namen der Komplexverbindung wird das Zentralatom hinter den Liganden genannt (in der Formel werden zuerst das Symbol des Zentralatoms und dann die Symbole der anionischen, neutralen oder kationischen Liganden geschrieben). Die Oxidationsstufe des Zentralatoms kann durch die Oxidationszahl nach Stock, die Ionenladung nach Ewens-Bassett angegeben werden oder ist aus dem Mengenverhältnis der Bestandteile zu bestimmen (vgl. B II 2b). Komplexe Anionen erhalten die Endung -at, komplexe Kationen und Neutralteile tragen keine unterscheidenden Endungen. Die Liganden werden in jeder Gruppe in alphabetischer Reihenfolge angegeben.
B VII 2) Namen für Liganden. Unterschieden werden anionische, kationische und neutrale sowie ein- und mehrzähnige Liganden. Der Bindestrich in nach der Binärnomenklatur benannten Liganden bleibt erhalten [z. B. Hydrogen-sulfid für H2S, aber Hydrogensulfido für (HS)-]. Das Präfix Di ist Bestandteil des Ligandennamens zweiatomiger Elemente, auch wenn es im Namen des Elements selbst nicht genannt wird (z. B. Distickstoff). a) Die Namen für neutrale und kationische Liganden bleiben unverändert, solange keine Mehrdeutigkeit besteht. Ausnahmen sind Aqua (früher wurde Aquo geschrieben), Ammin, Carbonyl, Nitrosyl, Thiocarbonyl und Thionitrosyl für H2O, NH2, CO, NO, CS, NS sowie Ethylen, z. B. [Cr(H2O)6]Cl3 Hexaaquachrom(3+)-chlorid, Na[Co(CO)4] Natrium-tetracarbonylcobalt(-I). b) Die Namen sowohl anorganischer als auch organischer anionischer Liganden enden auf o. Wenn die Anionnamen auf id, it oder at enden, ergeben sich generell die Suffixe ido, ito bzw. ato, z. B. H3C-COO- Acetato oder Ethanato, (H3C)2N- Dimethylamido. Neben den systematischen sind von der IUPAC einige traditionelle Ligandennamen erlaubt, z. B. für O2- Oxido und Oxo, für (HO)- Hydroxido und Hydroxo, S2- Sulfido und Thio. Ausnahmen sind z. B. Br- Bromo, Cl- Chloro, (CN)- Cyano, F- Fluoro, I- Iodo. Klammern werden für anorganische anionische Liganden benötigt, die vervielfachende Präfixe enthalten, z. B. (Triphosphato), und für Thio-, Seleno- und Telluro-Analoga von Oxoanionen, die mehr als ein Sauerstoffatom enthalten, z. B. (Thiosulfato). Beispiel: K[CrF4O] Kalium-tetrafluorooxochromat(1-). c) Von Aminen, Amiden oder Iminen abgeleitete Liganden werden als substituierte Amido- oder Imido-Liganden benannt, z. B. (H3C)2N- Dimethylamido-, H3CCONH- Acetamido-, d) Die Angabe der koordinierenden Atome – in den IUPAC-Regeln von 1970 kompliziert behandelt – ist in den Regeln von 1990 vereinfacht worden. Sie kann nach dem κ-System erfolgen, z. B. NCS- Thiocyanato-κS, bei Liganden mit mehreren Koordinationsmöglichkeiten durch Angabe der Donoratome, z. B. -NH2-CH2-COO-- Glycinato-O,N. In Namen für Komplexe mit ungesättigten Molekülen oder Gruppen wird die Bindung aller Atome an das Zentralatom durch η vor dem Namen des Liganden gekennzeichnete (η-System), z. B. [Cr(C3H5)3] Tris(η3-allyl)chrom. Die Verwendung von σ und π zur Angabe des Bindungstyps wird nicht empfohlen. e) Brückenliganden sind einatomige oder mehratomige Gruppen, die über das gleiche oder verschiedene Atome verbrückt sein können und werden durch μ bezeichnet, z. B. [(CO)3Fe(CO)3Fe(CO)3] Tri-μ-carbonyl-bis(tricarbonyleisen). f) Wasserstoff wird als Ligand in Komplexen stets anionisch behandelt. Sowohl Hydrido als auch Hydro werden für koordinierten Wasserstoff verwendet, wobei Hydro auf die Bor-Nomenklatur zu beschränken ist. Beispiele: H- Hydrido, D- [2H]Hydrido.
B VII 3) Zwei- und mehrkernige Verbindungen mit brückenbildenden Gruppen werden unter Verwendung der Namen für Brückenliganden benannt (siehe B VII 2e). Namen für ausgedehnte Strukturen werden analog gebildet, z. B. [-Zn(Cl)(NH3)-Cl-]ncatena-Poly[(aminchlorozink)-μ-chloro].
B VII 4) Zwei- und mehrkernige Verbindungen mit Metall-Metall-Bindung werden durch die dem Namen angehängten Symbole der direkt verbundenen Metallatome gekennzeichnet, z. B. (CO)3Co(CO)2Co(CO)3 Di-μ-carbonyl-bis(tricarbonylcobalt)(Co-Co).
B VII 5) Cyclopentadienyl-Komplexe werden allgemein als Metallocene bezeichnet, der Trivialname für Bis(η-cyclopentadienyl)eisen, Fe(C5H5)2, ist Ferrocen. Mit -ocen gebildete Namen wie Nickelocen, Manganocen, Ruthenocen usw. sollten auf Bis(η-cyclopentadienyl)metall-Komplexe beschränkt bleiben.
B VII 6) Die geometrische Gestalt von Aggregaten aus gleichartigen Atomen (Cluster) wird durch Präfixe, z. B. triangulo-, quadro-, tetrahedro-, octahedro- usw. bezeichnet.
B VIII) Additionsverbindungen. Da nach den IUPAC-Regeln die Namen mehratomiger Anionen auf -at enden, soll diese Endung allgemein nicht mehr für Additionsverbindungen verwendet werden, ausgenommen die Bezeichnung Hydrat für eine Verbindung, die unbestimmt gebundenes Kristallwasser enthält. Die Namen von Additionsverbindungen werden gebildet, indem man die Namen der einzelnen Verbindungen mit langen Bindestrichen aneinanderfügt und die Anzahl der Moleküle durch arab. Ziffern, durch Schrägstriche getrennt, in Klammern dem Gesamtnamen nachgestellt, angibt. Bei Verwendung von Hydrat für Kristallwasser werden Zahlwörter benutzt, z. B. CaCl2·6H2O Calcium-chlorid-hexahydrat oder Calcium-chlorid-Wasser (1/6), AlCl3·4C2H5OH Aluminium-chlorid-Ethanol (1/4).
B IX) Kristalline Phasen veränderlicher Zusammensetzung. Intermediäre kristalline Phasen, deren Zusammensetzung merkliche Schwankungen aufweist, werden Berthollide genannt. Für solche Verbindungen sollen bevorzugt Formeln verwendet werden. Wenn nötig, wird die Richtung der Abweichung angegeben: Eisen(II)-sulfid (Eisen-Unterschuß), Molybdän-dicarbid (Kohlenstoff-Überschuß).
B X) Polymorphie. Die Bezeichnungen polymorpher Modifikationen durch griech. Buchstaben oder röm. Ziffern, z. B. α-Eisen oder Eis-I, können als Trivialnamen beibehalten werden. Für chem. Zwecke wird dem Namen oder der Formel ein kursiv geschriebenes Symbol für das Kristallsystem hinzugefügt, z. B. für ZnS(c) Zinksulfid(c). Strukturen können durch Anhängen der Formel oder des Namens einer typischen Verbindung gekennzeichnet werden, z. B. AuCd(CsCl-Typ) für AuCd(c), TiO2(r) Brookit-Typ.
C) N. der organischen Chemie. Die systematische Benennung organischer Verbindungen ist wegen der Vielfalt der möglichen Strukturen weit schwieriger als die der anorganischen. Die ältesten Namen, die sich vielfach bis heute erhalten haben, sind reine Trivialnamen. In ihnen drücken sich oft die Herkunft (z. B. Harnstoff, Citronensäure) oder typische Eigenschaften (z. B. Methylorange, Pikrinsäure), mitunter auch der Verwendungszweck (Gerbsäure), der Name des Entdeckers (Michlers Keton) oder rein willkürliche Gesichtspunkte (Barbitursäure) aus. Trivialnamen entstehen auch heute neu; sie sind zur Bezeichnung strukturell noch nicht aufgeklärter Verbindungen bzw. als Kurzform für einen komplizierten systematischen Namen unentbehrlich (vgl. A, Allgemeines).
Systematische Namen werden vollständig aus speziell geprägten oder ausgewählten Silben gebildet und gegebenenfalls mit alpha-, numerischen oder alphanumerischen Präfixen versehen, z. B. Pentan, Oxazol. In semisystematischen Namen hat nur ein Teil systematische Bedeutung, z. B. Benzen, Cholesterol. Die meisten Namen in der organischen N. gehören zu diesem Typ.
C I) Unterscheidung der Namen nach dem Bildungsprinzip. 1) Substitutionsnamen entstehen durch Kombination des Namens für den Stammkörper (z. B. für einen Kohlenwasserstoff) mit der Bezeichnung des Substituenten; die Substituenten, d. h. Atome oder Atomgruppen, die in einem gegebenen Molekül an die Stelle von Wasserstoff treten, können sowohl durch Präfixe (z. B. Carboxy-, Hydroxy-, Sulfanyl-, Oxo-) als auch durch Suffixe (z. B. -ol, -thiol, -on, -al, -säure) bezeichnet werden (Tab. 4); für einige existieren nur Präfixe (z. B. Chlor-, Nitro-; Tab. 5). Beispiele: Ethanal, Nitrobenzen.
C I 2) In Austauschnamen (C VI 2b) zeigen spezielle Präfixe oder Infixe den formalen Austausch von Atomen oder Atomgruppen in einer Ausgangsverbindung an. Unterschieden wird: a) der Austausch von Skeletteinheiten, beispielsweise von C, CH oder CH2 in Kohlenwasserstoffen durch ein Heteroatom durch ein auf -a endendes Präfix ("a"-Term, Tab. 10), z. B. 2,7,9-Triazaphenanthren, von O in einer Sauerstoffverbindung durch S, Se bzw. Te durch Thio-, Seleno- bzw. Telluro-, z. B. 2H-Thiopyran, oder BH-Gruppen in Borwasserstoffen, z. B. 2,4-Dicarba-closo-pentaboran(5). b) der Austausch funktioneller Gruppen, beispielsweise =O und/oder -OH in Oxosäuren, z. B. Dithioessigsäure, Chlorophosphorsäure.
C I 3) Subtraktionsnamen drücken die Eliminierung bestimmter Atome oder Atomgruppen durch die Suffixe -en, -in bzw. die Affixe anhydro-, dehydro-, desoxy- oder nor- aus.
C I 4) Additionsnamen werden durch Kombination der Namen zweier Addenden gebildet, aus denen man sich das Molekül aufgebaut denken kann, z. B. Dihydropyridin, Styrenoxid, Homophthalsäure.
C I 5) Konjunktionsnamen werden durch Aneinanderhängen der unveränderten Namen von zwei Molekülen gebildet, wobei vorausgesetzt wird, daß die Bindung zwischen den Molekülen durch Austritt von ein oder zwei Wasserstoffatomen je Molekül zustande kommt, z. B. Naphthalenessigsäure.
C I 6) Radikofunktionelle Namen setzen sich aus dem Namen eines Restes und einer charakteristischen Gruppe zusammen, z. B. Ethylalkohol.
C I 7) Anellierungsnamen (C V 3) werden gebildet, indem die Namen der anellierten Ringsysteme durch ein o miteinander verbunden werden. Dadurch wird angedeutet, daß zwei oder mehr benachbarte Atome den so verknüpften Systemen gemeinsam angehören, z. B. Pentaleno[1,2-a]inden.
C I 8) Hantzsch-Widman-Namen (C VI 2 a)) bestehen aus "a"-Termen für Heteroatome (Tab. 11) und Suffixen zur Kennzeichnung der Ringgröße und des Sättigungsgrades (Tab. 12), z. B. Oxiran, 1,3-Thiazol.
C I 9) Spezielle N. Für einige Struktur bzw. Verbindungsklassen werden eigene Nomenklatursysteme diskutiert bzw. sind entwickelt worden (z. B. für Fullerene, Helicene, Phane, Polycyclen, Polyspirane, die Anellierungs- und Stereonomenklatur). Das als Nodal-Nomenklatur bezeichnete Nomenklaturprinzip behandelt die Strukturformel als Graphen. Für Gruppen vieler Naturstoffe, wie Alkaloide, Aminosäuren, Cyclitole, Kohlenhydrate, Nucleinsäuren, Nucleotide, Peptide, Steroide, Terpene und Vitamine, sowie deren Abkürzungen und Symbole sind, historisch bedingt, besondere N. entstanden, die beibehalten wurden.
Den folgenden Abschnitten liegen die von der IUPAC-Kommission für die N. der organischen Chemie 1979 (1993 aktualisiert) veröffentlichten definitiven und vorläufigen Regeln zugrunde, wobei die substitutive N. bevorzugt wird.
C II) Prinzip der Namensbildung. Die Bildung des substitutiven Namens erfolgt in folgenden Teilschritten: 1) Ermittlung der Hauptgruppe. Charakteristische Gruppen können sowohl als Präfixe als auch als Suffixe (Tab. 4) genannt werden, einige jedoch nur als Präfix (Tab. 5). Bei Vorkommen verschiedener charakteristischer Gruppen wird die in Tab. 4 zuerst genannte als Hauptgruppe ausgewählt.
C II 2) Bestimmung des Verbindungsstamms. Als Verbindungsstamm wird der Teil der Verbindung (Kohlenstoffkette oder Ringsystem) angesehen, der die Hauptgruppe trägt. Zur eindeutigen Bestimmung, wenn z. B. verschiedene Verbindungsteile zur Wahl stehen oder keine Hauptgruppe vorhanden ist, wurden eine Reihe von Auswahlkriterien festgelegt. Die wichtigsten sind: Verbindungsstamm wird a) das System mit den meisten Hauptgruppen, b) ein Ringsystem, b1) ein Heterocyclus, b2) ein Carbocyclus, c) die längste Kette.
C II 3) Benennung von Verbindungsstamm und Hauptgruppe. Der Verbindungsstamm wird nach den in den Abschn. C III bis C VI beschriebenen Regeln benannt. Die Hauptgruppe, sie kann auch mehrfach auftreten, wird als Suffix (Tab. 4) hinter dem Namen für den Verbindungsstamm genannt.
C II 4) Benennung der Substituenten. Andere charakteristische Gruppen als die Hauptgruppe sowie acyclische, carbocyclische und heterocyclische Reste können nur als substitutive Präfixe vor dem Namen des Verbindungsstammes genannt werden. Die Bildung der Namen für komplexe Substituenten erfolgt nach den für Verbindungen geltenden Prinzipien mit der Ausnahme, daß charakteristische Gruppen nur als Präfixe genannt werden können. Das mehrfache Auftreten der gleichen Substituenten wird durch vervielfachende Präfixe angezeigt.
C II 5) Festlegung der Numerierung. Die Numerierung der Atome erfolgt nach dem Prinzip der niedrigstmöglichen Lokanten. Bei Zahlenfolgen entscheidet dabei der erste unterschiedliche Wert, d. h. 2,3,8 ist niedriger als 2,4,4. Acyclische Kohlenwasserstoffe werden von einem Ende zum anderen durchnumeriert. Die Numerierung cyclischer Verbindungen ist bei den Einzelsystemen beschrieben. Wenn für die Numerierung des Verbindungsstamms verschiedene Möglichkeiten bestehen, werden den die niedrigstmöglichen Lokanten in der angegebenen Reihenfolge vergeben an a) das indizierte Wasserstoffatom, b) die Hauptgruppe, c) Mehrfachbindungen (Doppelbindungen haben Vorrang vor
Nomenklatur. Tab. 4: Für charakteristische Gruppen verwendete Präfixe unfd Suffixe in der Reihenfolge abnehmender Priorität (Substitutionsnomenklatur).
2) Für Anionen von Säuren, Alkoholen oder Phenolen.
3) Für Anionen, die durch Abspaltung von Protonen von Kohlenstoffatomen entstanden sind.
4) R- und R'-: acyclischer, carbocyclischer bzw. heterocyclischer Rest.
5) Dieses Präfix darf nur für den unsubstituierten Rest verwendet werden. Namen für komplexe Reste werden vom Restnamen Phosphoryl für P(O)≡ abgeleitet. Allgemeines Präfix für die Verwendung in der biochem. Nomenklatur ist Phospho-, wenn die Bindung an ein Heteroatom und nicht an Kohlenstoff erfolgt.
6) Bei Verwendung in Namen für Carbonsäuresalze rangiert die mit -carboxylat bezeichnete charakteristische Gruppe vor den Kationen.
Dreifachbindungen), d) alle als Präfixe genannten Substituenten einschließlich der Hydro-Präfixe, e) das nach der alphabetischen Reihenfolge zuerst genannte Präfix. In Substituenten erhält die Verknüpfungsstelle unter Beachtung der für die Numerierung des Verbindungsstamms geltenden Prinzipien den niedrigstmöglichen Lokanten, in acyclischen Resten immer 1. In cyclischen Resten hat das indizierte Wasserstoffatom Vorrang vor der Verknüpfungsstelle.
Nomenklatur. Tab. 5: Nur als Präfixe zu nennende charakteristische Gruppen (Substitutionsnomenklatur).
|
C II 6) Bildung des Gesamtnamens. Das Suffix für die Hauptgruppe steht hinter, Präfixe stehen vor dem Namen des Verbindungsstamms. Lokanten stehen grundsätzlich vor dem zugehörigen Namensteil. Mit Ausnahme der nicht abtrennbaren Präfixe (für Bezeichnung von Ringbildung, Ringspaltung, Größenänderung, Anellanden, "a"-Termen, Isomeren, indiziertem Wasserstoff, Brückengruppen und Hydro-) erfolgt die Anordnung alphabetisch. Präfixe für einfache Substituenten werden entsprechend der Buchstabenfolge des Namens geordnet; vervielfachende Affixe werden nicht berücksichtigt (z. B. 2,3,6,7-Tetrabrom-1,4-dimethyl-naphthalen). Präfixe für komplexe Substituenten werden entsprechend der Buchstabenfolge ihres vollständigen Namens eingeordnet. Innerhalb des komplexen Präfixes erfolgt die Anordnung der Nebensubstituenten ebenfalls alphabetisch (z. B. 1-Chlor-3-(ethylmethylamino)-2,7-dimethoxy-fluoren-4-carbonsäure, 1-(2-Hydroxy-ethyl)-8-(2-hydroxy-propyl)-1-naphthoesäure). Bestehen mehrere Präfixe aus gleichen Wortelementen, dann rangiert dasjenige vor dem anderen, welches an der ersten im Namen auftretenden Abweichung den niedrigeren Lokanten trägt (z. B. 2-(2-Nitro-phenyl)-7-(3-nitro-phenyl)-naphthalen).
C III) Aliphatische Kohlenwasserstoffe (Aliphaten). Die gesättigten Kohlenwasserstoffe der allg. Formel CnH2n+2 haben den Klassennamen Alkane (Paraffine, Grenzkohlenwasserstoffe). Die ersten 4 unverzweigten Glieder der Reihe (n = 1 bis 4) werden mit den Semitrivialnamen Methan, Ethan, Propan und Butan bezeichnet. Alle weiteren Namen bildet man aus dem Stamm eines griech. oder lat. Zahlwortes für n und der Endung -an, z. B. für n = 12 Dodecan. Die Namen für die ungesättigten aliphatischen Kohlenwasserstoffe Alkene (Olefine, Ethylenkohlenwasserstoffe) und Alkine (Acetylene, Acetylenkohlenwasserstoffe) werden aus dem Wortstamm der entsprechenden gesättigten Verbindung, der Angabe der Lage der Mehrfachbindungen (vgl. C II 5) und den Endungen -en, -adien (1 bzw. 2 Doppelbindungen), -in, -adiin (1 bzw. 2 Dreifachbindungen), -enin (je 1 Doppel- und 1 Dreifachbindung) usw. gebildet, z. B. H3C-CH=CH-CH3 But-2-en, H3C-CH=CH-C≡CH Pent-3-en-1-in. Kohlenwasserstoffreste werden benannt aus dem a) Wortstamm bzw. b) Namen des entsprechenden Alkans und den Endungen -yl- (einwertiger Rest), -yliden- (zweiwertiger geminaler Rest) bzw. -ylidin- (dreiwertiger geminaler Rest) und deren Kombination oder -yl-, -diyl-, -triyl-. Nach a) hat das bindende Atom den Lokanten 1. Beispiele: -CH2-CH2-CH2-
Propan-1,3-diyl-, H3C-CH2-C|= Propan-1-yl-1-yliden-, (H3C)2C= Propan-2-yliden- oder 1-Methylethyliden-. Folgende Trivialnamen, z. T. nur für die unsubstituierte Struktur, werden weiter verwendet für Kohlenwasserstoffe: CH4 Methan, H3C-CH3 Ethan, H3C-CH2-CH3 Propan, H3C-CH2-CH2-CH3 Butan, H3C-CH(CH3)2 Isobutan, H3C-CH2-CH(CH3)2 Isopentan, C(CH3)4 Neopentan, H2C=C=CH2 Allen, HC≡CH Acetylen, H2C=CH-C(CH3)=CH2 Isopren; für Reste: (H3C)2CH- Isopropyl-, (H3C)2CH-CH2- Isobutyl-, H3C-CH2-CH(CH3)- sec-Butyl-, (H3C)3C- tert-Butyl-, (H3C)2CH(CH2)2- Isopentyl-, (H3C)3C-CH2- Neopentyl-, H3C-CH2-C(CH3)2- tert-Pentyl-, H2C=CH- Vinyl-, H2C= CH-CH2- Allyl-, H2C=C(CH3)- Isopropenyl-, -CH2- Methylen, -CH2-CH2- Ethylen-, H2C= Methyliden-, (H3C)2C= Isopropyliden-, H2C=C= Vinyliden-.
C IV) Monocyclische Kohlenwasserstoffe sind Verbindungen, bei denen eine gesättigte oder ungesättigte Kette von Kohlenstoffatomen zu einem Ring geschlossen ist. Sie tragen den Klassennamen Cycloalkane, Cycloalkene usw. Die Namen einschließlich der für die Reste werden von denen der entsprechenden Aliphaten abgeleitet, denen das Präfix Cyclo- vorangestellt wird. Beispiele:

Die Verbindung o-, m- bzw. p-Menthan gehört zur Klasse der Terpene (Monoterpene) Die Namen für aromatische, monocyclische Kohlenwasserstoffe leiten sich vom Semitrivialnamen Benzen (Benzol) ab; der Klassenname (auch für polycyclische Verbindungen) ist Arene. Lokanten für Di-, Tri- und Tetrasubstitutionsprodukte mit gleichen Substituenten sind o -, 1,2- (für ortho-); m-, 1,3- (für meta-); p-, 1,4- (für para-); vic- = 1,2,3- und 1,2,3,4- (für vicinal-); asym = 1,2,4- und 1,2,3,5- (für asymmetrisch-); sym = 1,3,5- und 1,2,4,5- (für symmetrisch-). Beispiel:

Der einwertige bzw. zweiwertige Rest von Benzen heißt Phenyl- bzw. o-, m- oder p-Phenylen; Klassennamen sind Aryle bzw. Arylene. Folgende Trivialnamen sind weiter erlaubt:

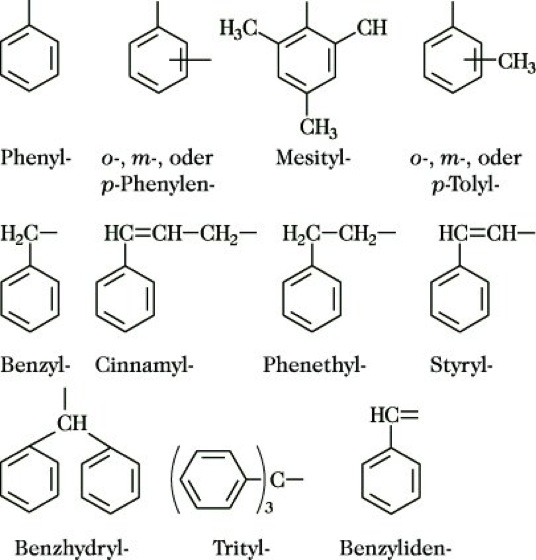
C V) Polycyclische Kohlenwasserstoffe. Wenn zwei oder mehr Ringe direkt miteinander verknüpft sind, so kann man je nach der Anzahl der zwei Ringen gemeinsamen Ringatome zwischen Ringsequenzen mit null gemeinsamen Atomen, Spiro-Systemen (Spirane) mit einem, ortho- sowie ortho- und peri-anellierten Systemen mit je zwei benachbarten und Brücken-Systemen mit zwei oder mehr gemeinsamen Atomen unterscheiden.
C V 1) Ringsequenzen können als cycloalkyl- bzw. arylsubstituierte Cycloaliphaten oder Aromaten benannt werden. Sind zwei oder mehr identische Ringe unverzweigt aneinandergereiht, so wird das Präfix Bi-, Ter-, Quater- usw. dem Stammnamen des entsprechenden Cyclus vorangesetzt. Beispiele:

Ringsequenzen aus Benzenringen dürfen nur unter Verwendung von -phenyl benannt werden.
C V 2) Spiro-Systeme (Spirane). Spirocyclische Systeme erhalten entweder a) den Namen des Kohlenwasserstoffs gleicher C-Zahl, dem entsprechend der Anzahl der Spiroatome das Präfix Spiro-, Dispiro- usw. und in eckige Klammern [] eine Charakteristik, die die Anzahl der von den Spiroatomen ausgehenden Brückenatome (beginnend mit der kleineren endständigen Brücke) angibt, vorangestellt werden, oder, wenn mindestens ein anelliertes oder verbrücktes Ringsystem mit Trivialnamen vorhanden ist, b) das Präfix Spiro-, Dispiro- usw. und die Namen der Einzelsysteme, beginnend mit dem alphabetisch zuerst zu nennenden System (die Spiroverknüpfung wird mit deren kleinstmöglichen Lokanten angegeben).

Die Numerierung nach a) beginnt im kleineren Außenring neben dem Spiroatom und verläuft so, daß die Spiroatome die niedrigstmöglichen Lokanten erhalten; nach b) wird die Numerierung der Einzelsysteme (Lokanten in Klammern) beibehalten.
Die alternative Benennung mit dem Spiro-Präfix zwischen den Namen der Einzelsysteme ist in der 1993er Ausgabe der IUPAC-Regeln aufgegeben worden.
C V 3) Ortho- sowie ortho- und peri-anellierte Systeme. Polycyclische Verbindungen mit der maximalen Anzahl nicht-kumulierter Doppelbindungen, in denen zwei Ringe nur zwei Atome gemeinsam haben, nennt man ortho-anelliert; solche, in denen ein Ring nur je zwei Atome mit jedem von zwei oder mehr Ringen einer Folge anellierter Ringe gemeinsam hat, werden als ortho- und peri-anelliert bezeichnet. Für 35 Polycyclen sind Trivialnamen mit der angegebenen Numerierung erlaubt (Tab. 6). Die Namen für Polycyclen ohne erlaubten Trivialnamen werden gebildet, indem dem Namen des größtmöglichen Stamm-Ringsystems der Name des möglichst einfach zu wählenden angegliederten Systems (Anelland) vorangestellt wird. Die Art der Anellierung wird in eckigen Klammern [] durch die Lokanten der Atome des Anellanden und durch die Seite des Stammsystems (1,2 = a), die an der Verknüpfung beteiligt sind, bezeichnet (Charakteristik). Die Namen aromatischer Anellanden enden auf o-; Ausnahmen sind folgende abgekürzte Präfixe: Acenaphtho-, Anthra-, Benzo-, Naphtho-, Perylo-, Phenanthro-. Für monocyclische Systeme mit der maximalen Anzahl nicht-kumulierter Doppelbindungen wird an den Wortstamm ein a- angehängt, z. B. Cyclopenta-. Die Numerierung des anellierten Systems erfolgt unabhängig von der der Einzelsysteme unter Beachtung folgender Konventionen:
a) Die Einzelringe werden wie folgt gezeichnet:
Die im Uhrzeigersinn vorzunehmende Numerierung beginnt an dem Ringatom, das am weitesten links im oberen rechten Ring steht. Atome an Anellierungsstellen werden durch die Stellenangabe des vorangehenden Atoms, erweitert durch a, b, c ..., lokalisiert.

Verbindungen aus 4 und mehr linear anellierten Benzolringen werden durch ein Zahlwortpräfix und das Suffix -acen benannt, z. B. Tetracen.
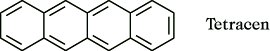
Ortho- sowie ortho- und peri-anellierte Systeme mit weniger als der maximalen Anzahl an nicht-kumulierten Doppelbindungen werden als Hydro-Derivate bezeichnet.
Nomenklatur. Tab. 6: Erlaubte Trivialnamen für ungesättigte ortho- sowie ortho- und peri-anellierte Kohlenwasserstoffe (Priorität steigend).
|
2) In der Nomenklatur anorganischer Verbindungen sind die Präfixe asym bzw. sym vorgeschrieben.
Folgende Trivialnamen für gesättigte polycyclische Systeme sind erlaubt: Indan, Prisman, Cuban, Adamantan. Reste erhalten die Namen des Kohlenwasserstoffs und die entsprechende Endung, z. B. Pyren-1-yl-, Fluoren-9-yliden-. Folgende Kurznamen sind weiter üblich: Naphthyl- (2 Isomere), Anthryl- (3 Isomere), Phenanthryl- (5 Isomere) und Adamantyl- (2 Isomere).
C V 4) Brücken-Kohlenwasserstoffe sind Verbindungen mit zwei oder mehr Ringen, in denen wenigstens zwei Ringe zwei oder mehr gemeinsame Kohlenstoffatome haben. Eine Anzahl von Brücken-Systemen mit Trivialnamen kommen in der Verbindungsklasse der Terpene (Monoterpene) vor. Die systematische Benennung ist a) nach der erweiterten Von-Baeyer-Nomenklatur oder b) als ortho- bzw. ortho- und peri-anellierte Verbindungen mit zusätzlichen Brücken möglich. Nach a) wird der Name aus einem der Anzahl der Ringe entsprechenden Präfix Bicyclo-, Tricyclo- usw., einer Charakteristik in [], in der in absteigender Folge die Anzahl der Atome zwischen den Brükkenköpfen angegeben wird, und dem Namen für den Kohlenwasserstoff der entsprechenden C-Zahl gebildet. Die Numerierung beginnt an einem Brückenkopf, verläuft über den längsten Weg zu diesem zurück in die größte Brücke (Hauptbrücke) hinein. Es folgen, ausgehend vom höchstnumerierten Brückenkopf die nach abnehmender Länge geordneten Sekundärbrücken (in der Charakteristik wird die Lage der Sekundärbrücken durch Hochzahlen angegeben). Nach b) wird die zusätzliche Brücke als zweiwertiger Rest (Tab. 7) vor dem Namen des ortho- bzw. ortho- und peri-anellierten Systems genannt. Die Numerierung des Polycyclus wird beibehalten; die Brückenatome werden ausgehend vom Brückenkopf mit der höheren Stellenangabe gezählt. Beispiele:
1) Entsprechend für Brücken ungesättigter polycyclischer Kohlenwasserstoffe (Tab. 6).
2) Entsprechend für ungesättigte monocyclische Kohlen-wasserstoff-Brücken, ausgenommen Benzen.
Nomenklatur. Tab. 8: Erlaubte Trivial- und Semitrivialnamen für Heterocyclen mit der maximalen Anzahl nicht-kumulierter Doppelbindungen (steigende Priorität).
|
2) Für Chalkogenanaloga werden die Präfixe Thio-, Seleno- bzw. Telluro- verwendet.
3) Das 2H-Isomere hat Priorität vor dem 1H-Isomeren.
4) Das 4aH-Isomere hat Priorität vor dem 1H-Isomeren.
5) Das 3H-Isomere hat Priorität vor dem 9H-Isomeren.
Nomenklatur. Tab. 9: Erlaubte Trivial- und Semitrivialnamen für hydrierte Heterocyclen (steigende Priorität).
|
2) Für den über N gebundenen Rest kann der Name Piperidino- bzw. Morpholino- verwendet werden.
Nomenklatur. Tab. 10: Rangfolge der Elemente und der in der Austauschnomenklatur verwendeten "a"-Terme in der Ordnung abnehmender Priorität.
|
C VI) Heterocyclen. Im weiteren Sinne sollten unter heterocyclischen Verbindungen Ringsysteme verstanden werden, die aus wenigstens zwei verschiedenen Elementarten aufgebaut sind, im engeren Sinne Strukturen, die im Ring neben Kohlenstoff noch andere Elemente, die Heteroatome, als Ringglieder enthalten.
C VI 1) Trivialnamen. Die in Tab. 8 aufgeführten Ringsysteme sind in steigender Rangfolge für die Wahl als Verbindungsstamm in Anellierungsnamen angeordnet. Die in Tab. 9 aufgeführten Trivial- und Semitrivialnamen für 11 hydrierte Heterocyclen sind weiter erlaubt, dürfen als Restnamen verwendet werden, nicht aber als Stammnamen für die Benennung anellierter Systeme.
Nomenklatur. Tab. 11: "a"-Terme für Heteroatome in Heterocyclen (Hantzsch-Widman-System), abnehmende Priorität.
|
2) Bis zur Revision 1979 mußte vor der Endung -in anstelle von Phospha-, Arsa- bzw. Stiba-, Phosphor-, Arsen- bzw. Antimon geschrieben werden. Die Phosphorin und Arsenin entsprechenden gesättigten Verbindungen hießen Phosphorinan und Arsenan. Bei Vorkommen von Blei, Germanium, Silicium und Zinn als Heteroatom konnte die Endung -an nicht angewendet werden. In diesem Falle wurde das Präfix Perhydro- vor dem Namen der entsprechenden ungesättigten Verbindung verwendet.
3) Zwischenzeitlich wurde Bismuta- geschrieben.
Die Namen Pyrrolidin, Imidazolin und Pyrazolin wurden in die Auflage von 1993 nicht übernommen, diese Strukturen werden auf Basis der Hantzsch-Widman-Namen der ungesättigten Heteromonocyclen bezeichnet.
C VI 2) Heteromonocyclen. Die systematische Benennung kann nach zwei Prinzipien erfolgen. Beide verwenden für die Bezeichnung der Heteroatome auf -a endende Namen, die "a"-Terme (Tab. 10 und 11).
a) Die erweiterte Hantzsch-Widman-Nomenklatur (vgl. C I 8) baut die Namen 3- bis 10gliedriger Heterocyclen aus dem "a"-Term für das Heteroatom (Tab. 11) und einem Ringgröße und Sättigungsgrad angebenden Wortstamm (Tab. 12) auf. Im Gegensatz zu den IUPAC-Regeln von 1979 wird nicht mehr zwischen stickstofffreien und stickstoffhaltigen Ringen unterschieden.
Nomenklatur. Tab. 12: Angabe von Ringgröße und Sättigungsgrad nach dem erweiterten Hantzsch-Widman-System (Revision 1982).
|
2) Der Stamm wird verwendet, wenn das Ringsystem keine Doppelbindung enthält oder keine möglich ist. Bis zur Revision 1982 wurde die Sättigung für 6- und mehrgliedrige N-haltige Ringe durch Perhydro- angegeben.
3) Bis zur Revision 1982 lautete der Stamm für ungesättigte 3-gliedrige N-haltige Heterocyclen -irin; er kann für Ringe, die nur Stickstoff enthalten, weiter verwendet werden.
4) Die traditionellen Stämme -iridin, -etidin bzw. -olidin sind für die Benennung N-haltiger Ringe vorzuziehen.
5) Bis zur Revision 1982 wurden für N-haltige Heterocyclen mit einer Doppelbindung die Endung -etin, für N-freie der Stammeten verwendet.
6) Bis zur Revision 1982 wurden für N-haltige Heterocyclen mit einer Doppelbindung der Stamm -olin, für N-freie der Stammolen verwendet.
7) Für den richtigen Stamm muß aus folgenden Atomsätzen derjenige ausgewählt werden, der das Heteroatom der niedrigsten Priorität enthält.
6A O, S, Se, Te, Bi, Hg
6B N, Si, Ge, Sn, Pb
6C B, F, Cl, Br, I, P, As, Sb
Die Namen Oxin (für Pyran) und Azin (für Pyridin) können nicht verwendet werden, da der erste als Trivialname für Chinolin-8-ol benutzt wurde, der zweite der Klassenname für =N-N=-Verbindungen ist.
Die speziellen Endungen für 4- und 5gliedrige Heteromonocyclen mit einer Doppelbindung, wenn mehr als eine möglich ist, werden nicht weiter verwendet.
Die Anzahl der "a"-Terme in der für Heteromonocyclen aufgestellten Tab. 11 wird um die für die Halogene auf 19 erweitert. Die Numerierung beginnt an einem Heteroatom derart, daß die Heteroatome insgesamt die niedrigst möglichen Lokanten erhalten. Nur wenn verschiedene Möglichkeiten bestehen, erhalten die vorrangigen Heteroatome die niedrigst möglichen Lokanten.
Folgende Kurzbezeichnungen für Reste sind weiter erlaubt: Furyl- (für Furanyl-), Pyridyl- (für Pyridinyl-), Piperidyl- (für Piperidinyl-), Chinolyl- (für Chinolinyl-), Isochinolyl- (für Isochinolinyl-), Thienyl- (für Thiophenyl-), Furfuryl- (für Fur-2-ylmethyl-), Thenyl- (für Thien-2-ylmethyl-). Die Namen Piperidino- und Morpholino- werden neben den Restnamen Piperid-1-yl- und Morpholin-4-yl- verwendet.
b) Austausch-Nomenklatur (C I 2). Die Namen werden aus dem "a"-Term für das Heteroatom (Tab. 10) und dem Namen des entsprechenden Kohlenwasserstoffs gebildet.
Beispiele:
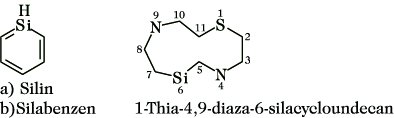
C VI 3) Heteropolycyclen. Für einige Heteropolycyclen gibt es Trivialnamen (Tab. 8 und 9). Die systematische Benennung kann unter Verwendung von erlaubten Trivialnamen für Heterocyclen erfolgen für a) Ringsequenzen (vgl. C V 1), b) Spiro-Systeme (vgl. C V 2), c) ortho- sowie ortho- und peri-anellierte Heterocyclen nach dem Anellierungsprinzip (vgl. C V 3). Kurznamen für Anellanden sind Furo- (für Furano-), Thieno- (für Thiopheno-), Imidazo- (für Imidazolo-), Pyrido- (für Pyridino-), Pyrimido- (für Pyrimidino-), Chino- (für Chinolino-), Isochino- (für Isochinolino-) und d) Brücken-Systeme (vgl. C V 4b). Alternativ können Heteropolycyclen nach der Austauschnomenklatur aufbauend auf den Namen der entsprechenden Kohlenwasserstoffe (vgl. C V 1, 2 und 4) benannt werden. Dabei kann dem Austauschnamen, wenn der entsprechende Kohlenwasserstoff nicht die maximale Anzahl nichtkumulierter Doppelbindungen enthält, aber mit einem Trivialnamen (s. C V 3b) bezeichnet wird, dieser Name zugrunde gelegt werden, z. B.

Ist dies nicht möglich, wird die nach Einführung der Heteroatome vorliegende Verbindung als Stammverbindung des Heterocyclus angesehen. Der Ausgangskohlenwasserstoff wird in der Form mit der maximalen Anzahl nichtkumulierter Doppelbindungen benannt:

Nach c) erhalten die Heteroatome die niedrigstmöglichen Lokanten. Ein an einer Anellierungsstelle befindliches Heteroatom wird bei der umlaufenden Numerierung mitgezählt. Bei Benennung nach a), b) und d) wird die Numerierung des Grundsystems beibehalten.
Beispiele:
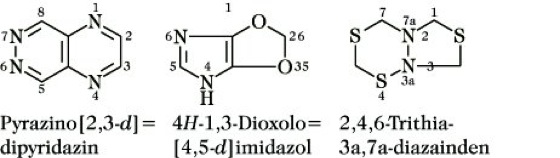
C VI 4) Behandlung der variablen Wertigkeit (Lambda-Konvention). Diese Methode wird auch bei der Benennung anorganischer Hydride (B II 3) angewendet. Die Unterscheidung von Heteroatomen, die in zwei oder mehr Bindungszahlen (Wertigkeiten) vorkommen können, wird durch die Lambda-Konvention vereinheitlicht. Danach wird die Nichtstandard-Bindungszahl durch λn (n ist die Bindungszahl eines Skelettatoms) vor dem Namen des Stammhydrids bezeichnet.

Für die Angabe von kumulierten Doppelbindungen wurde das Symbol δc (c ist die Anzahl der Doppelbindungen) vorgeschlagen.
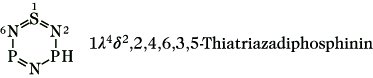
C VII) Funktionelle Derivate. Die verschiedenen Verbindungsklassen der organischen Chemie werden durch Suffixe, teilweise nur durch Präfixe für die charakteristischen Gruppen (Tab. 4) am Namen des Verbindungsstamms bezeichnet. Einige Verbindungsklassen lassen sich nur nach der radikofunktionellen Nomenklatur durch funktionelle Klassennamen charakterisieren. Die Nomenklatur der Organometallverbindungen (C VII 14 a) behandelt das Grenzgebiet zwischen anorganischer und organischer Chemie. Die Einzelverbindungen werden sowohl nach dem substitutiven als auch dem additiven (koordinativen) Prinzip benannt.
Die Benennung der Einzelverbindungen innerhalb der Verbindungsklassen kann im folgenden nur auszugsweise ausgeführt werden.
C VII 1) Halogenderivate können nach dem substitutiven Prinzip nur durch Präfixe benannt werden, z. B. H3C-Br Brommethan (radikofunktioneller Name: Methylbromid). Erlaubte Trivialnamen sind: HCF3 Fluoroform, HCCl3 Chloroform, HCBr3 Bromoform, HCI3 Iodoform, COCl2 Phosgen, CSCl2 Thiophosgen und entsprechend die anderen Chalkogen-Analogen.
C VII 2) Alkohole und Phenole werden durch das substitutive Suffix -ol bezeichnet. Nach der radikofunktionellen Nomenklatur wird der Klassenname -alkohol verwendet; die Bezeichnung -carbinol ist nicht mehr üblich. Beispiele für Trivialnamen sind: Ethylenglycol, Glycerol (Glycerin), Ethylenglycol, Pentaerythritol (Pentaerythrit), Pinacol (früher Pinacon), Phenol, Cresol (3 Isomere), Cavarcrol, Thymol, Brenzcatechin, Resorcinol (Resorcin), Hydrochinon, Pikrinsäure. Namen für über Sauerstoff gebundene Gruppen werden aus dem Restnamen und dem Suffix -oxy- gebildet. Folgende Kurznamen für Reste sind weiter erlaubt: Methoxy- für Methyloxy-, Ethoxy- für Ethyloxy-, Propoxy- für Propyloxy-, Isopropoxy- für Isobutyloxy-, sec-Butoxy- für sec-Butyloxy-, tert-Butoxy- für tert-Butyloxy- und Phenoxy- für Phenyloxy-.
C VII 3) Ether werden nach der substitutiven N. als alkoxy/aryloxysubstituierte Kohlenwasserstoffe oder Heterocyclen bezeichnet; der radikofunktionelle Klassenname ist -ether, z. B. H5C2-O-CH3 Methoxyethan (radikofunktioneller Name Ethylmethylether). Der Trivialname Anisol ist weiter erlaubt.
C VII 4) Aldehyde. Der substitutive Name wird aus dem der entsprechenden Stammverbindung und dem Suffix -al gebildet. Die direkt an einen cyclischen Verbindungsteil gebundene -CHO-Gruppe heißt -carbaldehyd. Trivialnamen leiten sich von dem der entsprechenden Säure (C VII 6) durch Ersatz von -säure durch -aldehyd ab, z. B. Acrylaldehyd, Zimtaldehyd.
C VII 5) Ketone werden durch das Suffix -on am Namen der entsprechenden Stammverbindung bezeichnet. Radikofunktionell wird der Name aus dem funktionellen Klassennamen -keton für die -CO--Gruppe und den Namen der an diese gebundenen Reste gebildet. Aromatische Diketone werden unter dem Klassennamen Chinone zusammengefaßt.
Beispiel: H5C2-CO-CH3 Butan-2-on (radikofunktioneller Name: Ethylmethylketon).
Erlaubt sind nur folgende Trivialnamen: a) für aliphatische Ketone: Aceton, Biacetyl1), Keten; b) für Ketone cyclischer Kohlenwasserstoffe mitSeitenketten: Acetophenon1), Benzil1), Benzophenon1), Chalcon1), Propiophenon1); c) für isocyclische Ketone: Acenaphthochinon, Anthrachinon, Benzochinon, Naphthochinon; d) für heterocyclische Ketone: Alloxan1), Barbitursäure, Chinolon2), Hydantoin, Isochinolon2), Pyrrolidon2); für das Thioketon: Rhodanin.
Eine Reihe von Stoffklassen, die sich von Carbonyl-Verbindungen ableiten, sind in Tab. 13 zusammengestellt.
C VII 6) Carbonsäuren. Die Umwandlung einer
-CH3-Gruppe in eine -COOH-Gruppe wird durch das Suffix -säure am Namen der entsprechenden Ausgangsverbindung ausgedrückt.
1) Nur für die unsubstituierte Verbindung.
2) Abgekürzte Form der systematischen Endung -idinon.
Nomenklatur. Tab. 13: von Carbonsäuren abgeleitete Stoffklassen.
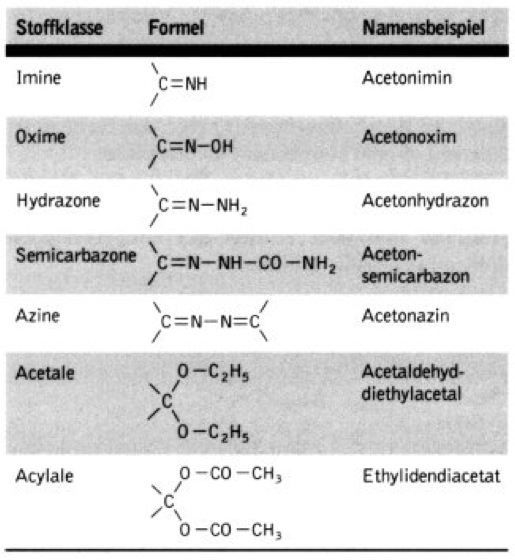
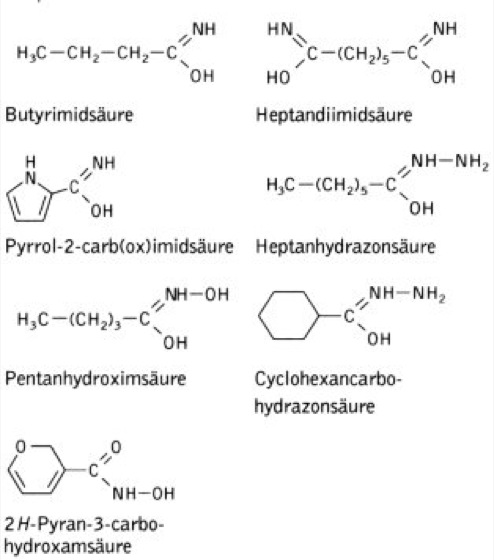
Die direkt am Verbindungsstamm gebundene -COOH-Gruppe heißt -carbonsäure. Erlaubt sind nur folgende Trivialnamen
a) für gesättigte aliphatische Monocarbonsäuren: Ameisensäure, Essigsäure, Propionsäure, Buttersäure, Isobuttersäure, Palmitinsäure, Stearinsäure; b) für gesättigte aliphatische Dicarbonsäuren: Oxalsäure, Malonsäure, Bernsteinsäure, Glutarsäure, Adipinsäure; c) für ungesättigte aliphatische Carbonsäuren: Acrylsäure, Propiolsäure, Methacrylsäure, Ölsäure; d) für isocyclische Carbonsäuren: Benzoesäure, Phthalsäure, Isophthalsäure, Terephthalsäure, Naphthoesäure (zwei Isomere), Zimtsäure; e) für heterocyclische Carbonsäuren: Furoesäure, Nicotinsäure, Isonicotinsäure;
f) Säurederivate können unter Verwendung modifizierender Silben (Infixe) benannt werden (s. Tab. 14 mit Beispielen).
C VII 7) Nitrile. Die Namen werden aus dem gegebenenfalls lat. Wortstamm der entsprechenden Carbonsäure und dem Suffix -onitril oder aus dem Namen des entsprechenden Kohlenwasserstoffs und dem Suffix -nitril gebildet, die direkt an einen cyclischen Verbindungsstamm gebundene -C≡N-Gruppe nennt man -carbonitril, z. B. Acetonitril oder Ethannitril, Thiophen-2-carbonitril.
C VII 8) Amine. Namen für primäre Amine werden aus dem Stamm- oder Restnamen des entsprechenden Kohlenwasserstoffs und dem Wort -amin gebildet. Sekundäre und tertiäre Amine werden als deren Substitutionsprodukte benannt, z. B. Hexan-2-amin oder 1-Methyl-pentylamin. Erlaubte Trivialnamen sind: Anilin, Toluidin (3 Isomere), Benzidin (nur 4,4'-Isomeres).
Nomenklatur. Tab. 14: Infixe für die Benennung von Säurederivaten.

1) Das in Klammern gesetzte C-Atom ist im Namensstamm der Säure eingeschlossen.
Beispiele:
C VII 9) Azo-Verbindungen werden a) systematisch als Substitutionsprodukte von Diazen benannt. Als Alternative können symmetrische Verbindungen durch Nennen von Azo- für die -N=N--Gruppe vor dem (nicht verdoppelten) Namen des unsubstituierten Stammoleküls, unsymmetrische Azo-Verbindungen aus den Namen der unsubstituierten Stammmoleküle (das komplexere zuerst) und dem Infix -azo- bezeichnet werden.
Beispiele:
C VII 11) Diazonium- und verwandte Verbindungen. a) Namen der die Gruppierung RN2+X- enthaltende Verbindungen werden aus dem für RH, dem Infix -diazonium- und dem Namen des Ions X- gebildet, z. B. C6H5-N2+Cl- Benzendiazonium-chlorid. b) Namen für Verbindungen mit der Gruppe RN=NX werden systematisch als Substitutionsprodukte von Diazen oder traditionell aus dem für RH, dem Infix -diazo- und der Bezeichnung für das Atom oder die Gruppe X gebildet, z. B. C6H5-N=N-OH Phenyldiazenol oder Benzendiazohydroxid. c) RN=N-O-M+ werden als Metalldiazenolate oder als Metalldiazotate bezeichnet, z. B. C6H5-N=N-O-Na+ Natrium-phenyldiazenolat oder Natrium-benzendiazotat. d) Die an ein Kohlenstoffatom gebundene N2-Gruppe wird mit dem Präfix Diazo- ausgedrückt, z. B. H2CN2 Diazomethan.
C VII 12) Organoschwefelverbindungen. a) Verbindungen mit zweiwertigem Schwefel. a1) S-Analoga von Verbindungen mit O-Funktion werden durch Verwendung von Thio- zusammen mit deren Namen bezeichnet. Mehrfacher Ersatz von O durch S wird durch ein Zahlwortpräfix angegeben, z. B. HS-CH2-CH2-SH Dithioethylenglycol, H3C(CH2)4CSSH Hexandithiosäure. Bei Thiocarbonsäuren unterscheidet man -thio-S-säure (-COSH) und -thio-O-säure (-CSOH). Der Name Thiophenol ist nicht mehr erlaubt. a2) Thiole und verwandte Verbindungen werden unter Verwendung der in Tab. 15 zusammengestellten Suffixe bzw. (bei Vorkommen einer anderen Hauptgruppe) Präfixe benannt. Beispiele: H3C-CH2SH Ethanthiol (substitutive N.), Ethyl-hydrosulfid (radikofunktionelle N.), Ethylsulfan (Hydrid-N.); der Name Ethylmercaptan ist nicht mehr erlaubt, HS-C6H4-COOH p-Sulfanyl-benzoesäure. b) Verbindungen mit vier- und sechswertigem Schwefel. b1) Säuren des Schwefels mit direkt am S-Atom gebundenem organischem Rest werden unter Verwendung der in Tab. 16 aufgeführten Affixe benannt, z. B. C6H5-SOH Benzensulfensäure, HOSO2-C6H4-COOH 4-Sulfo-benzoesäure; Ausnahme: Sulfanilsäure. Die Namen der Reste werden mittels -sulfonyl- (-SO2-) oder -sulfinyl- (-SO-) gebildet: H3C-SO- Methylsulfinyl-.
Nomenklatur. Tab. 15: Suffixe und Präfixe für charakteristische Gruppen mit zweiwertigem Schwefel.
4) Der Name -thioether ist nicht mehr erlaubt.
5) Das Präfix Thiono- ist nicht mehr erlaubt.
Ausnahmen: Tosyl- (nur für das p-Isomere), Mesyl-. b2) Säuren des Schwefels und deren Derivate mit nur über Sauerstoff an das S-Atom gebundenem Rest werden als Ester der entsprechenden Säuren (vgl. B V 2) bezeichnet. In der englischsprachigen Literatur wird die Ableitung vom Anionnamen nach der binären Nomenklatur bevorzugt: H3C-O-SO2-O-CH3 Schwefelsäuredimethylester oder Dimethyl-sulfat. Die Namen für über O oder N gebundene Reste werden aus den Präfixnamen ihrer Struktureinheiten zusammengesetzt oder durch Anhängen von -o an den Anionnamen gebildet: HO-SO2-O- Hydroxysulfonyloxy- oder Sulfato-. Zunehmend bevorzugt wird die Benennung der Sultone und Sultame als Heterocyclen:

C VII 13) Organoselen- und -tellurverbindungen werden analog den entsprechenden Schwefelverbindungen benannt, indem die Silbe sulf- und thi- durch selen- bzw. tellur- ersetzt wird, z. B. H5C2-Se-CH2-COOH Ethylselenoessigsäure, H5C2-Te-C2H5 Diethyltellurid.
C VII 14) Sonstige Organoelementverbindungen wurden bisher nicht nur international, sondern auch im nationalen Bereich nach unterschiedlichen Methoden benannt. 1973 wurden diese von der IUPAC zusammengefaßt und als vorläufige Regeln zur Benennung von organischen Verbindungen, die nicht ausschließlich aus Kohlenstoff, Wasserstoff, Sauerstoff, Stickstoff, Halogen, Schwefel, Selen und Tellur bestehen, veröffentlicht.
Nomenklatur. Tab. 16: Suffixe und Präfixe für die charakteristische Gruppe von Sauerstoffsäuren des Schwefels mit direkt an Schwefel gebundenem organischem Rest.

Danach erfolgt die Bezeichnung als Derivate der Hydride, Säuren oder nach der Nomenklatur für Koordinationsverbindungen. a) Organometallverbindungen, in denen das Metallatom nur an organische Reste und Wasserstoff gebunden ist, werden durch Zitieren der Reste in alphabetischer Reihenfolge vor dem Namen des Metalls bezeichnet. Wasserstoff muß immer mit dem Präfix Hydrido genannt werden: (C10H9)ReH2 (Dihydronaphthyl)dihydridorhenium. Alternativ ist die Benennung als Substitutionsprodukt der entsprechenden Hydride möglich: (C2H5)4Pb Tetraethylblei oder Tetraethylplumban. Metallocene (s. B VII 5. b) Organophosphorverbindungen und ihre Arsen-, Antimon- und Bismutanaloga werden als Derivate der Hydride (s. B II 3), der Säuren (Phosphorsäure, Arsensäure; Phosphinigsäure, Arsinigsäure; Phosphonigsäure, Arsonigsäure; Phosphorigsäure, Arsenigsäure) oder als Koordinationsverbindungen benannt, z. B. (C6H5)2PCl Chlordiphenylphosphin, Diphenylphosphinigsäurechlorid oder Chlorodiphenylphosphor; C6H5BiCl2 Dichlor(phenyl)bismutin oder Dichloro(phenyl)bismut. c) Organoborverbindungen. Die N. dieser Verbindungsklasse baut auf der der Borhydride auf. Der Name von BH3 ist Boran, auch die höheren Borhydride werden Borane genannt. Die Anzahl der Boratome wird durch ein vorgesetztes griech. Zahlwort angegeben (Ausnahmen: nona und undeca sowie icosa). Die Anzahl der vorhandenen Wasserstoffatome wird durch eine dem Namen in Klammern nachgestellte (arabische) Zahlenangabe angezeigt: B4H10 Tetraboran(10), B20H16 Icosaboran(16). Polyborane, in denen Skelettatome durch andere Elemente ersetzt sind, werden als Heteroborane bezeichnet: B10C2H12 Dicarbadodecaboran(12). Substitutionsprodukte, Reste u. dgl. werden wie üblich benannt: (H3C)3B Trimethylboran, -HB-BH- Diboran(4)-1,2-diyl-. Zur Borhydridstruktur s. Borane.
C VIII) Spezielles. 1) Ketten und Ringe a) mit regelmäßigen Folgen von Heteroatomen werden bei Verwendung entsprechender "a"-Terme (Ausnahme: Borane, Abschn. C VII 14c) analog den Kohlenwasserstoffen benannt, z. B. HS-S-S-SH Tetrasulfan, H2N(NH)7NH2 Nonaazan. b) Für unregelmäßige Folgen von Heteroatomen werden in Kürze auf "y"-Termen basierende Regeln veröffentlicht. Eine Kettenstruktur gibt die Endung -catena, eine cyclische Struktur die Endung -cyclus an.
C VIII 2) Namen für Radikale aus Kohlenwasserstoffen entsprechen denen der Reste. Für Sauerstoffradikale wird die Endung -oxy in -oxyl geändert. Stickstoffradikale werden benannt, indem -yl bzw. -ylen an den Namen der Base angehängt wird. Beispiele: H3C· Methyl, H3C-CH2-O· Ethoxyl, (H3C)2N· Dimethylaminyl, H3C-N: Methylaminylen.
C VIII 3) Kationen (vgl. B III 1), die formal durch Anlagerung von Hydronen an ein Heteroatom entstehen, werden unter Verwendung von -ammonium, -oxonium, -sulfonium, -selenonium, -telluronium, -chloronium, -bromonium, -iodonium (Präfixe: Ammonio-, Oxonio-, Sulfonio-, Selenonio-, Telluronio-, Chloronio-, Bromonio-, Iodonio-) benannt, z. B. [(H3C)4N]+ Tetramethylammonium-, [(H3C)2S(CH2)6N(CH3)3]2+Cl2- Trimethyl[6-(dimethylsulfonio)hexyl]ammonium-dichlorid. Ist das Heteroatom im Namen der Stammverbindung genannt, oder entsteht das Kation durch Anlagerung von Hydronen an einen ungesättigten Kohlenwasserstoff, so wird die Silbe -ium angehängt, z. B. [(H2N)3C]+ Guanidinium- bzw. [C2H5]+ Ethenium-. Namen für formal durch Abspaltung von Elektronen von einem Radikal bzw. Hydrid-Ionen von einem Stammhydrid erhaltene Kationen werden aus dem Radikalnamen und dem Wort Kation bzw. aus dem Stammnamen und der Endung -ylium gebildet, z. B. +CH2-CH2+ Ethan-1,2-(bis)ylium bzw. Ethylen-dikation (für H3C+ kann Carbenium- verwendet werden). Radikalkationen (Kationradikale) erhalten die Endung -iumyl, z. B.
[C2H6]·+ Ethaniumyl-, +CH4-CH2· Ethan-2-ium-1-yl.
C VIII 4) Anionen (vgl. B III 2), die durch Verlust eines Hydrons aus der charakteristischen Gruppe von Säuren oder Alkoholen entstehen, werden durch Ändern von -säure in -oat oder -at bzw. -carbonsäure in -carboxylat und von -ol in -olat (oder -oxid) oder -thiol in -thiolat (oder -sulfid) benannt. Die Endung -id wird bei Stammhydridanionen, die durch Verlust eines Hydrons entstanden sind, an den Stammnamen angehängt; leiten sie sich formal durch Addition eines Hydrid-Ions ab, so wird die Endung -uid verwendet. Präfixnamen werden aus dem Anionnamen und -o gebildet. Beispiele: H3C-CH2-O- Ethanolat, [Na+]2[O3S-C6H4-COO]2- Dinatrium-(4-sulfonato-benzoat), (H3C)2CH- Propan-2-id, H4B- Boranuid. Ausnahme: Die Salze des Acetylens werden weiter als Acetylide bezeichnet. Radikalanionen (Anionradikale) erhalten die Endung -yl am Anionnamen, z. B. [C2H4]·- Ethanidyl oder Ethenuidyl.
C VIII 5) Bei Verbindungen mit zwei oder mehr ionischen Zentren gleicher Ladung muß ein Strukturelement als Präfix genannt werden. Für Kationen gilt die Rangfolge Carbeniumionen, Heterokationen nach der Liste der "a"-Terme (Tab. 10), cyclische vor acyclischen Strukturen; für Anionen gilt die für charakteristische Gruppen festgelegte Priorität (Tab. 4), z. B.

C VIII 6) Die Namen für Verbindungen mit zwei oder mehr ionischen Zentren verschiedener Ladung werden gebildet, a) indem entweder das kationische Strukturelement als Präfix vor dem Anion oder das anionische Strukturelement als Suffix am Namen des Kations genannt wird, z. B.

b) Zwitterionische Verbindungen mit den ionischen Zentren in einer Struktur werden durch Kombinieren der entsprechenden Suffixe (Tab. 4) am Ende des Namens eines neutralen oder ionischen Stammhydrids in der Reihenfolge -ium, -ylium, -id und -uid benannt, z. B. (H3C)2-N+-N--CH3 1,2,2,2-Tetramethyldiazan-2-ium-1-id oder 1,2,2,2-Tetramethylhydrazin-2-ium-1-id.
C VIII 7) Isotop modifizierte Verbindungen. Von der IUPAC wurde 1981 ein allgemeines Nomenklatursystem für Verbindungen, deren Nuclidzusammensetzung von der natürlichen abweicht, veröffentlicht. (Die "natürliche Zusammensetzung" wird in der von der IUPAC in zweijährigen Abständen veröffentlichten Liste der relativen Atommassen definiert.)
Nomenklatur. Tab. 17: Zusammenstellung der Typen von isotop modifizierten anorganischen Verbindungen.
|
Nomenklatur. Tab. 18: Zusammenstellung der Typen von isotop modifizierten organischen Verbindungen.
|
Die eindeutige Benennung erfolgt durch Angabe von Art sowie gegebenenfalls Position und Anzahl der markierenden Nuclide entweder vor dem Gesamtnamen oder besser vor der Bezeichnung des markierten Teils der Verbindung. Es wird zwischen isotop unmodifizierten, isotop modifizierten (eingeteilt in isotop substituierte und isotop markierte, letztere wieder in spezifisch, selektiv oder nichtselektiv markierte) und isotop abgereicherten Verbindungen unterschieden. Zur Kennzeichnung der allgemeinen oder einheitlichen Markierung werden vor dem Namen für anorganische Verbindungen die Silben gen oder unf, für organische Verbindungen die Großbuchstaben G oder U verwendet. Am Symbol für metastabile Nuclide wird die Massenzahl durch ein m ergänzt: 133mXe. Die verschiedenen Typen von Formeln und Namen sind in den Tab. 17 und 18 zusammengestellt.
D) Geschichtliches. Die historische Entwicklung der N. kann nicht losgelöst von der der Symbole und Formeln betrachtet werden. In den ältesten Zeiten erfolgte die Benennung der Substanzen regellos und willkürlich. Kenntnisse über deren Zusammensetzung und Struktur lagen nicht vor, wenn sich auch schon früh Vorstellungen über den Aufbau der Materie entwickelt hatten (Atomistik, Vier-Elementen-Lehre). Im 16. Jh. forderte Paracelsus, die "Alchimie speculativa" durch die Deutung naturwissenschaftlicher Phänomene zu ersetzen. Die frühe N. war schwerfällig, für die gleiche Substanz gab es mehrere Trivialnamen. Im 17./18. Jh. verlangte das sich ständig erweiternde Wissen eine Regelung der Nomenklatur. Es gab mehrere Versuche, eine systematische N. zu entwickeln (Bergman, Macquer, Guyton de Morveau u. a.). Am 18. April 1787 trug Lavoisier vor der Akademie in Paris über eine planmäßige Benennung der (anorganischen) Substanzen vor. Zu dieser neuen N. schlugen Hassenfratz und Adet ein neues System von Symbolen vor, das als direkter Vorläufer der Elementsymbole von Berzelius (1814) angesehen werden muß; die früheren Symbole (Boyle, 1661; Stahl, 1697; Geoffroy, 1718; Bergman, 1775; Dalton, 1808) hatten sich als unzweckmäßig erwiesen.
Die sich entwickelnden Theorien (dualistische, elektrochem. Theorie; Substitutionstheorie; Radikaltheorie; Typentheorie u. a.) waren Grundlage für die Systematik der Stoffklassen und Benennung von Einzelverbindungen (Berzelius, 1820; Liebig, Wöhler, 1832; Dumas, 1834; Gerhardt, 1839) und fanden ihren Niederschlag in den verschiedenen Nomenklaturprinzipien, die durch spezielle Regeln unter anderem zur Benennung von poly- und heterocyclischen Verbindungen (Hantzsch, 1886; Widman, 1888; erweitert von Bredt, 1896; Baeyer, 1900; Stelzner, 1921; Patterson, 1925) ergänzt wurden. Mit der Aufstellung des Periodensystems der Elemente (Mendelev, Meyer, 1869), der Entwicklung der Strukturchemie und Strukturformeln (Cuper, 1858; Butlerov, 1861; Kekulé, 1865) wurden die Voraussetzungen für eine Reform der N. organischer Verbindungen geschaffen (Internationaler Chemiker-Kongreß, Paris, 1889, Genfer Nomenklatur, 1892). Wegen der "Unvollständigkeit" der Regeln (cyclische Verbindungen wurden nur kurz, heterocyclische Verbindungen wurden gar nicht behandelt) und von z. T. unbegründeten Einwänden wurde von der IUPAC 1921 eine Kommission für die N. der Organischen Chemie gegründet, die auf der N.-Konferenz in Lüttich, 1930, anstelle der Stammverbindung (Genfer N.) die "funktionelle Gruppe", d. h. den veränderlichsten Teil der Verbindung zur Grundlage der Benennung bestimmte und die Notwendigkeit einer offiziellen, d. h. Register-N. in Frage stellte. Die Arbeit der folgenden N.-Konferenzen (Luzern, 1936; Rom, 1938) waren wieder auf die Schaffung offizieller Namen ausgerichtet. Für anorganische Verbindungen stellte die Kommission für die N. der Anorganischen Chemie (gegründet 1921) 1938 Regeln auf, die 1940 veröffentlicht wurden. Die jetzt gültigen Regeln basieren auf der 1947 (London) beschlossenen Erweiterung und Revision. Das Regelwerk zur Benennung chem. Verbindungen wird durch Veröffentlichung von nach vorheriger öffentlicher Diskussion beschlossener neuer Regeln durch die einzelnen Nomenklaturkommissionen ständig aktualisiert und der Entwicklung der Chemie angepaßt.


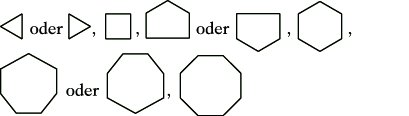





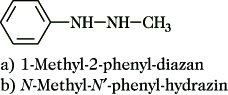

Wenn Sie inhaltliche Anmerkungen zu diesem Artikel haben, können Sie die Redaktion per E-Mail informieren. Wir lesen Ihre Zuschrift, bitten jedoch um Verständnis, dass wir nicht jede beantworten können.