Lexikon der Chemie: Phasendiagramm
Phasendiagramm, Zustandsdiagramm, Sammelbezeichnung für Diagramme, die die Phasenzusammensetzung von Ein- und Mehrstoffsystemen in Abhängigkeit von Druck, Volumen, Temperatur, Zusammensetzung oder Entropie wiedergeben. Durch die Gleichgewichtskurven der entsprechenden Phasenumwandlungen werden die Existenzbereiche der verschiedenen Phasen voneinander abgegrenzt. Die Anzahl der koexistierenden Phasen wird durch das Phasengesetz von Gibbs beschrieben. Als experimentelle Methoden zur Anfertigung von P. dienen Gleichgewichtsmessungen. Zu den P. gehören p,T-, p,V- und T,S-Diagramme, Dampfdruck-, Siede- und Schmelzdiagramme.
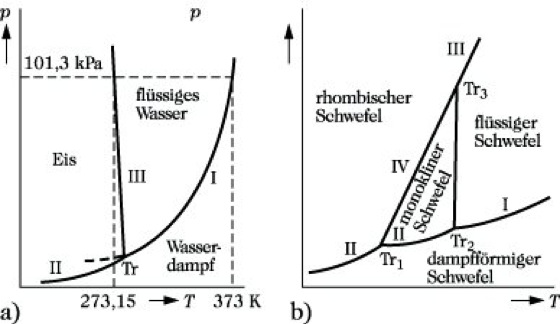
Phasendiagramm. Abb.: Phasendiagramme: (a) Zustandsdiagramm von Wasser (schematisch); I Dampfdruckkurve, II Sublimationskurve, III Schmelzdruckkurve, Tr Tripelpunkt. (b) Zustandsdiagramm von Schwefel (schematisch); IV Gleichgewichtskurve Smonokl.![]()
Srhomb.
Reine Stoffe. In P. reiner Stoffe werden die Gleichgewichtsdrücke p als Funktion der Temperatur T dargestellt. Die P. bestehen aus der Dampfdruckkurve (flüssig/gasförmig), der Sublimationsdruckkurve (fest/gasförmig) und der Schmelzdruckkurve (fest/ flüssig). Alle drei Kurven schneiden sich im Tripelpunkt (Abb. a). An diesem Punkt liegen alle drei Phasen nebeneinander im Gleichgewicht vor, d. h., er stellt den Schmelzpunkt beim Eigendampfdruck des reinen Stoffes dar. Für Wasser liegt er z. B. bei 273,15 K (0,0100 °C) und 610 Pa (4,58 Torr). Für alle drei Gleichgewichtskurven gilt die Clausius-Clapeyronsche Gleichung. Aus ihr folgt, daß der Schmelzpunkt für die meisten Stoffe mit dem Druck steigt und nur für wenige Ausnahmen (z. B. Wasser) sinkt. Für Atmosphärendruck (101,3 kPa) ist der Siedepunkt in Abb. a eingezeichnet. Die Dampfdruckkurve endet am kritischen Punkt. Die gestrichelte Verlängerung der Siedekurve unterhalb des Tripelpunkts entspricht dem Dampfdruck von unterkühltem Wasser, einem metastabilen Zustand. Existieren reine Stoffe in mehreren Modifikationen, so treten im P. zusätzlich die Gleichgewichtskurven der Phasenumwandlung und weitere Tripelpunkte auf (Abb. b).
Mehrstoffsysteme. Bei binären Mischungen, die aus zwei Stoffen bestehen, wird nach dem Phasengesetz von Gibbs die Zusammensetzung als weiterer Freiheitsgrad zur Beschreibung der Phasenzusammensetzung benötigt. Die vollständige Darstellung in der Ebene ist dann nicht mehr möglich. Als Schmelzdiagramm und Siedediagramm bezeichnet man die Abhängigkeit der Schmelz- bzw. Siedetemperatur von der Zusammensetzung, wobei der Druck konstant gehalten wird. Im Dampfdruckdiagramm wird der Dampfdruck von Mischungen bei konstanter Temperatur in Abhängigkeit von der Zusammensetzung dargestellt. Als Maß für die Zusammensetzung werden vorwiegend Molenbrüche bzw. Molprozente, aber auch Massenbrüche bzw. Masseprozente (Zusammensetzungsgrößen) verwendet.
P. von Mischungen mit mehr als zwei Komponenten erfordern spezielle Formen der Darstellung, z. B. Dreieckskoordinaten für ternäre Systeme.
Wenn Sie inhaltliche Anmerkungen zu diesem Artikel haben, können Sie die Redaktion per E-Mail informieren. Wir lesen Ihre Zuschrift, bitten jedoch um Verständnis, dass wir nicht jede beantworten können.