Lexikon der Chemie: Polymerisation
Polymerisation, chem. Reaktionstyp, bei dem zahlreiche Moleküle niedermolekularer Verbindungen (Monomere) über Kettenwachstumsreaktionen zu Makromolekülen (Polymere) vereinigt werden. Kennzeichen einer P. ist, daß die prozentuale Zusammensetzung der Elemente im Monomeren wie Polymeren die gleiche ist, daß sich also während des Polymerisationsvorganges keine Reaktionsprodukte abspalten wie bei der Polykondensation und keine Umlagerungen von Molekülgruppen stattfinden wie bei der Polyaddition. Die P. ist eine exotherme Reaktion, da das Polymerisat stets energieärmer als die ungesättigte Ausgangsverbindung ist. Zur Vermeidung von Explosionen muß die frei werdende Wärme abgeführt werden. Die Dichteunterschiede zwischen Monomerem und Polymerisat führen zur Volumenverkleinerung und werden zur Bestimmung der Umsatzrate genutzt. Ein Maß für die Anzahl der in einem Makromolekül vereinigten Monomeren ist der Polymerisationsgrad. Bei der P. können sich Moleküle der gleichen Art, aber auch verschiedene, ähnlich gebaute Substanzen zu Polymerisaten vereinigen. Bei der P. gleichartiger Moleküle (Homopolymerisation) unterschiedet man zwischen "Kopf-Schwanz"-Polymerisation, wenn sich die Monomeren der Form AB immer in der gleichen Lage AB-AB-AB-AB-AB zusammenlagern, und "Schwanz-Schwanz"- bzw. "Kopf-Kopf"-Polymerisation, wenn die Polymerkette die Orientierung AB-BA-AB-BA-AB- aufweist. Außerdem ist auch eine völlig unregelmäßige Reihenfolge wie etwa AB-AB-BA-BA-AB-BA- möglich.
Polymerisation. Tab.: Beispiele.
| ||||
| radikalisch | anionisch | kationisch | koordinativ | |
| Ethen | + | + | ||
| Propen | + | |||
| But-1-en | + | |||
| Isobuten | + | |||
| Buta-1,3-dien | + | + | + | |
| Isopren | + | + | + | |
| Styrol | + | |||
| Acrylnitril | + | + | ||
| Vinylchlorid | + | |||
| Acrylsäure- ester | + | |||
| Tetrafluor- ethylen | + |
Die P. ist eine Kettenwachstumsreaktion, die je nach Art des zugesetzten Katalysators nach einem radikalischen, koordinativen oder ionischen Mechanismus abläuft. Ausgelöst wird die P. durch eine Startreaktion; der weitere Aufbau der Polymerkette erfolgt durch eine Wachstumsreaktion, und durch Abbruchreaktionen wird der Kettenabbau beendet. Durch eine Übertragung des reaktiven Zustandes auf ein anderes Molekül kann die Kettenreaktion erneut gestartet werden.

Für die Bildung von Polymeren ist es notwendig, daß die Wachstumsreaktion sehr viel häufiger als die Übertragungs- und Abbruchreaktion auftritt. Unter Depolymerisation versteht man die zur Wachstumsreaktion gegenläufige Reaktion, d. h. die Abspaltung eines Monomeren aus dem aktivierten Polymeren. P. und Depolymerisation stehen miteinander im Gleichgewicht
Es bedeuten P*n+1 aktiviertes Polymeres und M Monomeres.
Für jedes Polymer-Monomer-Gleichgewicht gibt es eine bestimmte Grenztemperatur, bei der sich Kettenwachstum und Abspaltung im Gleichgewicht befinden und oberhalb der somit keine P. stattfinden kann (Ceiling-Temperatur).
Polymerisationsarten. (Beispiele s. Tab.) 1) Bei der radikalischen P. wird die Startreaktion durch ein Radikal ausgelöst. Die Radikale können entweder photochemisch, elektrochemisch, thermisch oder katalytisch durch radikalliefernde Initiatoren, z. B. Wasserstoffperoxid, Benzoylperoxid, Perborate, Persulfate, Azodiisobuttersäurenitril u. ä. gebildet werden. Die Kettenwachstumsreaktion der radikalischen P. beruht auf der Addition eines radikalischen Zwischenproduktes an die Doppelbindung eines Monomermoleküls (Abb. 1a). Bei der Übertragungsreaktion wird der radikalische Zustand des wachsenden Polymeren auf noch im System vorhandene Moleküle, z. B. nicht umgesetzte Monomere, Lösungsmittel, Initiator und Polymere, übertragen. Dabei verliert das Polymerradikal seine radikalische Eigenschaft (Abb. 1b). Die Abbruchreaktion erfolgt hauptsächlich durch Disproportionierung oder Kombination zweier Radikale (Abb. 1c).
Die radikalische P. liefert stets räumlich ungeordnete (ataktische) Polymere.
2) Bei der ionischen P. verwendet man ionische Katalysatoren, die mit den π-Elektronen der Monomerendoppelbindung eine Wechselwirkung eingehen.
Man unterscheidet zwischen anionischer und kationischer P. Bei der anionischen P. wird die Kettenwachstumsreaktion durch das Anion des Initiatormoleküls oder durch Übertragung eines Elektrons auf die Doppelbindung des Monomeren gestartet. Als Initiatoren werden Metallhydride, Natriumalkoholate, Natriumamid, tertiäre Phosphine, Grignard-Verbindungen u. a. eingesetzt (Abb. 2a). Während der Wachstumsreaktion reagiert ein Polymercarbanion mit dem Monomeren so lange, bis die Monomeren verbraucht sind oder die Reaktion durch Abbruchreaktionen beendet wird (Abb. 2b). In unpolaren Lösungsmitteln und bei der Substanzpolymerisation liegen bei der anionischen P. keine freien Ionen vor. Träger der Wachstumsreaktion sind hier polarisierte Metall-Kohlenstoff-Bindungen, die teilweise assoziiert sind (pseudoanionische P.). Die Komplexbildung bewirkt eine Lockerung der Metall-Kohlenstoff-Bindung und eine Aktivierung des monomeren Alkens. Die anschließende Einschubreaktion des Alkens wird als Insertionsreaktion und die auf diese Weise erfolgende P. als Insertionspolymerisation bezeichnet (Abb. 3). Die kationische P. wird durch Addition eines Kations an eine Doppelbindung gestartet. Als Initiator werden Protonensäuren und Lewis-Säuren eingesetzt (Abb. 4a). Das entstandene Carbenium-Ion kann sich durch Ladungsausgleich stabilisieren oder mit weiteren Monomeren reagieren (Abb. 4b). Bei der kationischen P. spielt der Ladungsausgleich zwischen den aktiven Kettenenden und dem Gegenion eine wichtige Rolle. Die Reaktionsgeschwindigkeit der ionischen P. steigt mit zunehmender Dielektrizitätskonstante des Lösungsmittels.

Polymerisation. Abb. 3: Insertionsreaktion.

Polymerisation. Abb. 4: Kationische Reaktion.
3) Träger des Kettenwachstums bei der koordinativen P. sind Übergangsmetallkomplexverbindungen, in deren Koordinationssphäre der Einbau des Monomeren in die wachsende Polymerkette erfolgt. Erster Schritt der Polymerisation ist die Bildung einer Metall-Kohlenstoff-Bindung, in die dann weitere Monomere eingebaut werden (Abb. 5). Die Übergangsmetallkomplexverbindungen werden aus Salzen der Übergangsmetalle der III. bis VIII. Nebengruppe, insbesondere der Halogenide von Titan, Vanadium, Chrom, Cobalt und Nickel, durch Alkylierung mit Metallalkylen der I. bis III. Hauptgruppe, vornehmlich der Aluminiumalkyle, hergestellt. Die koordinative P. hat große technische Bedeutung für die Herstellung von Polyethylen nach dem Niederdruckverfahren und für die Herstellung von Polypropylen. Butadien und Isopren werden mit Hilfe dieser Katalysatoren zu 1,4-cis-Polybutadien und 1,4-cis-Polyisopren (Kautschuk) polymerisiert. Verschiedene cyclische Monomere, z. B. Cyclopenten, Ethylenoxid, Caprolactam und cyclische Siloxane, lassen sich durch Ringöffnungspolymerisation zu Makromolekülen polymerisieren. Diese kann nach einem ionischen oder koordinativen Mechanismus als Stufen- oder Kettenwachstumsreaktion ablaufen (Abb. 6).

Polymerisation. Abb. 5: Koordinative Polymerisation.
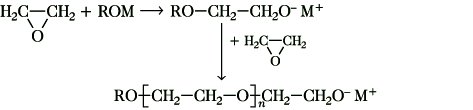
Polymerisation. Abb. 6: Ringöffnungsreaktion.
Als stereospez. P. bezeichnet man alle P., die zu räumlich geordneten Polymeren (isotaktische und syndiotaktische Polymere) führen. Diese entstehen bevorzugt bei der koordinativen und anionischen P.
Polymerisationshilfsmittel. Außer den oben angeführten Polymerisationskatalysatoren und Initiatoren können für den Polymerisationsprozeß noch Regler, z. B. Mercaptane, eingesetzt werden. Diese beeinflussen den Polymerisationsgrad und mit ihm Löslichkeit, Viskosität, thermoplastische Verarbeitbarkeit und mechanische Eigenschaften. Sie können z. B. nach einer bestimmten Kettenlänge Kettenabbruch oder auch Verzweigungen und Vernetzungen bewirken.
Polymerisationsverfahren. Bei der Blockpolymerisation (Massepolymerisation) werden flüssige Monomere ohne Zusatz von Lösungs- oder Dispersionsmitteln zu festen, meist hochmolekularen Polymeren umgesetzt. Bei der Lösungspolymerisation wird das Monomere in einem Lösungsmittel aufgelöst, in dem auch das entstehende Polymere löslich ist. Nach beendigter P. kann das Polymere durch Zugabe eines Lösungsmittels, von dem nur das Monomere gelöst wird, ausgefällt werden. Diese Form der P. hat den Vorteil, daß sich die entstehende Wärme leichter abführen läßt. Die nach diesem Verfahren erzielten Polymerisationsgrade sind nicht sehr hoch; sie sind abhängig von der Art und Menge des Lösungsmittels. Ist das Polymere im Lösungsmittel unlöslich und fällt während der P. aus, so spricht man von Fällungspolymerisation. Bei der Emulsionspolymerisation wird das Monomere mit Hilfe eines Emulgators in Wasser emulgiert und das Polymerisat ausgefällt. Als Startmittel dienen wasserlösliche Substanzen, als Emulgiermittel hauptsächlich Fettalkoholsulfonate. Wird das Monomere durch starkes Rühren in Form feiner Tröpfchen in einer nicht mischbaren Flüssigkeit verteilt, so spricht man von einer Suspensions-, Perl- oder Kornpolymerisation, da sich das Polymere in Perlenform abscheidet. Damit die monomeren Tröpfchen nicht verkleben, werden Suspensionsstabilisatoren oder Verteilungsmittel, wie wasserlösliche, organische Kolloide (z. B. Stärke, Gelatine oder synthetische Hochpolymere), zugesetzt. Die P. kann auch in der Gasphase erfolgen, z. B. beim Polyethylen. Bei dieser Gasphasenpolymerisation wird durch das im Kreislauf geführte Monomere ein Wirbelbett der Polymerkörner aufrechterhalten. Die Vorteile dieses Verfahrens bestehen darin, daß die Reaktionswärme leicht abgeführt werden kann und daß das Polymerisat in reiner, trockener Form anfällt. Einige kristalline Monomere, z. B. Trioxan, können auch im kristallinen Zustand polymerisieren. Dabei wird die P. im allg. durch energiereiche Strahlung ausgelöst. Um zu Polymerisaten mit besonderen gewünschten Eigenschaften zu gelangen, wendet man die Misch- oder Copolymerisation an; dabei geht man von einem Gemisch verschiedener Monomere aus. Eine besondere Art der Copolymerisation ist die Pfropfcopolymerisation (Graftcopolymerisation). Darunter versteht man die Aufpfropfung von Polymeren an bestehende Stammketten. Hierbei bestehen die Seitenketten aus anderen Monomeren als die Stammketten. Demgegenüber versteht man unter Blockcopolymerisation die Bildung von kettenförmigen Polymeren, in denen "Blöcke" oder "Sequenzen" gleicher Monomereinheiten die Kette bilden. So folgt z. B. auf einen "Block" aus dem Monomeren A ein solcher aus dem Monomeren B usw. Die einzelnen Blöcke werden durch getrennte P. der Monomere gewonnen und dann in einem zweiten Reaktionsschritt copolymerisiert.


Wenn Sie inhaltliche Anmerkungen zu diesem Artikel haben, können Sie die Redaktion per E-Mail informieren. Wir lesen Ihre Zuschrift, bitten jedoch um Verständnis, dass wir nicht jede beantworten können.