Lexikon der Chemie: Pyrolyse
Pyrolyse, ein Verfahren der Erdölverarbeitung zur Gewinnung niederer Alkene (Olefine) aus Erdölfraktionen (Cracken). Die Pyrolyseverfahren gehören zu den wichtigsten Verfahren zur Herstellung petrochem. Primärchemikalien.
Mitteltemperaturpyrolyseverfahren. Zur Erzeugung niederer Olefine, insbesondere von Ethen, Propen sowie der Butene und des Butadiens, sind vom Grundsatz her alle Kohlenwasserstoffe mit zwei oder mehr Kohlenstoffatomen geeignet. Die Ausbeute an Olefinen ist um so höher, je größer der Wasserstoffanteil des Ausgangsproduktes ist (Tab.). In den meisten Pyrolyseprozessen wird Leichtbenzin verwendet. Der Einsatz höherer Erdölfraktionen (z. B. Gasöl oder Schwerbenzin) ist stets mit einem Ausbeuteverlust an niederen Olefinen verbunden (Abb. 1).

Pyrolyse. Abb. 1: Ethenausbeute in Abhängigkeit vom C/H-Masseverhältnis des Einsatzproduktes.
Pyrolyse. Tab.: Produktverteilung in Abhängigkeit von der eingesetzten Kohlenwasserstoff-Fraktion.
| ||||||||||||||||
| Ethan | 825 | 3,0 | 7 | ,4 | 42 | ,9 | 37 | ,3 | 2 | ,3 | 0 | ,9 | 1 | ,1 | 4 | ,5 |
| Propan | 800 | 0,9 | 26 | ,4 | 32 | ,2 | 6 | ,8 | 11 | ,9 | 10 | ,8 | 3 | ,4 | 7 | ,4 |
| Leichtbenzin | 760 | 0,9 | 12 | ,7 | 24 | ,0 | 5 | ,0 | 19 | ,7 | 0 | ,5 | 9 | ,8 | 27 | ,2 |
| Schwerbenzin | 745 | 0,8 | 11 | ,7 | 22 | ,0 | 2 | ,3 | 11 | ,8 | 0 | ,6 | 10 | ,2 | 40 | ,4 |
Mechanismus. Oberhalb 700 °C beginnt mit einer für technische Belange ausreichenden Geschwindigkeit der Zerfall eines Paraffinkohlenwasserstoffs in zwei Radikale: R1-CH2-CH2-CH2-CH2-R2 → R1-CH2-CH2-CH2-CH2· + R2·. Unter Fragmentierung entsteht ein Olefin (z. B. Ethen) und ein um die Kettenlänge des Olefins kleineres Radikal (β-Spaltung): R1-CH2-CH2· + CH2=CH2 → R1-CH2-CH2-CH2-CH2· → R1-CH2· + CH2=CH-CH3 → R1· + CH2=CH-CH2-CH3. Die unimolekulare β-Spaltung eines Radikals ist mehrmals möglich, bis ein Radikal entsteht, das keiner β-Spaltung mehr zugänglich ist, z. B.

Das sehr reaktive Methylradikal geht bevorzugt eine bimolekulare C-H-Spaltung ein:
CH3· + R1-CH2-CH2-CH2-R2 →
CH4 + R1-C· H-CH2-CH2-R2.
Die unimolekulare β-Spaltung und die bimolekulare C-H-Spaltung sind die Träger der Kettenreaktion.
Disproportionierungsreaktionen und Radikalrekombinationen bewirken den Kettenabbruch, z. B.
R1· + R2-CH2· → R1-CH2-R2;
R1-CH2-CH2· + R1-CH2-CH2· → R1-CH=CH2 + R1-CH2-CH3.
Benzol wird unter diesen Bedingungen nicht gespalten, während die Benzolhomologen bevorzugt Benzylradikale ergeben, die zu unerwünschten Aufbauprodukten abreagieren, z. B. C6H5-CH2R → C6H5-CH2· + R·, 2 C6H5-CH2· → Tetrahydroanthracen + H2. Zur Unterdrückung dieser Aufbaureaktionen wird den zu pyrolysierenden Kohlenwasserstoffen Wasserdampf zugesetzt (Verdünnungseffekt).
Das Optimum der Spaltung von Kohlenwasserstoffen wird hauptsächlich bestimmt durch die Spalttemperatur, die Verweilzeit und den Kohlenwasserstoffpartialdruck. Die Herstellung von niederen Olefinen wird begünstigt durch hohe Temperaturen, kurze Verweilzeit und niedrigen Partialdruck. Hinsichtlich der Pyrolyseschärfe (severity) haben sich zwei Verfahrensweisen durchgesetzt, das Low-Severity-Cracken unterhalb 800 °C mit etwa 1 s Verweilzeit und das High-Severity-Cracken bei fast 900 °C mit etwa 0,5 s Verweilzeit.
Technische Pyrolyseverfahren. Die einzelnen Pyrolyseverfahren zur Herstellung niederer Olefine unterscheiden sich insbesondere durch die Art und Weise der Wärmezuführung und der Entfernung des abgelagerten Kokses.
Die meisten Pyrolyseanlagen arbeiten nach dem Prinzip der Röhrenofentechnologie (Abb. 2). Die Chrom-Nickel-Rohre stehen in modernen Röhrenöfen senkrecht und werden direkt durch Heizgas oder Heizöl auf etwa 1050 °C an den heißesten Stellen aufgeheizt,. Die heißen Spaltgase werden zur Vermeidung von Folgereaktionen in Quenchkühlern schnell auf etwa 300 °C abgekühlt (gequencht). In Abhitzekesseln wird das Spaltgas bis oberhalb des Taupunktes abgekühlt. Bei diesem Vorgang wird gleichzeitig hochgespannter Dampf erzeugt, der entscheidend zur Deckung des Energiebedarfs von Pyrolyseanlagen beiträgt. Die weiteren Verfahrensschritte sind Vortrennung in Gas und Kondensat, Reinigung des Rohgases von Schwefelwasserstoff, Kohlendioxid und Kohlenoxidsulfid durch Druckwäsche mit 5- bis 15%iger Natronlauge und Trocknung des Gasgemisches mit Hilfe von Molekularsieben, Aluminiumoxid oder Diethylenglycol.
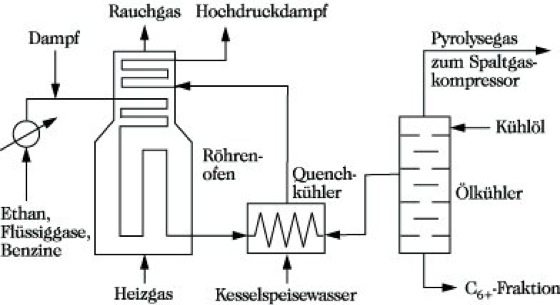
Pyrolyse. Abb. 2: Erzeugung niederer Olefine von Kohlenwasserstoffen im Röhrenofen.
Die Trocknung muß sehr sorgfältig vorgenommen werden, da es sonst in der sich anschließenden Tieftemperaturdestillationsstufe zur Abscheidung von Eis und Gashydraten kommen kann.
In einer nachgeschalteten Gastrennanlage wird das Spaltgas durch Tieftemperaturdruckdestillation in die einzelnen Komponenten zerlegt (Abb. 3). Die dafür notwendigen tiefen Temperaturen werden durch einen Kältemittelkreislauf aus Ethen (≈ -100 °C) und Propen (≈ -40 °C) erzeugt. Die bei der Produktkühlung auftretenden Kältemitteldämpfe (Ethen und Propen) werden erneut verflüssigt und wieder zur Kühlung eingesetzt. Die durch Destillation gewonnenen Produkte genügen den Qualitätsanforderungen der Nachverarbeitungsverfahren im Normalfall noch nicht. Insbesondere Ethin, Propin und Propadien stören in den jeweiligen Fraktionen. Durch selektive Hydrierung oder durch selektive Waschprozesse werden diese störenden Verunreinigungen entfernt.

Pyrolyse. Abb. 3: Tieftemperaturdruckdestillation des Pyrolysegases. Hydrierreaktionen für die selektive Hydrierung des Ethens und Propens.
Zur Deckung des Ethenbedarfs und zur Verbreiterung der Rohstoffbasis werden Verfahren entwickelt, um auch höhersiedende Erdölfraktionen (Siedebeginn oberhalb 250 °C) in die P. einzusetzen. Ein interessantes Verfahren ist das Kureha-Verfahren. Durch partielle Oxidation von entasphaltiertem Rohöl in einem Spezialreaktor wird bei Temperaturen bis 2000 °C in Gegenwart von Wasserdampf das Einsatzprodukt gespalten. Neben anderen Werkstoffen enthält das Spaltgas gleichzeitig Ethen und Ethin im Verhältnis 1 : 1.
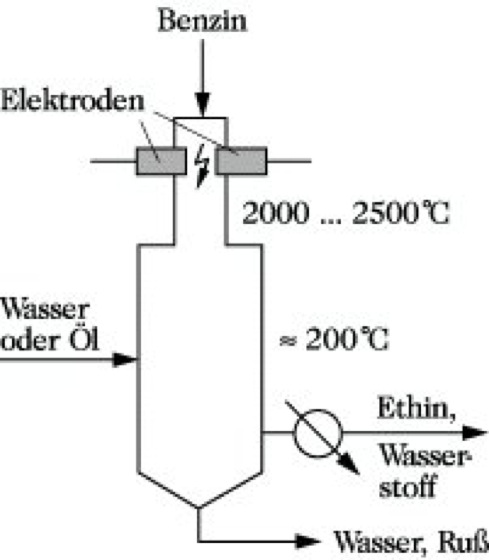
Hochtemperaturpyrolyseverfahren(HTP-Verfahren). Zielprodukt der Hochtemperaturpyrolysen ist das Ethin. Daneben entstehen niedere Olefine wie bei der Mitteltemperaturpyrolyse sowie Kohlenmonoxid und Wasserstoff, so daß diese Verfahren gleichzeitig Synthesegas liefern. Abb. 4 zeigt, daß mit steigender Temperatur der Unterschied hinsichtlich der Stabilität von Ethen und Ethin immer geringer wird. Oberhalb von 1300 °C ist Ethin stabiler als Ethen. Das ist der Grund dafür, daß man zur technischen Ethinerzeugung aus Kohlenwasserstoffen Temperaturen oberhalb 1500 °C benötigt. Zur Einbringung der hohen Reaktionswärme in den Reaktor arbeitet man mit gasförmigen Wärmeträgern oder im Lichtbogen. Als Verfahren kommen zur Anwendung die Verbrennung von Heizgas mit Sauerstoff (Abb. 5), die Wasserstoff-Lichtbogen-Pyrolyse, die Lichtbogenpyrolyse (Abb. 6) und der Tauchflammenprozeß, bei dem eine hochsiedende Erdölfraktion mit vorgeheiztem Sauerstoff umgesetzt wird; die sich dabei ausbildende Flammenfront taucht in das zu pyrolysierende Öl ein, dessen Temperatur auf etwa 200 °C gehalten wird.
Allen Verfahren ist gemeinsam, daß man in die heißen Verbrennungsgase oder in den Lichtbogen den Kohlenwasserstoff einbringt. Nach einer Verweilzeit von wenigen Bruchteilen einer Sekunde wird das Gas aus dem Reaktor herausgeführt und wegen des leichten Zerfalls des Ethins nach CH≡CH → 2 C + H2 sofort durch Einspritzen von Wasser oder Öl auf Temperaturen unter 200 °C abgekühlt (gequencht). Da bei der Hochtemperaturpyrolyse oberhalb von 2000 °C auch Aufbaureaktionen ablaufen, ist es möglich, Erdgas bzw. Methan einzusetzen und durch Dehydrodimerisierung zum Ethin zu gelangen:


Wenn Sie inhaltliche Anmerkungen zu diesem Artikel haben, können Sie die Redaktion per E-Mail informieren. Wir lesen Ihre Zuschrift, bitten jedoch um Verständnis, dass wir nicht jede beantworten können.