Lexikon der Chemie: Schmelzdiagramm
Schmelzdiagramm, ein Phasendiagramm, das den Zusammenhang zwischen dem festen und flüssigen Aggregatzustand, der Temperatur, der Anz Hl der koexistenten Phasen und den Konzentrationen der Komponenten angibt, wobei meist der Druck konstant gehalten wird. Die Schmelzkurven stellen somit Isobaren dar. Für alle S., die nur stabile Phasen berücksichtigen, gilt das Phasengesetz von Gibbs.
1. S. von Zweistoffsystemen (binäre Systeme)
1.1. S. von Systemen, bei denen sich die Komponenten im flüssigen Zustand gar nicht oder nur teilweise mischen lassen und im festen Zustand entweder nur beschränkt oder nicht mischbar sind. Solche Systeme sind relativ selten. Die Abb. 1 stellt ein Beispiel für ein System mit völliger Unmischbarkeit im flüssigen und festen Zustand unter Normalbedingungen dar. Im Phasenraum A liegen die beiden Flüssigkeiten heterogen nebeneinander vor. Bei der Schmelztemperatur S1 der ersten Komponente erstarrt die Gesamtmenge des Stoffs 1. Im Phasenraum B koexistieren also Kristalle des Stoffs 1 heterogen neben Schmelze des Stoffs 2. Bei der Schmelztemperatur S2 der zweiten Komponente erstarrt die gesamte Menge des Stoffs 2, so daß im Phasenraum C die beiden Kristallarten der beiden Stoffe heterogen nebeneinander vorliegen.
Die meisten Flüssigkeiten, die kurz oberhalb des Schmelzpunktes nicht oder nur teilweise mischbar sind, zeigen oberhalb der kritischen Entmischungstemperatur vollständige Mischbarkeit. Meist ist allerdings die kritische Entmischungstemperatur nicht bei Normaldruck zu erreichen, so daß bei erhöhtem Druck gearbeitet werden muß, um dem Verdampfen entgegenzuwirken.
1.2. S. von Systemen, bei denen die einzelnen Komponenten im flüssigen Zustand völlig mischbar sind. Diese sehr häufig vorkommenden Systeme unterscheiden sich nach dem Verhalten der festen Stoffe zueinander.
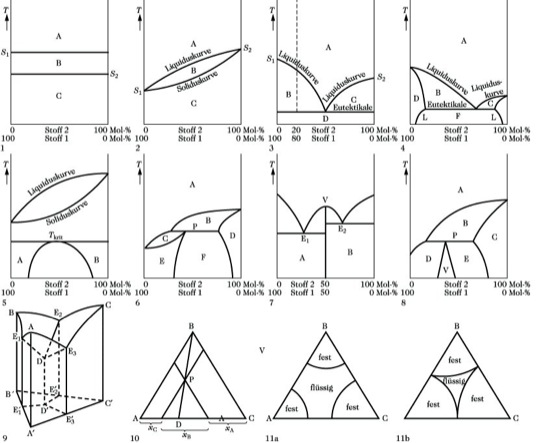
Schmelzdiagramm. Abb. 1 bis 11: Typen von Schmelzdiagrammen.
1.2.1. Völlige Mischbarkeit der Komponenten im festen Zustand (Abb. 2): Die Komponenten bilden in jedem Verhältnis miteinander Mischkristalle, z. B. das System Gold/Silber. Die Mischkristalle liegen im Phasenraum C vor. Im Phasenraum B, der durch die Schmelzpunkte S1 und S2 der Komponenten gekennzeichnet ist, stehen die Mischkristalle mit der homogenen Schmelze der beiden Komponenten im Gleichgewicht, während der Phasenraum A die im flüssigen Zustand ebenfalls völlig mischbaren Komponenten enthält. Der Phasenraum B wird von C durch die Erstarrungs- oder Soliduskurve (lat. solidus ›fest‹), von A durch die Löslichkeits- oder Liquiduskurve (lat. liquidus ›flüssig‹) getrennt.
Analog zu den Siedediagrammen kann auch bei den S. ein Maximum (z. B. das System Blei/Thallium) oder Minimum (z. B. das System Gold/Kupfer) auftreten.
1.2.2. Völlige Unmischbarkeit der Komponenten im festen Zustand; Bildung eines Eutektikums (Abb. 3): Der Phasenraum A enthält die in homogener Mischung vorliegenden flüssigen Komponenten. Bei S1 und S2 beginnt jeweils eine reine Komponente zu erstarren (kristallisieren), so daß die Schmelze ärmer an der auskristallisierenden Komponente wird. Entlang der Liquiduskurve S1 – E oder S2 – E kann die Zusammensetzung der Lösungen abgelesen werden, die sich bei verschiedenen Temperaturen mit dem Stoff 2 oder dem Stoff 1 im Gleichgewicht befinden. Man erreicht von beiden Seiten her schließlich die eutektische Temperatur. Die bei dieser Temperatur vorliegende Mischung bezeichnet man als Eutektikum. (Bei wäßrigen Salzlösungen spricht man von Kryohydrat und kryohydratischem Punkt). Am eutektischen Punkt liegen 4 Phasen vor: die beiden reinen Komponenten, die Schmelze und die gasförmige Phase der Komponenten, die wegen des immer vorhandenen Dampfdrucks aller Stoffe stets auftritt. Bei der eutektischen Temperatur erstarrt das Eutektikum wie ein reiner Stoff ohne Temperaturintervall. In den Phasenräumen B und C liegt jeweils eine reine feste Komponente zusammen mit der Mischschmelze im Gleichgewicht vor.
Wird z. B. eine Lösung, die 20 Mol-% des Stoffes 2 und 80 Mol-% des Stoffes 1 enthält, abgekühlt, so beginnt der Stoff 1 auszukristallisieren, wenn die Temperatur den Punkt a auf der Liquiduskurve S1 – E erreicht hat. Im Phasenraum D scheiden sich die Stoffe 1 und 2 in fester Form nebeneinander ab. Zu Systemen, die ein Eutektikum bilden, gehören z. B. Cadmium/Bismut, Blei/Antimon, Silber/Blei. Letzteres wird technisch genutzt, um Silber in Silber-Blei-Schmelzen anzureichern. Auch bei Kältemischungen spielt der eutektische Punkt eine Rolle.
1.2.3. Teilweise Mischbarkeit der einzelnen Komponenten im festen Zustand. Man unterscheidet bei diesen Systemen mit begrenzter Mischkristallbildung verschiedene Grundtypen:
1.2.3.1. Häufig bildet sich ein Eutektikum mit begrenzter Mischbarkeit in den Randgebieten, z. B. bei dem System Kupfer/Silber (Abb. 4). Im Phasenraum A liegen wieder die vollständig mischbaren Schmelzen vor, während die Räume D und E mit Mischkristallen der begrenzt mischbaren Komponenten erfüllt sind. Die Grenzkonzentrationen, bis zu denen die beiden Komponenten noch mischbar sind, werden durch die Schnittpunkte der Liquiduskurven mit der Eutektikalen gegeben. Die Gebiete B und C enthalten eine Schmelze mit je einer Mischkristallart im Gleichgewicht; das Eutektikum wird durch die beiden Mischkristallarten in ihrer jeweiligen Grenzkonzentration gebildet. Die Kurven L heißen Lösungslinien, da sie die Grenzen der Löslichkeit der beiden Stoffe ineinander bei jeder jeweiligen Temperatur angeben.
1.2.3.2. Systeme mit lückenloser Mischkristallbildung können bei tieferer Temperatur eine Entmischung unter Ausbildung einer Mischungslücke zeigen, z. B. das System Gold/Nickel (Abb. 5). Bei Temperaturerniedrigung zerfallen die Mischkristalle bei Erreichen der kritischen Temperatur Tkrit in ein Gemenge der beiden Mischkristallarten A und B.
1.2.3.3. Bei Systemen, bei denen die Mischungslücke bis in das Temperaturgebiet reicht, in dem die Mischkristalle aus der Schmelze gebildet werden (Abb. 6), entsteht ein Peritektikum P, bei dem die Mischkristallart E bei Erhöhung der Temperatur in Schmelze und die Mischkristallart D zerfällt. Im Gebiet F liegen die Mischkristalle E und D nebeneinander vor, während C und B die Mischkristallarten im Gleichgewicht mit der Schmelze enthalten. Im Phasenraum A liegen die vollständig mischbaren Schmelzen vor.
1.2.4. Systeme mit Verbindungsbildung (intermetallische Verbindungen): Sie werden unterteilt in kongruent schmelzende Verbindungen (Abb. 7), wobei die Verbindungen unzersetzt direkt in die Schmelze oder Lösung übergehen, und inkongruent schmelzende Verbindungen, die vor dem Schmelz- oder Lösungsvorgang in ihre Bestandteile zerfallen. Das S. einer kongruent schmelzenden Verbindung weist stets ein Maximum V auf. Es existieren hier 2 eutektische Punkte E1 und E2, wobei zu E1 der Stoff 2 und die Verbindung aus den beiden Stoffen und zu E2 der Stoff 1 und ebenfalls die Verbindung aus beiden Stoffen gehören. Jedes S. eines Systems mit kongruent schmelzenden Verbindungen kann in Teilsysteme A und B analog dem einfachen eutektischen System aufgegliedert werden.
Beispielsweise bilden die Systeme Bismut/Tellur und Natrium/Kalium kongruent schmelzende Verbindungen Bi2Te3 bzw. Na2K.
Systeme mit inkongruent schmelzenden Verbindungen bilden ein Peritektikum P (Abb. 8). Beim Erhitzen zerfällt die Verbindung V in Schmelze A und Mischkristalle C. Im Gebiet D liegt die Verbindung im Gleichgewicht mit der Schmelze A, im Gebiet E im Gleichgewicht mit den Mischkristallen C vor, während B die Mischkristalle C neben Schmelze A enthält.
2. S. von Dreistoffsystemen (ternäre Systeme). Diese S. können vollständig nicht mehr in der Ebene dargestellt werden, sondern nur noch durch räumliche Modelle. Abb. 9 zeigt ein solches in die Ebene projiziertes S. mit Eutektikum. Das Modell hat als Grundfläche ein gleichseitiges Dreieck A'B'C', dessen Ecken die reinen Komponenten darstellen sollen. Wenn man auf der Strecke A'B' (A'C', B'C') die Zusammensetzung der Mischung E1' (E3', E2') aus den Komponenten A und B (A und C, B und C) aufträgt, dann entsprechen die Seitenflächen AA'B'BE1AA'C'CE2 und CC'B'BE2des Raummodells den drei binären Systemen, die aus den drei Komponenten des ternären Systems gebildet werden können. In der Abb. 9 sind das drei einfache eutektische binäre Systeme mit den binären Eutektika E1, E2 und E3. Die äußeren Begrenzungsflächen der Figur enthalten also je zwei Komponenten, das Innere der Figur jedoch alle 3 Komponenten im Gleichgewicht miteinander. Der Punkt D wird ternäres Eutektikum genannt; er gibt die Zusammensetzung der am tiefsten schmelzenden ternären Mischung an (ablesbar aus der Projektion D' von D auf die Grundfläche).
Um die Konzentration eines beliebigen Punktes P zu ermitteln, projiziert man denselben auf die Grundfläche der Raumfigur (Abb. 10). Es werden dann die Parallelen zu den Dreiecksseiten durch P gezogen, wobei zwei beliebige Parallelen genügen, und bis zu den Schnittpunkten mit der nicht parallelen Dreiecksseite verlängert. Dann geben die den Ecken gegenüberliegenden Teilstrecken die Molenbrüche x der in der Mischung am Punkt P enthaltenen Komponenten A, B und C an, sofern man auf den Dreiecksseiten die Molenbrüche von Null bis Eins aufträgt. Entlang der Geraden BD ist das Verhältnis der Komponenten A zu C konstant, es ändert sich also nur das Verhältnis A zu B und B zu C. Zur teilweisen flächenhaften Darstellung ternärer Systeme schneidet man parallel zur Grundfläche Isothermen, also Flächen bei konstanter Temperatur, aus der Raumfigur (Abb. 11). Die im Inneren vorhandenen Linien ergeben dann die Teile der Begrenzungsflächen der einzelnen Phasenräume bei der dem isothermen Schnitt entsprechenden Temperatur; man kann sie mit den Höhenlinien einer Landkarte vergleichen. Die Temperatur in Abb. 11a ist höher gewählt als die in Abb. 11b (hier T2< T1), bei der bereits die Temperaturen der binären Eutektika unterschritten sind. Neben diesem einfachsten Typ eines S. eines Dreistoffsystems können kompliziertere ternäre Systeme kombiniert aus allen denkbaren binären Eutektika vorkommen.
Beispiele für ternäre Systeme mit Eutektikumsbildung sind Bismut/Blei/Zinn, Kaliumnitrat/Natriumnitrat/Lithiumnitrat, Kaliumcarbonat/Kaliumchlorid/Natriumfluorid; Beispiele für ternäre Systeme mit völliger Mischbarkeit der Komponenten sind Kupfer/Mangan/Nickel und Cäsiumchlorid/Rubidiumchlorid/Kaliumchlorid.
Wenn Sie inhaltliche Anmerkungen zu diesem Artikel haben, können Sie die Redaktion per E-Mail informieren. Wir lesen Ihre Zuschrift, bitten jedoch um Verständnis, dass wir nicht jede beantworten können.