Lexikon der Chemie: Thermogravimetrie
Thermogravimetrie, Abk. TG, thermoanalytische Methode zur Bestimmung der Änderung der Masse einer Substanz in Abhängigkeit von der Temperatur beim Erhitzen. Mit Hilfe der T. können die Verdampfungs-, Sublimations-, Desorptions-, Entwässerungs-, Zersetzungs- und Oxidationsvorgänge fester Substanzen untersucht werden. Auch analytische Probleme, z. B. die Bestimmung des Wassergehaltes lassen sich mit Hilfe der T. lösen. Ein wichtiges Anwendungsgebiet der T. ist die Untersuchung von Polymeren. Es lassen sich einerseits Aussagen über Zersetzungstemperaturen und Zersetzungsmechanismen machen, zum anderen charakteristische Thermogramme für unterschiedliche Polymere erhalten, die ihre Identifizierung erlauben.
Eine Apparatur für thermogravimetrische Analysen besteht aus folgenden Hauptbauelementen: 1) einer empfindlichen Thermowaage, die es erlaubt, die Masseänderung einer in einem Ofen befindlichen Probe kontinuierlich zu verfolgen, 2) einer Heizung mit Temperaturprogramm, die einen linearen Temperaturanstieg mit einer vorgegebenen Geschwindigkeit (etwa zwischen 0,5 bis 25 °C/min) erlaubt, wobei Temperaturen bis etwa 1200 °C untersucht werden, 3) einem Thermoelement zur Temperaturmessung, das möglichst eng mit der Probe verbunden ist, 4) einer Registriereinrichtung, die das Thermogramm aufzeichnet, in dem die Masse der Probe als Funktion der Temperatur angegeben ist.
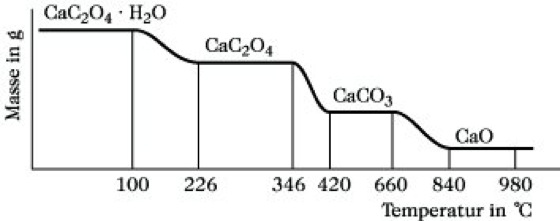
Thermogravimetrie. Abb. 1: Thermogramm der Zersetzung von Calciumoxalatmonohydrat.
Abb. 1 zeigt das Thermogramm, das von Calciumoxalatmonohydrat bei einem Temperaturanstieg von 5 °C/min erhalten wird. Die horizontalen Abschnitte der Kurve entsprechen Temperaturbereichen, in denen die angegebenen Verbindungen stabil sind. Dazwischen kommt es zu definierten Zersetzungen der Probe. Häufig wird die erste Ableitung des Thermogramms aufgezeichnet, die mitunter eine bessere Erkennung bestimmter Umwandlungspunkte erlaubt (Derivativ-Thermogravimetrie, DTG). Die T. kann auch zur quantitativen Analyse von Gemischen eingesetzt werden, wie es in Abb. 2 am Thermogramm von Calcium-, Strontium und Bariumoxalatmonohydrat dargestellt ist. Während der Übergang von den Hydraten zu den wasserfreien Verbindungen bei annähernd gleicher Temperatur erfolgt, wird bei weiterer Temperatursteigerung zuerst Calciumcarbonat, dann Strontium- und schließlich Bariumcarbonat zersetzt, was eine quantitative Bestimmung der vorliegenden Elemente erlaubt. Als Nachteil der T. muß angesehen werden, daß überlappende thermische Prozesse meist nur schwierig zu trennen sind.
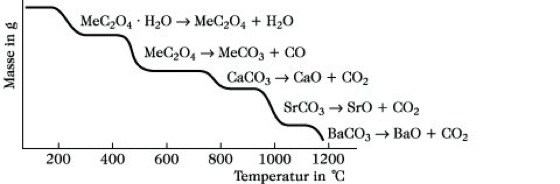
Thermogravimetrie. Abb. 2: Thermogramm der Zersetzung von CaC2O4·H2O, SrC2O4·H2O und BaC2O4·H2O.
Wenn Sie inhaltliche Anmerkungen zu diesem Artikel haben, können Sie die Redaktion per E-Mail informieren. Wir lesen Ihre Zuschrift, bitten jedoch um Verständnis, dass wir nicht jede beantworten können.