Lexikon der Chemie: Zustandssumme
Zustandssumme (Symbol Z oder Q), eine zentrale Größe in der statistischen Thermodynamik, die angibt, wie sich die Gesamtenergie eines Moleküls auf seine verschiedenen Freiheitsgrade verteilen
kann. Sie ist definiert durch die Beziehung 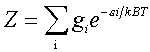
, wobei kB die Boltzmann-Konstante, T
die absolute Temperatur, εi einen definierten Energiezustand i und gi die Anzahl der Zustände mit gleicher Energie (Energieentartung) angibt. Die Summation erfolgt über alle Energiezustände. Mit Hilfe der Z. ist die Berechnung makroskopischer thermodynamischer Zustandsgrößen aus Moleküldaten möglich. So gelten z. B. folgende Zusammenhänge: U = RT2(d ln Z/dT); S = R ln Z + RT(d ln Z/dT) und F = -RT ln Z. Unter der Voraussetzung, daß sich die Gesamtenergie ε1 eines Moleküls additiv aus den Energiebeiträgen zusammensetzt, die in seinen einzelnen Freiheitsgraden gespeichert sind, ε1 = εtrans + εrot + εschw + εe1 + εKern, läßt sich die e-Funktion der Z. in ein Produkt von e-Funktionen und damit in Teilzustandssummen für diese verschiedenen Freiheitsgrade aufspalten: Z = Ztrans·Zrot·Zschw·Zel·ZKern. Für diese Teilzustandssummen gelten folgende Beziehungen: Zustandssumme Ztrans für 3 Translationsfreiheitsgrade:
Ztrans = h-3(2πmkBT)3/2V mit h = Plancksche Konstante, m = Molekülmasse, V = Volumen des Gases; Zustandssumme Zrot der Rotation des Moleküls: Zrot = h-2σ-1(8π2IkBT) für lineare Moleküle und Zrot = h-3 σ-1 π1/2·(8 π2kBT)3/2(IaIbIc)1/2 für nichtlineare Moleküle mit σ = Symmetriezahl (Zahl der Deckungsoperationen bei einer Drehung um 360°), I = Hauptträgheitsmoment des linearen Moleküls, Ia, Ib, Ic = Trägheitsmomente bezüglich der drei Drehachsen des Moleküls; Zustandssumme Zschw der Schwingung:

mit j = Numerierung der 3 N – 6 Schwingungsfreiheitsgrade und uj = hνj/kBT, wobei νj die Schwingungsfrequenz der j-ten Normalschwingung bezeichnet. Lineare Moleküle verfügen über 3 N – 5 Schwingungsfreiheitsgrade, so daß für sie j von 1 bis 3 N – 5 läuft.
Chem. Reaktionen verlaufen ohne Änderung der Kernzustände, thermische Vorgänge im allg. im elektronischen Grundzustand, so daß ZKern und Zel keinen Einfluß auf die gesamte Z. haben und deshalb ZKern = Zel = 1 gesetzt werden. Damit ermöglicht die Kenntnis der Moleküldaten m, I und aller νj die Berechnung der Z. und damit thermodynamischer Zustandsgrößen und Gleichgewichte.
Wenn Sie inhaltliche Anmerkungen zu diesem Artikel haben, können Sie die Redaktion per E-Mail informieren. Wir lesen Ihre Zuschrift, bitten jedoch um Verständnis, dass wir nicht jede beantworten können.