Lexikon der Geowissenschaften: Sauerstoffkreislauf
Sauerstoffkreislauf, Sauerstoffzyklus, geochemischer Kreislauf des Sauerstoffs. Sauerstoff gehört zu den Chalkogenen (Hauptgruppe VI A im Periodensystem der Elemente, zusammen mit Schwefel, Selen, Tellur und Pollonium); Oxidationsstufen sind –2 und selten auch –1 (z.B. bei Peroxiden H2O2 oder Sauerstofffluoriden O2F2). Sauerstoff hat einen kleinen Atomradius (0,74 Å), als O2-Anion dagegen einen sehr großen (1,40 Å). Die Ordnungszahl von Sauerstoff ist 8, es hat drei stabile Isotope (16O, 17O und 18O) mit den durchschnittlichen Häufigkeiten 99,76%, 0,037% und 0,20%, die aber durch Isotopenfraktionierungsprozesse verändert werden (18O/16O).
Die primordiale Erde hatte keine Atmosphäre. Erst im Zuge der Abkühlung und Ausgasung des neu entstandenen Planeten konnte eine Atmosphäre kondensieren. Sie war, abgesehen von primär entgastem Sauerstoff, praktisch sauerstofffrei, und erst per Photodissoziation von H2O durch die einfallende UV-Strahlung konnte sich freier Sauerstoff bilden. Dieser Prozeß ist selbstregulierend, da Wasser und Sauerstoff nahezu die gleichen Energiespektren der UV-Strahlung absorbieren. Mit steigender O2-Konzentration geht dadurch Energie zur O2-Bildung verloren (Urey-Effekt). Weiteres Regulativ waren die Pufferkapazität der Urozeane und der Sauerstoffverbrauch durch Oxidation (u.a. Bildung von gebänderten Eisenerzen (Banded Iron Formation) und terrestrischen Rotsedimenten). Mit dem zeitlich nicht genau definierten Einsetzten der mikrobiellen Sulfatreduktion im Archaikum könnte der Sauerstoffpegel der Atmosphäre deutlich angestiegen sein, aber erst durch die ›Erfindung‹ der Photosynthese konnte der Sauerstoffgehalt der Atmosphäre nennenswert steigen, mit Besiedelung des Festlandes bis in die Größenordnung heutiger Sauerstoffgehalte, wobei zu Zeiten extremer Photosyntheseaktivität (Bildung der Kohlenlagerstätten im Karbon) ein höherer Sauerstoffpartialdruck angenommen werden muß als der heutige PAL (Present Atmospheric Level).
Molekularer Sauerstoff (O2) dissoziiert unter Einwirkung von starker UV-Strahlung. Bei der Rekombination entsteht auch Ozon (O3). Diese natürliche, oberhalb der wasserdampfreichen Zone der Atmosphäre ablaufende Ozonbildung schützt terrestrische Lebensformen vor letaler UV-Strahlung. Zwischen Photosynthese (O2-Freisetzung aus CO2 und H2O) und Verbrauch von O2 durch Organismen (Atmung, postmortale Oxidation) hat sich ein Gleichgewicht eingestellt, das aber durch den erhöhten Verbrauch von O2 durch Verbrennen fossiler Energieträger bei gleichzeitiger Reduzierung der Sauerstoffproduktionsflächen (Regenwald) empfindlich gestört wird. Sauerstoff ist mit 20,99 % das zweithäufigste Element in der Atmosphäre; faßt man Lithosphäre und Hydrosphäre zusammen, so ist es mit 49,2 % Anteil häufigstes Element, gefolgt von Silicium, Aluminium und Eisen. Abgesehen von sauerstofffreien Salzen und Sulfiden ist es in Kombination mit Si und Al Hauptbestandteil vieler Silicatminerale. Auch als Oxid (z.B. mit Fe als Fe2O3 oder Ti als TiO2) oder Hydroxylion (OH-, z.B. FeOOH) bzw. Kristallwasser (H2O, z.B. CaSO4·2H2O) ist es oft zu finden. Als Reservoire und Austauschpartner für den geochemischen Sauerstoffkreislauf stehen neben Atmosphäre Hydrosphäre, Kruste und Teile des Erdmantels zur Verfügung ( Tab.). Der Sauerstoffaustausch zwischen den Reservoiren ( Abb. 1), aber auch der Sauerstoffaustausch zwischen Phasen innerhalb eines Reservoirs sind mit Fraktionierungsprozessen der Sauerstoffisotope verbunden. Einige Reservoirs zeigen eine charakteristische Bandbreite ( Abb. 2). Die ›Stärke‹ der Fraktionierung wird dabei als δ18O-Wert (Abweichung in Promille vom Standard 18O/16O-Isotopenverhältnis der Standards SMOW (Standard Mean Ocean Water) oder PDB (Peedee Belemnit-Standard) für Niedrigtemperaturfraktionierung) angegeben. Folgende Fraktionierungsmechanismen (nicht nur bei der Sauerstoffisotopie) werden unterschieden:
1) Temperaturfraktionierung: a) Hochtemperatur, als Kombination aus chemischer Bindungsstärke und physikochemischen Prozessen (Schmelzen, Kristallisation, Diffusion): z.B. Bildungstemperaturen von Mineralen in Magmatiten und Metamorphiten. b) Niedrigtemperatur: z.B. die Bestimmung von Diagenesetemperaturen von Sedimenten (Carbonate, Phyllosilicate). 2) Destillation (als kinetischer Effekt): z.B. die Verdunstung und Kondensation von Wasser in einem offenen System ( Abb. 3). 3) Biofraktionierung (ebenfalls ein kinetischer Effekt): z.B. Bestimmung von Paläowassertemperaturen an biogenen Calciten (Muschelschalen, Foraminiferen).
Verdunstung, Kondensation und Rückführung von Wasser in das Reservoir ›Ozean‹ werden durch das Klima beeinflußt. In Kaltzeiten wird das isotopisch ›leichte‹ Wasser als Eis in Gletschern fixiert und fließt nur sehr langsam in das Meerwasserreservoir zurück. Dadurch wird das Ozeanwasser isotopisch immer ›schwerer‹. Organismen, die dem Wasser Sauerstoff entziehen, bilden (trotz zusätzlicher Biofraktionierung) diese veränderte Meerwasserisotopie im Calcit ihrer Gehäuse ab. Systematische Untersuchungen an Kernen aus Tiefseesedimenten und Eiskernen zeigen ein charakteristisches Muster und ermöglichen somit eine ›Sauerstoffisotopenstratigraphie‹ (nach Cesare Emiliani, einem Schüler von Urey auch als Emiliani-Kurve bzw. Emiliani-Stadien benannt). [WL]
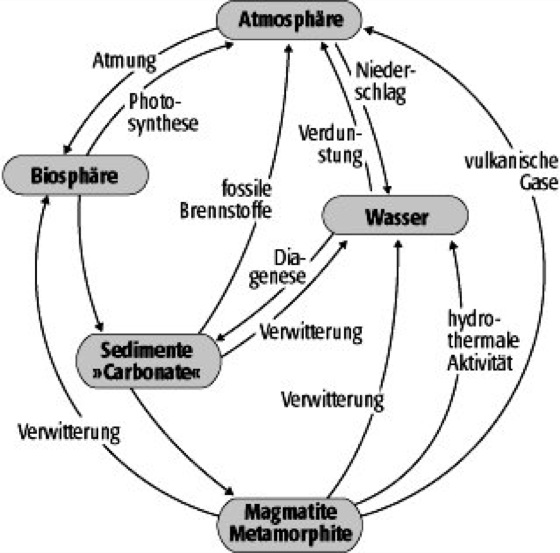
Sauerstoffkreislauf 1: der geochemische Sauerstoffkreislauf. Die einzelnen Reservoire zeigen eine charakteristische Bandbreite der Sauerstoffisotope. Sauerstoffkreislauf 1:
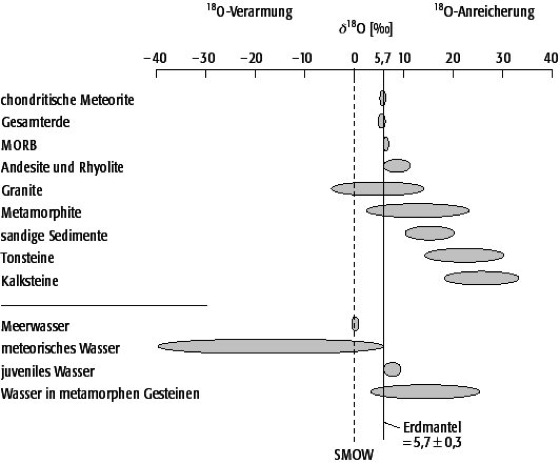
Sauerstoffkreislauf 2: Isotopie von Sauerstoffreservoire im Vergleich zum Erdmantel und SMOW (δ18O [0/00]). Sauerstoffkreislauf 2:
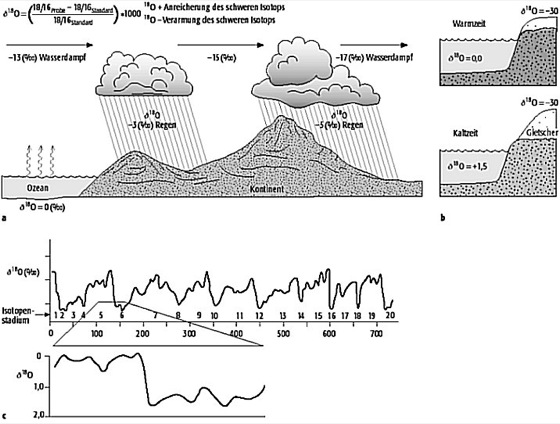
Sauerstoffkreislauf 3: a) Sauerstofffraktionierung durch Destillationsprozesse (Rayleigh-Fraktionierung) und b) ihre Langzeitauswirkung als Folge klimatischer Veränderungen. c) Sauerstoffisotopenstadien der vergangenen 700.000 Jahre. Sauerstoffkreislauf 3:
Sauerstoffkreislauf (Tab.): Sauerstoffmengen der Erde.

Wenn Sie inhaltliche Anmerkungen zu diesem Artikel haben, können Sie die Redaktion per E-Mail informieren. Wir lesen Ihre Zuschrift, bitten jedoch um Verständnis, dass wir nicht jede beantworten können.