Lexikon der Geowissenschaften: Wasserchemismus
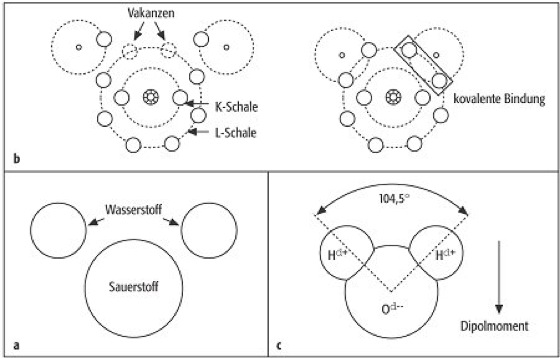
Wasserchemismus, Chemismus des Wassers als ein Stoff mit besonderen chemischen und physikalisch-chemischen Eigenschaften. Aus diesem Grund findet es eine vielfache Verwendung in allen Bereichen menschlicher Tätigkeiten. Zudem spielt es in der belebten und unbelebten Natur bei fast allen Vorgängen eine zentrale Rolle oder ist zumindest daran in irgendeiner Weise beteiligt. Die Ursache für die ungewöhnlichen Eigenschaften ist in der molekularen Struktur begründet. Das Wassermolekül (Monohydrol, H2O) besteht aus zwei Wasserstoffatomen (H) und einem Sauerstoffatom (O) ( Abb. 1a). Es wird durch die aus einem gemeinsamen Elektronenpaar bestehende kovalente Bindung zusammengehalten ( Abb. 1b). Das Molekül ist in der Form des Wasserdampfes existent. Es hat einen winkelförmigen Aufbau, wobei die Valenzbindungen vom Sauerstoff zu den beiden Wasserstoffatomen einen Winkel von 104,5º einschließen und einen O-H-Bindungsabstand von 0,096 nm aufweisen ( Abb. 1c). Der Moleküldurchmesser beträgt 0,275 nm, der Abstand zwischen den beiden H-Atomen 0,154 nm. Die Ionisierungsenergie des Moleküls beträgt 12,62 eV. Die relative Molekülmasse ist 18,01534. Sie ergibt sich aus der relativen Atommasse für 1H=1,00797 und für 16O=15,9994.
Der Schwerpunkt der Elektronen im Molekül liegt aufgrund dieser Struktur nicht zentral. Die unterschiedliche Elektronegativität von O- und H-Atomen führt zu Partialladungen von -0,34 am Sauerstoff- und je +0,17 an den beiden Wasserstoffatomen. Das Molekül weist daher ein positiv und ein negativ geladenes Ende auf und stellt damit einen Dipol mit einem Dipolmoment dar. Auf dem Dipolcharakter der Wassermoleküle beruhen viele der außergewöhnlichen chemischen und physikalischen Eigenschaften des Wassers, wie z.B. das gute Lösungsvermögen, die Viskosität, die Oberflächenspannung usw.
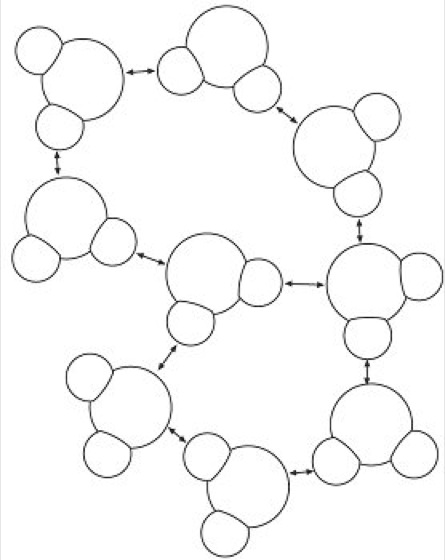
Das Kontinuum Wasser ist eine Verbindung von Monohydrolen ( Abb. 2). Die zwischenmolekulare Bindung erfolgt neben den van der Waalsschen Massenanziehungskräften über die positiven und negativen freien Ladungen am Wassermolekül. Der negative Pol des einen zieht den positiven Pol des anderen Hydrols an. Diese elektrostatische Bindung wird als Wasserstoffbrückenbindung bezeichnet. Sie ist viel stärker als die van der Waalssche Massenanziehung und bewirkt die Entstehung von Molekülaggregaten (H2O)x (Polyhydrole). In ihnen sind die Wassermoleküle zu einem Verband von ungewöhnlicher Dichte und Kontinuität der Struktur verkettet. Mit steigender Temperatur werden die Molekülaggregate instabiler.
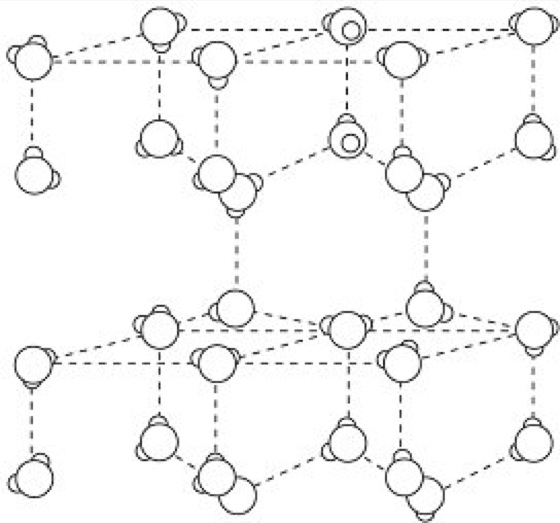
Beim Erstarren des Wassers bildet sich in der Natur Eis („normales” Eis, Modifikation „Eis I”). Darin sind, wie die Abbildung 3 zeigt, die Sauerstoffatome tetraedrisch angeordnet, die Wasserstoffatome bilden zu den umgebenden Sauerstoffatomen sowohl kovalente wie Wasserstoffbrückenbindungen aus. Insgesamt ergibt sich dadurch eine hexagonale Kristallstruktur mit zahlreichen Hohlräumen. Zugleich erfolgt eine Volumenvergrößerung und Dichteminderung (Wasser, mechanische Eigenschaften). Eine Elementarzelle hat eine Kantenlänge von 0,451 nm bzw. 0,735 nm. Neben der Normalform gibt es noch zahlreiche weitere Eismodifikationen, die unter Hochdruck oder bei tiefen Temperaturen entstehen können.
In der flüssigen Phase des Wassers sind nicht alle Wasserstoff- und Sauerstoffatome in Wassermolekülen gebunden. Es bestehen daneben noch geringe Mengen H+- und OH--Ionen. Die Aufspaltung eines Moleküls wie des Wassers in Ionen wird als Dissoziation bezeichnet. Aus dem ungewöhnlich großen Dipolmoment der Wassermoleküle und der sich daraus ergebenden hohen Dielektrizitätskonstante resultiert die beachtliche Fähigkeit des Wassers, andere Stoffe aufzulösen. Dies betrifft besonders solche Stoffe, deren Moleküle allein oder hauptsächlich durch Ionenbindung zusammengehalten werden. Eine solche Bindung entsteht aus der Coulombschen Anziehung, zum Beispiel wenn Na+- und Cl--Ionen sich gegenseitig anziehen und NaCl-Moleküle (Kochsalz) bilden. Diese Bindungen sind verhältnismäßig schwach. Wenn sie an der Oberfläche eines in Wasser getauchten Salzkristalls unterbrochen werden, wird die Anziehung zwischen den gelösten, entgegengesetzt geladenen Ionen durch die hohe Dielektrizitätskonstante stark vermindert. Die Trennung der Ionen (Dissoziation) wird zusätzlich dadurch gefördert, daß die positiven Ionen dazu neigen, sich an die negativ geladene Sauerstoffseite des H2O-Moleküls und die negativen Ionen sich an die positiv geladene Wasserstoffseite anzuhängen (Komplexierung durch Wassermoleküle, Hydratisierung). Durch diesen Vorgang ändert sich die zwischenmolekulare Struktur des Wassers erheblich. Nicht dissoziierende Substanzen sind gut in Wasser löslich, wenn ihre Moleküle ebenfalls ein Dipolmoment besitzen oder wenn sie unter Ausbildung von Wasserstoff-(H-)Brücken mit den Wassermolekülen in Wechselwirkung treten können. Der Lösungsvorgang ist mit Volumenkontraktion und Wärmeumsatz (positive oder negative Wärmetönung) verbunden.
In der Natur kommt Wasser in reiner Form praktisch nicht vor; es sind immer anorganische oder organische Stoffe in gelöster oder ungelöster Form in ihm enthalten. Wasser kann Stoffe verschiedenster Art (Feststoffe, Flüssigkeiten, Gase) lösen. Die Wasserinhaltstoffe können die ursprünglichen physikalischen und chemischen Eigenschaften des Wassers erheblich verändern (zum Beispiel Siedepunkt, Dichte, u.a.). Außerdem kann das Wasser Zwei-Phasen-Systeme mit Feststoffen (Suspensionen), mit Flüssigkeiten (Emulsionen) und mit Gasen (Schäume, Nebel) bilden. [HB]
Wenn Sie inhaltliche Anmerkungen zu diesem Artikel haben, können Sie die Redaktion per E-Mail informieren. Wir lesen Ihre Zuschrift, bitten jedoch um Verständnis, dass wir nicht jede beantworten können.