Lexikon der Neurowissenschaft: Farbensehen
Farbensehen s, Farbsehen, Ecolour vision, die Fähigkeit, mittels verschiedener Typen von Photorezeptoren Licht von unterschiedlicher spektraler Zusammensetzung – auch bei gleicher Helligkeit – in unterschiedlicher Weise aufzunehmen, um gegebenenfalls selektiv darauf zu reagieren. Das Farbensehen dient der Identifizierung, Erkennung und Lokalisierung wichtiger Objekte, wie Nahrung oder Feinde, aber auch der Signalgebung, wie z.B. Warnfarben bei vielen Insekten, der Tarnung und der Kommunikation. Die Abbildung auf der Netzhaut kommt zustande durch die spektrale Zusammensetzung des Lichts, der Reflektionseigenschaften der Objekte und die unterschiedliche Absorption bestimmter Wellenlängen durch das Augenmedium. Zum Farbensehen werden mindestens zwei verschiedene Sehfarbstoffe benötigt, deren spektrale Empfindlichkeiten sich unterscheiden und überschneiden müssen (Farbrezeptoren; Zapfen). Im Gehirn wird das Verhältnis der Aktivitäten der einzelnen Zapfentypen ausgewertet (Farbwahrnehmung), wobei jede Wellenlänge theoretisch mit einem einmaligen solchen Verhältnis verknüpft ist. Bei zwei Photorezeptortypen (Dichromatie) wird an der Schnittstelle ihrer Empfindlichkeitsspektren ein achromatisches Grau wahrgenommen, da beide Rezeptoren gleichstark gereizt werden (neutraler Punkt). – Die Entwicklung des Farbensehens kann evolutionär zunächst als eine Verbreiterung des spektralen Absorptionsbereichs gedeutet werden; z.B. erweitert die Hinzufügung des roten zum grünen Spektralbereich beim Menschen primär den spektralen Empfindlichkeitsbereich, ermöglicht aber zugleich durch entsprechende neuronale Weiterverarbeitung auch die unterschiedliche Farbempfindung. Das Farbensehen wurde in der Evolution mehrmals unabhängig entwickelt. Es gibt mindestens drei Linien zu hochentwickelten Farbsehsystemen: eines zum Primatenfarbensehen, eines zum Farbensehen der Fische, Amphibien, Reptilien und Vögel und eines zum Farbensehen der Insekten (z.B. Hymenopteren). Das Farbensehen ist bei tagaktiven Tieren mit ebenfalls tagaktiven Vorfahren am stärksten ausgeprägt, wie z.B. bei Fischen, Reptilien oder Vögel. – Bei den Fischen ist die Fähigkeit zum Farbensehen abhängig vom jeweiligen Habitat, manchmal von der Jahreszeit und vom Alter der Tiere und wechselt oftmals bei Änderungen. Die Forelle z.B. besitzt als Jugendfisch einen UV-Rezeptor, der jedoch nach 1-2 Jahren wieder vollständig verschwindet. Einige Karpfenfische wechseln im Sommer von Porphyropsin zu Rhodopsin als vorherrschendes Pigment; der Pazifische Lachs ersetzt Rhodopsin durch Porphyropsin während seiner Wanderung vom offenen Meer zu den Laichplätzen im Süßwasser. Fische in seichtem Küstengewässer, das von blau-grünem Licht dominiert wird, haben oft nur zwei Zapfenpigmente mit Absorptionsmaxima von 430 nm und 530 nm (z.B. Kabeljau). Süßwasserfische besitzen mindestens drei, meistens vier verschiedene Zapfensorten, wobei die Sensitivitäten der Zapfen weit auseinanderliegen und somit ein großer Bereich vom UV bis zum Rot abgedeckt wird (z.B. Guppy, Goldfisch). Je tiefer der Lebensraum im Süßwasser, desto weiter verschiebt sich das sichtbare Spektrum ins längerwellige Rot und desto häufiger findet man das Porphyropsin als Sehpigment (z.B. Goldfisch, Forelle, Rotauge) neben dem Rhodopsin. Farbensehen tief im Ozean ist bei wenigen Tiefseefischen mit eigener Lichtquelle möglich, denn sie besitzen neben den Photorezeptoren für die vorherrschende Wellenlänge von 480 nm auch einen zweiten Typ, der am stärksten auf die eigenen produzierte Wellenlängen reagieren. – Amphibien können ebenso wie die Fische zusätzlich klare Öltröpfchen in den Zapfen haben. Frösche und der Feuersalamander sind trichromatisch (Absorptionsmaxima: 450 nm, 500 nm und 570 nm beim Feuersalamander), wobei hier die Stäbchen am Farbensehen mitbeteiligt sind. Oftmals wird bei der Metamorphose das Porphyropsin abgebaut, hin zu einer von Rhodopsin dominierten Netzhaut beim adulten Tier. – Vögel und Reptilien besitzen im inneren Zapfensegment zusätzlich verschiedenfarbige Öltröpfchen, die als Filter die einfallenden Wellenlängen begrenzen und somit die Sensitivität der Zapfen steigern. Das Schmälern der Bandbreite der Photorezeptoren wird durch die erhöhte Anzahl der verschiedenen Rezeptortypen (meistens vier) kompensiert. Durch Kombination der verschiedenen Öltröpfchen mit den einzelnen Zapfentypen sind potentiell noch mehr Farbrezeptortypen möglich. Die farbigen Tröpfchen absorbieren UV und kurzwelliges Licht und verschieben somit die maximale Empfindlichkeit der Zapfen weiter ins rote Spektrum (UV-Rezeptoren besitzen transparente Tröpfchen). Aufgrund der UV-Durchlässigkeit des Augenmediums dienen die Tröpfchen zudem als Schutz vor der schädlichen UV-Strahlung für diejenige Rezeptoren, die nicht UV-empfindlich sind (bei Säugern dient vor allem die gelbliche Linse als UV-Filter). Bei den Reptilien sind Schildkröten tetrachromatisch mit einem zusätzlichen UV-Rezeptor. Süßwasser-Schildkröten besitzen als Anpassung an ihren Lebensraum Porphyropsin als Chromophor. Nachtaktive Echsen und Geckos sind wohl dichromatisch mit stäbchenartigen Zapfen, die im blauen und im grünen Spektralbereich empfindlich sind. Interessanterweise besitzen Schlangen, deren Vorfahren (wie die der Säuger) im Dunkeln aktiv waren (unter der Erde grabend) auch keine Öltröpfchen mehr, dafür jedoch eine Linse, die UV-Licht absorbiert. Vögel sind meistens tetrachromatisch (z.B. Taube) mit dem Vorteil einer feineren Unterscheidung von Wellenlängen über einen größeren Spektralbereich bis ins nahe UV. Als Anpassung an die nächtliche Lebensweise besitzen Eulen erheblich mehr Stäbchen als Zapfen, sind aber immer noch mindestens trichromatisch. – Fast alle Säugetiere können Farben unterscheiden (Ausnahme: nachtaktive Säuger wie z.B. Ratten), wobei die meisten dichromatisch sind, mit einem Blaurezeptor (Absorptionsmaximum 430 nm bis 450 nm) und einem zweiten Zapfentyp im längerwelligen Bereich (Absorptionsmaxima Hund: bei 429 nm und 555 nm, Meerschweinchen: 429 nm und 529 nm). Dies ist begründet in der nächtlichen Lebensweise der Vorfahren der Säugetiere, die erst vor ca. 65 Millionen Jahren teilweise wieder zur tagaktiven Lebensweise übergehen konnten. Nur die Altweltaffen (und damit auch der Mensch) haben ein vollständig trichromatisches Farbsehsystem entwickelt, wobei bei allen Arten die Absorptionsmaxima der drei Zapfentypen relativ konstant bei ungefähr 430 nm, 535 nm und 565 nm liegen. Die Altweltaffen sind durch den Erwerb eines zusätzlichen Pigments durch Duplikation und Modifikation des Gens für das längerwellige Pigment trichromatisch geworden. Dies fand vor ungefähr 35 Millionen Jahren statt, was ungefähr dem Zeitpunkt der Trennung von Neuwelt- und Altweltaffen entspricht. Das Farbsehsystem der heutigen Neuweltaffen stellt ein mögliches Zwischenstadium zwischen Dichromatie und Trichromatie dar. Dort sind alle Männchen dichromatisch, ungefähr zwei Drittel der Weibchen jedoch trichromatisch. Das Gen für den längerwelligen Rezeptor liegt auf dem X-Chromosom mit drei möglichen Allelen (Absorptionsmaxima bei 536 nm, 550 nm und 563 nm beim Totenkopfäffchen). Weibliche Individuen besitzen im Gegensatz zu den Männchen zwei Genorte, womit alle heterozygoten Weibchen trichromatisch sind. Eine ähnliche Situation besteht nach neuesten Erkenntnissen auch bei einigen Halbaffenarten. – Bei Invertebraten findet man immer mehrere Pigmenttypen in einem Photorezeptor (Komplexauge). Bei den Insekten können außerdem alternierende Schichten in der Cornea als Interferenz-Filter fungieren, wobei durch deren Variation einzelne Ommatidien auf bestimmte Wellenlängenbereiche eingestellt werden können. Betrachtet man die generelle Verteilung der bisher bekannten Absorptionsmaxima der Photopigmente von Insekten, findet man vier Typen von Rezeptoren mit den Durchschnittswerten von 350 nm, 440 nm, 530 nm und 600 nm. Systeme mit drei verschiedenen Sehpigmenten sind bei den Insekten die Regel, so z.B. bei der Honigbiene (Empfindlichkeitsmaxima bei 335 nm, 435 nm und 540 nm; siehe Abb. ). Der UV-Rezeptor ist besonders wichtig für die Erkennung von Blumenblüten und die Erfassung von polarisiertem Licht (Polarisationssehen). Bei anderen Hymenopteren (z.B. Wespen, Ameisen) wird ebenfalls ein mindestens trichromatisches Farbsehsystem angenommen. Schmetterlinge (Lepidopteren) besitzen meistens vier Farbrezeptortypen, von denen einer zusätzlich im roten Spektralbereich empfindlich ist. Einige Dipteren besitzen zusätzlich ein Chromophor außen am Pigment, das als Antenne fungiert und Licht im UV-Bereich absorbiert (sogenanntes sensitizing pigment). Fangschreckenkrebse besitzen mindestens 12 spektral verschiedene Rezeptortypen, 8 für sichtbares Licht und 4 für den UV-Bereich. Ob diese und auch andere Invertebraten tatsächlich Farben so fein unterscheiden können, hängt von der nachfolgenden neuronalen Verschaltung ab (Farbwahrnehmung). Letztlich läßt sich die Fähigkeit zur Farbunterscheidung (und damit das Farbensehen) nur durch geeignete Verhaltensstudien (auch beim Menschen) oder wellenlängenabhängige Reaktionsversuche (z.B. Phototaxis, Beutefang) nachweisen. – Beim Menschen findet das Farbensehen hauptsächlich in der Umgebung der Fovea centralis statt, die nur Zapfen enthält. Die Zapfendichte nimmt nach wenigen Millimetern zur Peripherie hin rapide ab und bleibt dann auf konstant niedrigem Niveau. Die innersten 25 Bogenminuten der Fovea sind gänzlich ohne Blauzapfen und daher dichromatisch. Die in der Fovea befindlichen Rot- und Grünzapfen sind zufällig verteilt. Zusätzlich befindet sich dort eine Konzentrierung von gelbem Pigment, das kurzwelliges Licht filtert ("gelber Fleck"). Bis mindestens 40 Grad Sehwinkel können alle Farben unterschieden werden (bei sehr großen Reizen noch weiter in der Peripherie). Bei kleinen Reizen verschwindet der Farbeindruck zunächst für Grün, dann für Rot, Gelb und als letztes für Blau. Bereits im Alter von etwa 2-3 Monaten ist das trichromatische Farbensehen beim Menschen voll ausgeprägt und funktionsfähig. Mit zunehmendem Alter verändert sich das Farbensehen, z.B. durch Verlust von Zapfenpigmenten oder zunehmende Gelbfärbung der Linse, wobei vor allem die Aufnahme von kurzwelligem Licht stärker nachläßt.
F.St.
Farbensehen
Farbensehen der Honigbiene:
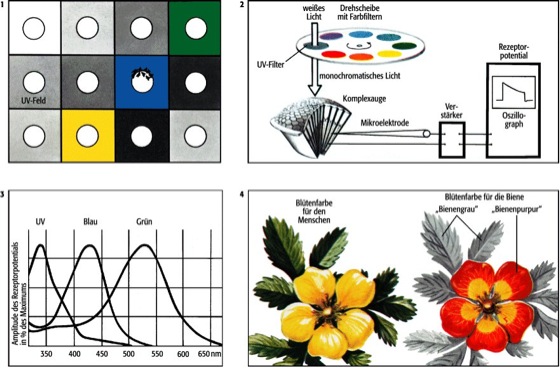
Anfang des 20. Jahrhunderts wies K. von Frisch nach, daß Bienen Farben zu unterscheiden vermögen. Dazu dressierte er die Bienen darauf, aus einem Schälchen mit Zuckerwasser zu trinken, das auf einem blauen Stück Papier stand (1). Die Bienen erkannten dieses Schälchen auch wieder, wenn er es zwischen viele andere Schälchen stellte, die auf verschiedenen Graupapieren standen. Der selbe Versuch gelingt auch, wenn man verschiedene Farbfelder im Wechsel mit Graufeldern benutzt: Die Bienen fliegen jeweils das Feld bevorzugt an, auf dem sie mit Zuckerwasser belohnt wurden, selbst wenn dieses Feld immer wieder verschoben wird (keine Ortsdressur!). Mit einer aus diesem Prinzip entwickelten Methode gelang es nachzuweisen, daß das Farbensehen der Biene in vielen Zügen mit dem des Menschen übereinstimmt.
Heute läßt sich das farbensehende Rezeptorsystem der Honigbiene auch durch direkte elektrophysiologische Messungen untersuchen. Durch die auf einem Rad angeordneten Farbfilter wird schmalbandiges Spektrallicht ("monochromatisches" Licht) erzeugt. Über eine in die Sinneszellen einer Ommatidie des Komplexauges eingestochene Mikroelektrode wird die von dem Lichtreiz erzeugte Spannungsänderung abgeleitet, verstärkt und über einen Oszillographen sichtbar gemacht (2). Bei diesem Experiment zeigt sich, daß es drei verschiedene Zelltypen mit verschiedenen Empfindlichkeitsspektren gibt. Ihre Reaktionen sind (zum besseren Vergleich mit den kolorimetrischen Ergebnissen beim Menschen) in % der maximalen Reaktion dargestellt (3). Die Form der Kurven ist denen des menschlichen Farbensehens nicht unähnlich. Lediglich der Wellenlängenbereich des sichtbaren Lichts ist bei den Bienen zu kürzeren Wellenlängen hin verschoben. Bienen können also ultraviolettes Licht wahrnehmen, sehen aber keine langwelligen Strahlungen.
Die Ähnlichkeit des farbwahrnehmenden Rezeptorsystems bei Mensch und Biene läßt nicht darauf schließen, daß auch die Systemausgänge, die letztlich wirksamen "Farbempfindungen", ähnlich geordnet sind. Man kann daher nur in einem übertragenen Sinn von "Bienenrot" oder "Bienengrau" sprechen. Trotzdem lassen sich durch die Berücksichtigung der verschiedenen Rezeptorsysteme Unterschiede erschließen, die in der Wahrnehmung von Mensch und Biene entstehen müssen. Abbildung 4 zeigt die Blüte des Fingerkrauts, links durch ein Gelbfilter, rechts durch ein UV-Filter betrachtet. Für den Menschen erscheint diese Blüte einheitlich gelb, während mit dem UV-Filter sichtbar wird, daß der UV-reflektierende Randbereich der Blüte die Saftmale im Blüteninnern für UV-empfindliche Augen hervorhebt. Die Kolorierung des Bildes versucht die abweichende Wahrnehmung der Biene für das menschliche Auge anschaulich zu machen.
Wenn Sie inhaltliche Anmerkungen zu diesem Artikel haben, können Sie die Redaktion per E-Mail informieren. Wir lesen Ihre Zuschrift, bitten jedoch um Verständnis, dass wir nicht jede beantworten können.