Synthetische Biologie: »Wir können Lösungen finden, die die Natur nie erreicht hat«
Kerstin Göpfrich beschäftigt sich mit dem Bau von synthetischen Zellbestandteilen. Sie erforscht auch, ob sich vielleicht sogar lebende Zellen erschaffen lassen. Dabei setzt sie auf DNA und RNA als Baumaterial. Mithilfe von Computerdesign konstruiert sie Moleküle, die sich zu bestimmten Formen falten. Damit ist es möglich, völlig andere Biostrukturen zu erzeugen, als die Natur sie hervorbringt. Wofür könnte das gut sein? Spektrum befragte die Forscherin am Rande einer Fachkonferenz in Heidelberg.
Frau Göpfrich, Sie betreiben synthetische Biologie – eine Fachrichtung, in der es darum geht, biologische Systeme zu erzeugen, die in der Natur nicht vorkommen. Hierbei erforschen Sie sogenannte Bottom-up-Ansätze. Was ist das?
In der synthetischen Biologie unterscheiden wir zwei entgegengesetzte Herangehensweisen, und zwar Bottom-up und Top-down. Beim Top-down-Ansatz versucht man, biologische Zellen etwa mithilfe von genetischen Manipulationen so zu verändern, dass man ihnen gewünschte Eigenschaften verleiht. Ein Beispiel dafür ist die Minimalzelle, die man genetisch so stark reduziert hat, dass sie nur noch jene 473 Gene besitzt, die offenbar unbedingt überlebensnotwendig sind. Beim Bottom-up-Ansatz gehen wir andersherum vor. Da fangen wir nicht mit einer lebenden Zelle an, sondern mit einzelnen Molekülen. Die versuchen wir zusammenzusetzen, um eine Art von Minimalzelle von Grund auf neu aufzubauen. Man könnte sagen, wir versuchen, eine Zelle im Labor zu erzeugen – oder einen Übergang von toter zu lebendiger Materie zu bewirken. Hierfür möchten wir ein Minimalsystem bauen, das dazu fähig ist, sich selbst zu vermehren und eine Evolution zu durchlaufen, und damit dann gewünschte Eigenschaften hervorbringen kann. Es geht also nicht darum, menschliche Zellen oder gar Gewebe zu erzeugen, sondern um eine kleinste, sich selbst kopierende und verbessernde Einheit. Vielleicht ist der Begriff »Zelle« da schon fast zu hochgegriffen.
Was ist der Vorteil von Bottom-up, verglichen mit Top-down?
Erst einmal ist es eine Frage, die von Neugier getrieben ist: Kann es gelingen, Leben künstlich herzustellen? Wir kennen genau ein Beispiel für einen Himmelskörper, auf dem sich Leben entwickelt hat, und das ist die Erde – und selbst dort passierte es, soweit wir wissen, nur ein einziges Mal. Als Experimentalist ist man nie zufrieden mit n gleich eins, also mit einem Experiment, das nicht wiederholbar ist. Daher interessiert mich: Können wir Leben aus molekularen Bausteinen selbst bauen? Das ist für mich der große Grund, mich überhaupt mit dem Themenfeld zu beschäftigen. Natürlich können wir diese Frage nur beantworten, wenn wir das auch wirklich von Grund auf, sprich Bottom-up, versuchen. Und nicht Top-down, indem wir eine bereits lebende Zelle nehmen und dann nach und nach immer weiter reduzieren.
Und wenn man nicht nur aus Neugier handelt und fragt, welchen praktischen Nutzen diese Forschung haben könnte?
Hier in Heidelberg schauen wir beispielsweise in Richtung Immunologie. Immunfunktionen künstlich zu beeinflussen, etwa um Krankheiten zu behandeln, ist sowohl mit Bottom-up- als auch mit Top-down-Ansätzen möglich. Ein Beispiel für eine Top-down-Anwendung ist die CAR-T-Zelltherapie, bei der man Immunzellen aus Patienten entnimmt, ein CAR-Gen mittels Gentechnik in sie einschleust und die so veränderten Zellen anschließend wieder in den Patienten bringt, damit sie Tumorzellen in seinem Körper angreifen. Damit lassen sich viele Krebsarten erfolgreich behandeln, die bisher als unheilbar galten. Allerdings ist die Skalierbarkeit solcher Ansätze nur begrenzt, weil sie kostspielig sind.
Was meinen Sie mit Skalierbarkeit?
Dass man etwas bei Bedarf in großen Mengen herstellen kann, sodass beispielsweise viele Patienten davon profitieren können – im Falle einer CAR-T-Zelltherapie etwa die genetisch veränderten Immunzellen. Und da könnte ein Bottom-up-Ansatz viele Vorteile haben. Zum einen könnte er es erlauben, Genregulationsmechanismen der Zelle zu umgehen. Die machen einem bei Top-down-Verfahren häufig einen Strich durch die Rechnung, etwa wenn die gentechnisch veränderten Immunzellen das eingeschleuste Gen nicht so oft ablesen wie gewünscht. Mit Bottom-up lässt sich das vielleicht verhindern, indem man alles von Grund auf neu baut und dabei optimiert. Wir können damit Lösungen finden, die die Natur nie erreicht hat. Denn die natürliche Evolution ist eine Zufallsbewegung, ein sogenannter Random Walk, der immer nur von gewissen Startpunkten ausgeht und auch nur bestimmte Richtungen einschlagen kann. Es gibt dabei viele Einschränkungen: Der Startpunkt ist stets ein existierender Organismus; jede neue Tochtergeneration muss lebens- und vermehrungsfähig sein und so weiter. Deswegen gibt es im Raum der Möglichkeiten viele Gebiete, wohin die natürliche Evolution nie gelangt, obwohl dort theoretisch gute Lösungen warten. Ich bin überzeugt, dort gibt es viel zu entdecken.
Für Ihre Doktorarbeit haben Sie künstliche Kanalmoleküle hergestellt, die sich in Zellmembranen einfügen. Dafür nutzten Sie das DNA-Origami, also die Technik, Molekülstrukturen aus DNA-Strängen zu falten. Wozu diente das?
Zunächst einmal war das wieder von Neugier getrieben. Zellen bauen ihre funktionale Maschinerie aus Proteinen, und auch Transmembrankanäle in Zellen sind immer proteinbasiert, soweit wir wissen. Und da kann man sich natürlich die Frage stellen: Lässt sich eine komplementäre, ganz andersartige molekulare Maschinerie aus anderen sequenzcodierenden Polymeren bauen, etwa aus DNA, RNA oder was auch immer? Wir haben damit angefangen und gesehen, es funktioniert.
Was kann man damit machen?
Ein mögliches Anwendungsfeld ist die Detektion von Molekülen. Man kann zum Beispiel ein DNA-Molekül durch die Öffnung des künstlichen Transmembrankanals ziehen, dabei ein elektrisches Feld anlegen und den Stromfluss durch den Kanal messen – abhängig davon, wie dicht das DNA-Molekül die Pore jeweils verschließt. Aus den gemessenen Strömen lässt sich die Sequenz der DNA ablesen. Vielleicht ist es auch möglich, die Technik medizinisch zu nutzen. Eine Idee, die ich in meiner Doktorarbeit zusammen mit einem Neurowissenschaftler verfolgt habe, lautete: Wenn Nervenzellen nicht mehr so gut feuern, kann man sie dann wieder in Schwung bringen, indem man mit künstlichen Porenmolekülen einen zusätzlichen Kalziumfluss durch ihre Membran ermöglicht? Es stellte sich heraus, dass das nicht so einfach ist, weil unsere Poren nicht selektiv genug waren.
Heute arbeiten Sie mit RNA-Origami, dem Falten molekularer Strukturen aus RNA-Strängen. Was ist der Vorteil gegenüber DNA-Origami?
DNA-Origami basiert auf Basenpaarungen, also den Wasserstoffbrückenbindungen zwischen je zwei Nukleobasen, die sich in der DNA-Doppelhelix gegenüberliegen. Wenn man einen einzelnen DNA-Strang künstlich herstellt und so konstruiert, dass er sich mittels Basenpaarungen mit anderen, kürzeren DNA-Strängen zu einer bestimmten Form der Doppelhelix faltet, kann man damit sehr schöne molekulare Gerüste bauen, in denen man dann beispielsweise weitere Moleküle positionieren kann. Aber RNA kann nicht nur eine Doppelhelix, sondern noch viele andere Faltungen bilden, und dadurch eröffnen sich völlig neue Möglichkeiten. Wenn man DNA-Origami mal mit dem Kinderspielzeug »Lego Duplo« gleichsetzt, dann ist RNA-Origami so etwas wie »Lego Technic«. RNA-Strukturen können viel mehr, wenn es um Funktionalität geht.
Welche anderen Faltungen sind das?
Ein Beispiel hierfür sind RNA-Aptamere, das sind antikörperähnliche Strukturen aus RNA, die spezifisch ganz bestimmte Moleküle erkennen und sich an sie binden. Ein anderes Beispiel sind Ribozyme, also RNA-Strukturen, die katalytisch aktiv sind und somit biochemische Reaktionen beschleunigen. Wenn wir molekulare Maschinen bauen wollen – so wie die aus Proteinen, die wir in unseren Zellen haben –, dann ist RNA als Ausgangsmaterial die bessere Wahl. Das sieht man an den Ribosomen, den makromolekularen Komplexen, die in unseren Zellen die Proteine zusammenbauen. Das sind molekulare Apparate mit komplexer Funktion, die großteils aus RNA aufgebaut sind.
Warum kann RNA so viel mehr als DNA?
Chemisch gesehen ähneln sich die beiden sehr. Der Unterschied liegt in einer weiteren OH-Gruppe an jedem RNA-Baustein. Diese OH-Gruppe kann Wasserstoffbrücken formen, zusätzlich zu denen, die sich zwischen den Nukleobasen bilden. Mit den Extra-Wasserstoffbrücken können ganz andere Faltungen entstehen – nicht nur die Doppelhelix durch Basenpaarung, sondern noch etliche weitere. Es sind komplexeste Strukturen möglich, die oft nicht einfach vorherzusagen sind.
Wie funktioniert RNA-Origami? Wie gehen Sie dabei vor?
Zunächst entwerfen wir das Design der gewünschten Struktur. Wir überlegen uns erst einmal die grobe Form. Sagen wir, wir wollen ein Rechteck. Dann fragen wir uns, wie wir einzelne RNA-Moleküle so falten können, dass sie das Rechteck formen. Welche Sequenz müssen wir ihnen geben, damit sie eine entsprechende Gestalt annehmen? Das ist das sogenannte inverse Faltungsproblem: Man geht von einer Struktur aus und überlegt sich dann, welche Sequenz diese Struktur hervorbringt. Wir lösen das Problem am Computer und rechnen die erhaltene RNA-Sequenz in die entsprechende DNA-Sequenz um. Die DNA-Sequenz stellen wir dann künstlich her und versehen sie mit einem Promotor, einem Sequenzabschnitt, an den sich Enzyme binden können, die das künstliche DNA-Molekül ablesen. Das Ergebnis ist ein synthetisches Gen. Wenn die Enzyme, sogenannte Polymerasen, es ablesen, entsteht die gewünschte RNA. Die faltet sich, noch während sie produziert wird, zu der gewünschten Form.
»RNA-Origami passiert durchweg bei 37 Grad, also auch in natürlichen zellulären Umgebungen. Das ist ein großer Vorteil des Verfahrens«
Müssen Sie dabei mit sprunghaften Temperaturänderungen arbeiten?
Nein. Das kennen Sie wahrscheinlich vom DNA-Origami, wo solche Temperatursprünge nötig sind, um die Wasserstoffbrücken immer wieder aufzubrechen und neu entstehen zu lassen. RNA-Origami passiert durchweg bei 37 Grad, also auch in natürlichen zellulären Umgebungen. Das ist ein großer Vorteil des Verfahrens, dass es kompatibel ist mit der normalen Zellphysiologie. Deshalb ist RNA-Origami sehr gut skalierbar: Man kann die künstliche DNA-Vorlage beispielsweise in E.-coli-Bakterien einbringen und die Mikroben dann in einem Bioreaktor so viel RNA herstellen lassen, wie man will. Das könnte gerade für medizinische Anwendungen relevant sein.
Haben Sie so etwas wie einen Baukasten mit RNA-Sequenzen darin, die jeweils bestimmte räumliche Strukturen hervorbringen?
Wir haben eine Datenbank mit einer Art Sequenz-Legosteinen. Wenn wir beispielsweise eine RNA-Struktur mit einer Art Stamm bauen möchten und dieser Stamm soll an einer bestimmten Stelle enden, dann benötigen wir dort sozusagen den Lego-Endstein. Oder wenn wir einen 90-Grad-Winkel in die Struktur einbringen wollen, dann müssen wir schauen, in welchen natürlich auftretenden RNA-Molekülen ein 90-Grad-Winkel vorkommt. Den Molekülabschnitt dort, diesen Lego-Block, den übernehmen wir dann und bauen ihn in unsere Struktur ein.
Als Fernziel Ihrer Arbeiten möchten Sie nicht nur zelluläre Komponenten herstellen, sondern sogar komplette Zellen. Wie kann das funktionieren?
Hier muss ich, glaube ich, etwas klarstellen, damit keine Missverständnisse auftreten. Wenn wir das Wort »Zelle« hören, dann denken wir automatisch an biologische Zellen, wie wir sie heute kennen. Zellen, die eine riesige Vielfalt von Proteinen haben, die DNA in RNA umschreiben und diese wiederum in Proteine. Zellen, die aus Millionen von Komponenten bestehen und wahnsinnig komplex sind. Wenn man aber vier Milliarden Jahre zurückgeht, kommt man an den Punkt, wo das Leben entstanden ist. Damals müssen simplere Prozesse die Vervielfältigung und Evolution der frühen Lebensformen ermöglicht haben. Die molekulare Maschinerie kann damals noch nicht so komplex gewesen sein.
Das heißt, mit dem, was Sie bauen, würden Sie gern an diesen Punkt kommen?
Ja. Nicht notwendigerweise mit denselben Molekülen und Umweltbedingungen, sondern einfach an einen Startpunkt, wo ein von uns konstruiertes System sich selbst vervielfältigt und eine Evolution durchläuft, bei der es komplexer werden kann. Ich habe vorhin gesagt, Evolution ist eine Zufallsbewegung; das gilt aber nur, solange wir sie frei laufen lassen. Im Labor können wir eine gerichtete Evolution herbeiführen – ich kann meiner künstlichen Zelle beispielsweise nur Krebszellen vorsetzen und dann jeweils gezielt die Exemplare heraussuchen, die sich so verändert haben, dass sie Krebszellen aufspüren und töten. Damit sind wir viel schneller als die natürliche Evolution, und wir gehen im Gegensatz zu ihr von einer Minimalzelle als Startpunkt aus, die wir selbst konzipiert haben.
Wie simpel kann so eine Minimalzelle sein?
Wenn ihre Komponenten aus RNA bestehen, ist die Translationsmaschinerie, die in natürlichen Zellen die Anweisungen der Boten-RNAs in Proteine übersetzt, verzichtbar. Und dann muss so ein Minimalsystem erst einmal nicht viel mehr können als zu wachsen und sich zu teilen, das ist sicherlich mit relativ wenigen Genen erreichbar. Vielleicht genügt es schon, ein System mit zwei Sorten von Bausteinen zu konstruieren, nämlich Zellskelettelementen und Membranporen, und deren Zusammenspiel zeitlich gekonnt zu orchestrieren.
Minimalsysteme aus RNA als Startpunkte des Lebens: Das klingt nach der RNA-Welt-Hypothese, die davon ausgeht, das irdische Leben habe mit RNA-Molekülen als universellen Bausteinen begonnen. Halten Sie persönlich diese These für plausibel?
Ich stelle mir die Ursuppe auf der Erde als Chaos vor. Da wird nicht alles nur RNA gewesen sein. Da schwammen noch alle möglichen anderen Moleküle herum, es gab Gesteinsoberflächen, es gab Wasser und so weiter. Deshalb ist dieser Fokus auf eine Molekülsorte aus meiner Sicht nicht so sinnvoll, weil komplexe Systeme wie Zellen immer durch Interaktion entstehen. Trotzdem glaube ich, dass RNA eine wichtige Rolle gespielt hat. Einfach, weil es irgendeine Art von Informationsspeicher gegeben haben muss, und irgendeine Art von Stoffwechselkatalyse auch, und RNA kann beides.
»Selbst wenn die ersten Lebensformen vielleicht sehr einfach waren, dann war es ihre Umgebung sicher nicht«
Aber eben nicht isoliert?
Genau. Selbst wenn die ersten Lebensformen vielleicht sehr einfach waren, dann war es ihre Umgebung sicher nicht. Eher im Gegenteil: Je komplexer das Leben wird, desto besser kann es sich regulieren und mit verschiedenen Umweltbedingungen umgehen und umso weniger ist es auf eine bestimmte komplexe Umgebung angewiesen, um an überlebenswichtige Ressourcen wie Biomoleküle zu kommen. Am Anfang des Lebens musste wahrscheinlich die Umwelt noch sehr viele dieser Ressourcen liefern.
Lassen sich alle Bestandteile einer lebensfähigen Zelle mithilfe von RNA-Origami konstruieren?
Nicht direkt. RNA kann zwar etwas Wichtiges, nämlich sich selbst kopieren. Dabei passieren hin und wieder Fehler, sodass Mutationen auftreten und eine Evolution in Gang kommt. Was man dann aber sehr schnell sieht: Als Ergebnis dieser Evolution wird die RNA immer einfacher. Denn je kürzer sie ist, desto schneller kann sie sich kopieren, was ihr einen Vermehrungsvorteil verschafft. Das ist natürlich nicht so schön. Denn man möchte ja, dass die Evolution von Minimalsystemen ausgehend zu komplexeren Lebensformen mit neuen Merkmalen führt – und nicht bloß den einfachstmöglichen Replikator hervorbringt.
Wie lässt sich das erreichen?
An dieser Stelle helfen uns Lipidmoleküle weiter, die einen wasserliebenden und einen wasserabstoßenden Teil haben. Sie sitzen in der Regel an Grenzflächen, etwa zwischen Wasser und Luft, und neigen unter bestimmten Bedingungen dazu, Bläschen zu formen, in denen sie andere Moleküle wie RNA einschließen können. Wenn das geschieht, dann läuft die Evolution nicht mehr nur zum einfachsten System hin. Weil es dann nicht mehr nur wichtig ist, schnell zu sein, sondern auch, möglichst gut mit anderen Molekülen zu interagieren – etwa um porenähnliche Strukturen in der Bläschenhülle zu formen, durch die benötigte weitere Moleküle einströmen können und so weiter. Dann haben auf einmal auch komplexere Merkmale einen Selektionsvorteil. Hier zeigt sich, wie nachteilig es ist, die Dinge isoliert zu betrachten. Mit RNA allein scheint es rätselhaft, woher die Komplexität kommt. Aber wenn man die Umgebung einbezieht, die Entstehung abgegrenzter Räume und so weiter, dann ist das einfacher zu beantworten.
Welche Funktionen, die natürliche Zellen aufweisen, können künstliche RNA-Strukturen mit Sicherheit nicht erfüllen?
Man muss anerkennen, dass Proteinenzyme katalytisch aktiver sind als Ribozyme, also einfach schneller. Deshalb ist es nicht überraschend, dass heutige Lebewesen eben Proteine als molekulare Maschinen verwenden. In einem direkten Wettbewerb werden Zellen, deren Funktionen großteils auf RNA basieren, das Nachsehen haben. Aber wer sagt denn, dass die Evolution nicht auch in solchen Zellen irgendwann RNA-Maschinen wie das Ribosom hervorbringt, die dann die Proteinherstellung sogar in synthetischen Zellen ermöglichen? Wir sind in vielerlei Hinsicht noch am Anfang, etwa beim Einbeziehen von Ribozymen in RNA-Nanostrukturen. Aber wir sehen, dass so etwas wie eine künstliche Zelle möglich ist, und der entscheidende Schritt wird die Orchestrierung des Genoms sein – also, dass wir regulatorische Elemente so einbauen, dass die richtige Komponente zur richtigen Zeit in der richtigen Menge am richtigen Ort produziert wird.
»Wenn Information und Funktion nicht im selben Molekül vereint sind, dann ist der Lösungsraum der Möglichkeiten für die Evolution viel größer«
Auch in Ihren synthetischen Zellen besteht das Genom immer aus DNA?
Ja. Der Grund dafür lautet: Wenn Information und Funktion nicht im selben Molekül vereint sind, dann ist der Lösungsraum der Möglichkeiten für die Evolution viel größer. Wenn die RNA zugleich Erbinformation speichert und katalytische Aktivität bereitstellt, dann kann eine Veränderung in ihr rasch den Tod bedeuten. Sind die beiden Funktionen aber entkoppelt, ist das System insgesamt widerstandsfähiger. Deshalb haben mein Team und ich entschieden, unsere Minimalzellen mit einem DNA-basierten Genom auszustatten, das für funktionale RNA-Moleküle codiert. Aber das ist nur ein möglicher Ansatz; andere Herangehensweisen können genauso zum Erfolg führen. Meine Hoffnung ist, dass es noch vor meinem Renteneintritt nicht mehr nur n gleich eins Beispiele für Leben gibt, sondern vielleicht n gleich zwei, drei oder vier.
Sie arbeiten in einem Forschungsprojekt mit, in dem es darum geht, Virusantigene in Gerüste einzubetten, die aus RNA oder DNA gefaltet sind. Was ist der Vorteil davon?
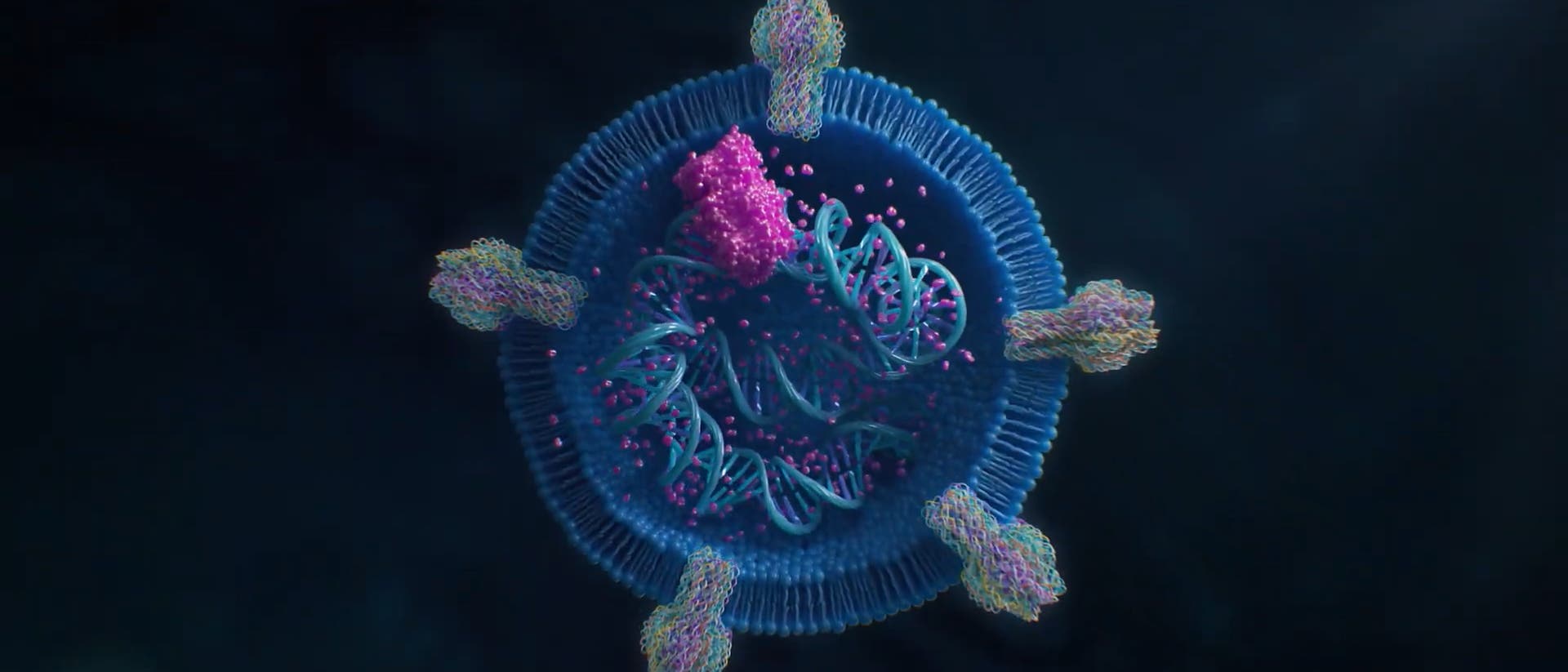
Viren präsentieren ihre Oberflächenproteine in einer gewissen Anzahl und Dichte auf ihrer Außenseite. Vielen ist vielleicht noch das Bild von Coronaviren geläufig, die außen mit Spike-Proteinen besetzt sind. Darauf reagiert dann unser Immunsystem. Wenn wir Virusantigene aber künstlich herstellen und verabreichen, etwa im Rahmen einer Impfung, dann schwimmen die frei in Lösung. Sie sind dann also nicht in gewissen Abständen und in bestimmter Anzahl präsent. Deshalb gelingt es manchmal nicht, mit Impfstoffen eine lang anhaltende, ausreichende Immunantwort zu erzeugen. Hier könnte es von Vorteil sein, Antigene in einem Gerüst zu platzieren – und zwar so dicht und zahlreich, dass die Immunzellen davon optimal stimuliert werden. DNA-Origami eignet sich dafür im Moment oft besser als RNA-Origami, einfach weil die Methode viel weiter fortgeschritten ist.
Gibt es schon praktische Erfahrungen mit solchen Gerüst-Antigen-Strukturen?
Tatsächlich ja. DNA-Origami-Impfstoffe gegen HI-Virusinfektionen werden gerade in vorklinischen Studien getestet und zeigen vielversprechende Ergebnisse. Wann das einmal in der Klinik ankommen wird, ist aber offen. In jedem Fall sind bis dahin noch viele regulatorische Hürden zu nehmen.
Sie haben die Initiative »Ring a Scientist« gegründet. Schulklassen können sich dort Wissenschaftlerinnen und Wissenschaftler per Videokonferenz in den Unterricht holen.
Die Idee dazu hatte ich während meiner Doktorarbeit, gemeinsam mit meinem damaligen Freund, der jetzt mein Mann ist. Ich bin damals oft in Schulen gegangen und habe über Wissenschaft gesprochen. Es kamen viele solche Anfragen von Schulen; etliche davon lagen weit weg. Irgendwann war es zeitlich nicht mehr machbar, selbst dorthin zu fahren, aber per Videokonferenz ließ es sich einrichten. Wir merkten, dass das gut ankam – ich konnte das Labor zeigen, für die Lehrer war es viel weniger Aufwand und es fielen keine Reisekosten an. Und es ließ sich gut in den Arbeitsalltag integrieren. Ich erzählte Kolleginnen und Kollegen davon, und die sagten: »Ach ja, das würde ich auch mal machen.« Und so haben wir die Plattform »Ring a Scientist« aufgesetzt.
Was genau kann man dort machen?
Schülerinnen und Schüler, Lehrende, Wissenschaftler, Akademikerinnen, Mitarbeiter von Pressestellen und so weiter können sich dort registrieren. Man kann nach Expertinnen und Experten suchen und sie um eine Videokonferenz bitten. Das Ganze startete schleppend, doch während der Covid-19-Pandemie hat es total geboomt. Jetzt läuft es quasi von selbst und sehr gut, obwohl kein Funding dahintersteht. Es ist schön zu sehen, wie man mit sehr wenigen Mitteln eine so weitreichende Kommunikation ermöglichen kann.
Wie oft gibt es solche Videokonferenzen?
500 Wissenschaftlerinnen und Wissenschaftler sind inzwischen auf der Plattform. Wir dokumentieren das nur zum Teil, aber ich denke, etwa alle zwei bis vier Wochen finden Gespräche statt. Lehrerinnen und Lehrer nehmen das gern in Anspruch, und sie machen es oft enorm gut. Ich habe schon so schöne Gespräche dort geführt oder Diskussionen anmoderiert, oder war Teil von Jurys in Schülerprojekten, die seitens der Schüler und Lehrer fantastisch vorbereitet waren. Wir bekommen von überall auf der Welt Anfragen; die verschiedenen Sprachen der bei uns registrierten Personen sind in den Profilen hinterlegt; und es ist besonders schön, Wissenschaft auch in den ländlichen Raum zu bringen, wo man nicht einfach mal eine lokale Uni besuchen kann. Ich glaube, die Covid-19-Pandemie hat gezeigt, dass Wissenschaftskommunikation die gesamte Gesellschaft erreichen muss – und nicht erst dann, wenn es emotional wird, weil es dann eigentlich zu spät ist. Es reicht hierbei nicht aus, irgendwelche Events zu veranstalten, wo enorm gebildete Leute zusammenkommen und sich Vorträge anhören. Wenn die Wissenschaft Technologien entwickelt, die die Gesellschaft nicht annehmen will, muss ein Dialog stattfinden. Und zwar nicht nur unter den Menschen, die sich eh für diesen Dialog interessieren, sondern möglichst unter allen. Und in den Schulen erreicht man sehr viele.
Wenn Sie inhaltliche Anmerkungen zu diesem Artikel haben, können Sie die Redaktion per E-Mail informieren. Wir lesen Ihre Zuschrift, bitten jedoch um Verständnis, dass wir nicht jede beantworten können.