Gentechnologie: Moskitos mit Selbstmordgen
Hinter dem kleinen Ort Rio Florido wird die Straße, die durch Soja-, Kakao-, Bananen- und Mangoplantagen führt, zu einem kurvenreichen, holprigen Schlammweg und endet schließlich vor einer bewachten Sperre. Wir befinden uns ganz im Südosten Mexikos nahe der Grenze zu Guatemala bei der Stadt Tapachula. Die Anlage ist mit Stacheldraht umzäunt. Auf einem Warnschild sind ein Mann und eine Frau abgebildet, zwischen ihnen eine Stechmücke. Auf Spanisch steht darauf, dass hier genetisch modifizierte Moskitos gehalten werden, deren Handhabung spezielle Vorsichtsmaßnahmen erfordert. Der Posten lässt uns durch das Tor.
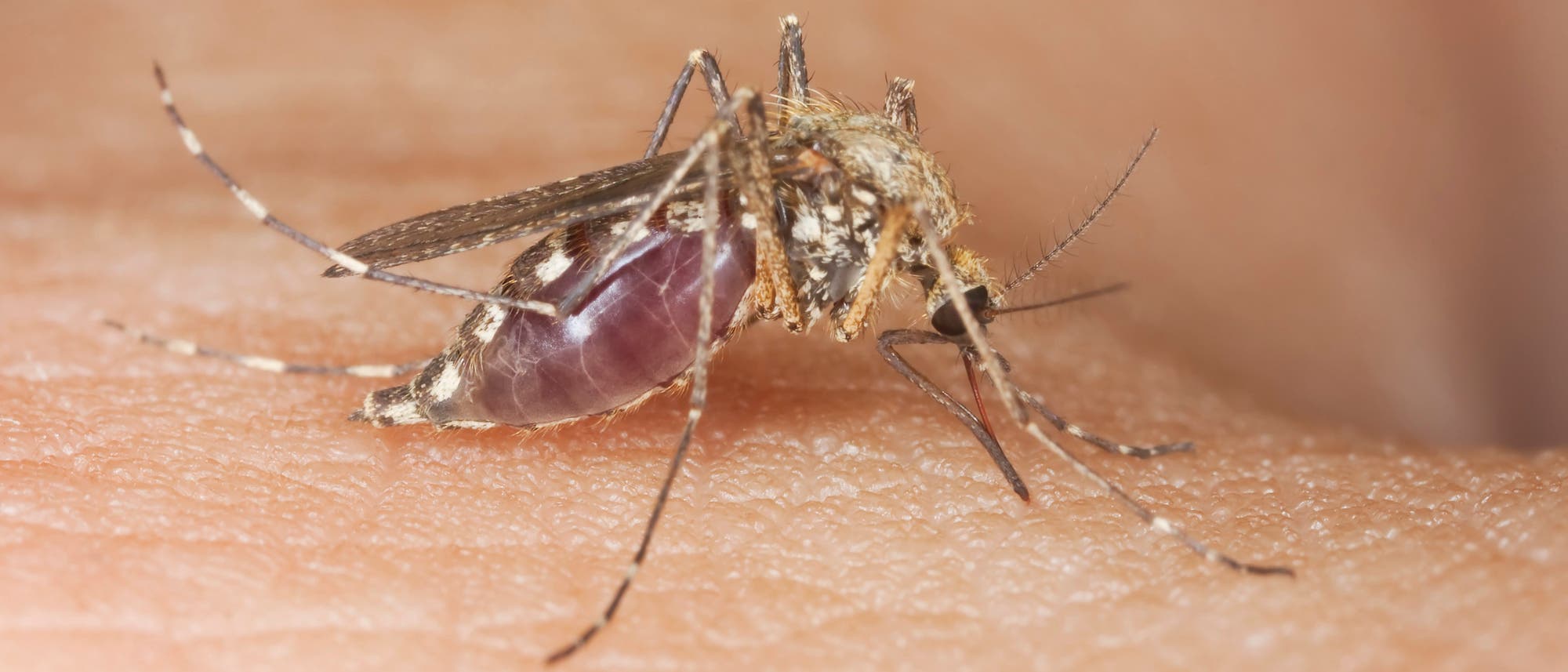
Drinnen beschatten Cashewbäume eine Plattform voller großer Käfige, die mit Gaze verhüllt sind. In ihnen tummeln sich Unmengen Gelbfiebermücken, auch Ägyptische Tigermücken genannt. Wissenschaftlich heißt diese Moskitoart heute meist Stegomyia aegypti, aber viele sprechen noch wie früher von Aedes aegypti. Diese kleinen, kaum hörbaren Mücken sind besonders in den Tropen und Subtropen weit verbreitet und gelten als Hauptüberträger des Denguevirus.
Hier in Südmexiko gehört die Spezies zu den vorherrschenden Stechmücken. In der Versuchsanlage werden genetisch veränderte ("transgene") Männchen darauf angesetzt, sich mit normalen Weibchen der lokalen Population zu paaren. Die neuen Gene sollen die weibliche Nachkommenschaft außer Gefecht setzen – ein Trick, mit dem sich womöglich das Denguefieber ausrotten ließe und damit eine der problematischsten und schwersten Infektionskrankheiten, deren Häufigkeit derzeit sehr schnell zunimmt. Gelbfiebermücken sind zwar nicht die einzigen, aber die Hauptüberträger dieser bedrohlichen Seuche.
Weltweit infizieren sich inzwischen pro Jahr schätzungsweise rund 100 Millionen Menschen mit Dengueviren, genauer gesagt mit einem von vier eng verwandten Serotypen. In manchem ähneln die Symptome denen einer Virusgrippe. Typisch sind aber neben hohem Fieber, Kopfschmerzen und Übelkeit unter anderem auch Hautausschläge sowie sehr starke Gelenk- und Muskelschmerzen bis hin zu Krämpfen und Bewegungsstörungen. Lebensbedrohlich wird es, wenn innere Blutungen und Hautblutungen oder ein Kreislaufschock auftreten, was besonders bei einer Zweitinfektion mit einem anderen Serotyp vorkommt.
Kostenloses Probeheft | Blättern Sie durch die aktuelle Ausgabe und sichern Sie sich Ihr kostenloses Probeheft!
Noch gibt es gegen Dengueviren keine Impfung und keine spezifischen Medikamente. Gegenmaßnahmen beschränken sich auf die Eindämmung der Mückenbestände etwa mit Insektiziden sowie die übliche Vorbeugung gegen Moskitostiche, zum Beispiel mit Repellents oder schützender, teilweise auch imprägnierter Kleidung und speziell besprühten dichten Netzen. Vorwiegend stechen die winzigen Biester tagsüber und in der Dämmerung. Ihre Larven gedeihen in jeder kleinsten Wasserpfütze, ob in alten Autoreifen, an Pflanzen oder in Vasen, in Dachrinnen oder zwischen Müll. Dort überstehen die Insekteneier sogar lange Trockenphasen. Deswegen gehört zu den vordringlichen Maßnahmen, alle Gefäße dicht abzudecken und jegliches offene Wasser zu vermeiden.
Eine offensivere Strategie verfolgt der Molekularbiologe Anthony A. James von der University of California in Irvine, dessen streng abgeschirmte Feldstation wir hier in Südmexiko besuchen. Er und seine Kollegen haben Gelbfiebermücken Gene verpasst, mit denen neue Mückenweibchen keine funktionsfähige Flugmuskulatur mehr entwickeln und bald nach dem Schlüpfen eingehen, während die männlichen Nachkommen unbeeinträchtigt bleiben. Nur die Weibchen saugen Blut, können sich aber nun nicht mehr paaren und nicht stechen, während sich die Männchen der nächsten Generationen fleißig sexuell betätigen und dabei die tödliche Genfracht verbreiten. Damit sollte die betreffende Population bald zusammenbrechen. Dass dies funktionieren kann, haben bereits Laborversuche an der Colorado State University in Fort Collins erwiesen, die Megan Wise de Valdez durchführte, eine Mitarbeiterin von James. Als man zu normalen Gelbfiebermücken transgene Männchen setzte, gingen die Bestände in den Käfigen binnen fünf Monaten zu Grunde. Nun soll sich das Verfahren in Südmexiko im Freien zunächst in großen verschlossenen Behältnissen gegen die dortigen Mücken bewähren.
Wenn die Studie erfolgreich verläuft, könnte man solcherart veränderte Moskitos massenweise in Dengue-Endemiegebieten freisetzen und mit ihrer Hilfe die Plagegeister dezimieren. Noch warnen manche Experten allerdings vor unabsehbaren Folgen für die Natur. Die Forscher sind sich bisher nicht einig, welche Maßstäbe und Kriterien sie dazu ansetzen sollten. Denn für Tests an und den Umgang mit transgenen Organismen existieren auf internationaler Ebene noch keine übergreifend verantwortlichen Organisationen oder allgemein verbindlichen Gesetze. Im Grund können Wissenschaftler und Unternehmen auf dem Gebiet tun, was sie für richtig und zweckmäßig halten. Sogar eine unkontrollierte Freisetzung transgener Insekten zu Testzwecken ist in manchen Drittweltländern möglich, und das, ohne die Menschen vor Ort davon in Kenntnis zu setzen, geschweige denn ihr Einverständnis einzuholen.
James bemüht sich bei seinem Projekt um möglichst viel Öffentlichkeitsarbeit. Dafür scheuen er und seine Mitarbeiter seit Jahren weder Zeit noch Aufwand. Beispielsweise erwarben sie das Stück Land für die abgeschottete Versuchsstation nach Verhandlungen mit den kommunalen Verantwortlichen von Tapachula über das dortige traditionelle Verteilungssystem. Über die laufenden Studien und zukünftigen Vorhaben informieren sie die Bevölkerung in Veranstaltungen und Diskussionen. Dieser Wissenschaftlergruppe ist es besonders wichtig, die transgenen Insekten zunächst zwar unter freilandnahen Bedingungen, aber hermetisch abgeschirmt zu prüfen.
Sein früherer Forschungskollege Luke Alphey, Gründer des in Großbritannien ansässigen Biotechnologieunternehmens Oxitec, schuf dagegen zum Schrecken der Fachwelt gleich vollendete Tatsachen: In den Jahren 2009 und 2010 ließ seine Firma auf der nordwestlich von Jamaika gelegenen Karibikinsel Grand Cayman Millionen von gentechnisch veränderten Gelbfiebermücken frei. Davon erfuhren James und viele andere Experten erst 2010 auf einem Fachkongress in Atlanta – als die Studie auf den Kaimaninseln schon 14 Monate lief und Alphey sie vorstellte. Seitdem führte Oxitec Freisetzungen auch in Malaysia und in Brasilien durch.
Viele Fachkollegen erfuhren von der Freisetzung auf den Kaimaninseln erst, als die Studie schon 14 Monate lief
Fachleute fürchten, das forsche Vorpreschen könnte der gesamten Arbeit mit transgenen Insekten schaden und man würde Ähnliches erleben wie mit gentechnisch modifizierten Nutzpflanzen in Europa. Schlimmstenfalls würde die neue Technologie ausgebootet, bevor ihr Potenzial und mögliche Auswirkungen auf die Natur überhaupt ausgelotet sind. Denn obwohl der Ansatz bisher Erfolg versprechend aussieht und die Labortests günstig verliefen, erscheint es vielen Experten unbedingt geboten, das Verfahren zuerst unter freilandnahen, aber sicheren Bedingungen in den Tropen und Subtropen akribisch zu prüfen. Schließlich würden die transgenen Moskitos später einmal den Dschungel erobern. James zählt zu den Pionieren für Molekulargenetik von Stechmücken. Als einer der Ersten hatte er ein Moskitogen kloniert, also außerhalb des Insekts vervielfältigt, und Stechmücken gentechnisch manipuliert. Im Jahr 2001 beschloss er, dieses Spezialwissen zur Bekämpfung von durch Insekten übertragene Tropenkrankheiten einzusetzen. Er wollte versuchen, für Pflanzenschädlinge entwickelte Methoden bei Mücken zu verwenden, die für Menschen gefährlich sind.
Damals hatte Alphey, noch an der University of Oxford, bei Drosophila-Taufliegen ein Verfahren zur Erzeugung von transgenen Fliegen entwickelt, bei dem die Weibchen selektiv früh verenden. Letztlich handelt es sich dabei um eine moderne – gentechnologische – Version der jahrzehntealten, durchaus erfolgreichen Methode, Schadinsekten von Nutzpflanzen durch Aussetzen steriler Männchen zu dezimieren. Früher hat man Unmengen dieser Tiere im Labor herangezüchtet, die Männchen aussortiert und durch Bestrahlen unfruchtbar gemacht. Ließ man sie anschließend draußen in Überzahl auf die Weibchen los, verdrängten sie die fruchtbaren Männchen bei der Begattung. Oft brach der Bestand mangels Nachkommen schon nach wenigen Freisetzungen zusammen – was sich unter anderem 1977 in Tapachula gegen die Mittelmeerfruchtfliege (Ceratitis capitata) bewährte, einen bedeutenden Pflanzenschädling.
Für Stechmücken eignet sich solches Bestrahlen allerdings schlecht. Es schwächt die Männchen so sehr, dass sie schon beim Aussortieren oder spätestens auf dem Transport sterben. Doch Alpheys neue Methode ließ sich auf Moskitos übertragen. Hierbei wird eine Genomregion genutzt, die nur die Weibchen benötigen. Außerdem identifizierten James und Alphey 2002 einen genetischen Schalter für die Flugmuskelentwicklung. Sie zeigten, dass Weibchen, bei denen er abgestellt wird und die deswegen keine Flugmuskeln entwickeln, keine Männchen anlocken. Folglich sollten entsprechend ausgestattete Moskitoweibchen harmlos sein.
Um das Verfahren sowie weitere ähnlich aufgebaute Eingriffe kommerziell zu verwerten, gründete Alphey 2002 die Firma Oxitec. Als James 2005 von der Stiftung der amerikanischen National Institutes of Health – die weit gehend von der Bill & Melinda Gates Foundation getragen wird – für Tests gentechnischer Strategien zur Bekämpfung des Denguefiebers 20 Millionen US-Dollar bekam, reichte er 5 Millionen an Oxitec weiter, damit die Firma solche transgenen Moskitos konstruierte.
Angriff auf die Flugmuskeln mit einer Kaskade genetischer Schalter
Mitarbeiter entwarfen nun eine DNA-Kassette mit fünf Genen und zugehörigen regulatorischen Elementen, damit die neuen Gene jeweils zum gewünschten Zeitpunkt an- und abgeschaltet werden. Das System funktioniert als Kaskade: Während der Metamorphose von der Larve zur Mücke, also in der Puppe, aktiviert der geschlechtsspezifische Schalter bei den Weibchen das erste Gen. Daraufhin entsteht ein Protein, welches den Schalter für ein zweites Gen anwirft. Und dieses kodiert für ein Toxin, das die Flugmuskulatur zerstört. Damit die Forscher den Überblick behalten, ob die Tiere diese Gene aufweisen, fügten sie außerdem DNA-Sequenzen für rot und grün fluoreszierende Proteine hinzu.
Allerdings dürfen die transgenen Moskitoweibchen zunächst nicht gleich sterben, sondern müssen erst einmal Unmengen von Eiern legen, weil man viele transgene Männchen braucht. Der Trick ist, die Genkaskade über einen weiteren Schalter mittels eines "Gegengifts", in diesem Fall des Antibiotikums Tetracyclin, zu blockieren, das man dem Wasser zusetzt, in dem die Larven leben. Nun kann das Toxin nicht gebildet werden. Dies ist zudem eine Sicherheitsmaßnahme, damit womöglich doch freikommende transgene Moskitoweibchen keine reproduktionsfähigen weiblichen Nachkommen produzieren – unter natürlichen Bedingungen leben die Larven nicht in antibiotikahaltigem Wasser.
In weiten Teilen Mexikos, auch in Tapachula, gehört das Denguefieber seit Langem zu den gewichtigsten Gesundheitsgefahren. Fatal sind die geradezu explosionsartigen Ausbrüche, die sich in dicht besiedelten Gebieten besonders verheerend auswirken. 2009 und 2010 war zum Beispiel Tapachulas Vorort Pobres Unidos ("Vereinigte Arme") sehr stark heimgesucht. Der Epidemiologe Rogelio Danis-Lozano und die Parasitologin Janine Ramsey, die auf James’ Station die tägliche Arbeit leitet, zeigen mir das Armutsviertel.
Fast alle Häuser haben keine Vorderwand, so dass Moskitos frei hineinfliegen können. Der nasse Erdboden und die feuchte Luft im Innern ziehen die Insekten geradezu an. Überall gibt es Müllberge und vielerlei Behältnisse, wo sich Regenwasser sammelt – ideale Mückenbrutstätten. Danis- Lozano macht uns auf eine randvolle, große, gelbe Wanne aufmerksam. Darin schwimmen Unmassen dünner, schwarzer Würmchen zuckend umher. Die Besitzerin ahnt nicht, dass in ihrem Waschzuber Moskitolarven heranwachsen, obwohl sie das Denguefieber natürlich kennt.
Solche Verhältnisse sind typisch für viele Denguefiebergebiete der Welt. In über 100 tropischen und subtropischen Ländern Amerikas, Asiens und Afrikas ist die Krankheit verbreitet, und sie greift immer weiter um sich. Seit den 1970er Jahren hat sich die Zahl der Fälle alle zehn Jahre verdoppelt. Zum einen durch den wachsenden internationalen Reise und Warenverkehr, zum anderen, weil Menschen zunehmend in Ballungsgebiete ziehen, werden die Ausbrüche immer häufiger und heftiger. Das Denguefieber sei eine der aggressivsten wiederkehrenden Infektionskrankheiten, schrieben 2008 die amerikanischen Epidemiologen David M. Morens und Anthony S. Fauci vom National Institute of Allergy and Infectious Diseases in Bethesda (Maryland). Bei der hämorrhagischen Verlaufsform stirbt unbehandelt bis zu jeder Fünfte. Intensivmedizinische Maßnahmen können die Sterberate zwar auf ein Prozent senken, aber dieses Virus fordert dennoch weltweit mehr Todesopfer als die übrigen hämorrhagischen Viruserkrankungen zusammen, eingeschlossen das Ebola- und Marburgfieber.
Einer der Gründe, weswegen sich James dem Denguefieber zuwandte und nicht beispielsweise der Malaria, ist die Beteiligung nur sehr weniger Moskitoarten – während ungefähr drei Dutzend Mückenspezies den Malariaerreger weitergeben können. Die Gelbfiebermücke und Hauptüberträgerin stammt ursprünglich aus Afrika und war dort anscheinend früher ein Insekt in den Wäldern, das irgendwann den Menschen zu seinem Hauptwirt auserkor. Mit Sklavenschiffen gelangte das Tier schon vor rund 400 Jahren nach Amerika und breitete sich dort rasch aus. Heute vermehren sich diese Stechmücken als Kulturfolger in jeder kleinen Kuhle mit ein paar Schluck Wasser. Erwachsene Weibchen leben ungefähr einen Monat. Weil sie fast ausschließlich Menschen stechen, bleibt ihnen somit viel Zeit und Gelegenheit, das Virus mit einer Blutmahlzeit aufzunehmen und weiterzugeben.
Diese tagaktiven Moskitos fliegen so leise, dass ich von dem Schwarm in dem kleinen Anzuchtkäfig fast nichts höre, den mir die Entomologin Laura Valerio von der University of California in Davis zeigt. Wir sind in Tapachula im abgesicherten Insektarium des Gesundheitsforschungszentrums. Die Forscherin zieht einen Handschuh an, um in den Käfig hineinzulangen und auf eines der transgenen Weibchen zu deuten. Während die Männchen aufgescheucht umherschwirren, bleiben die Weibchen sitzen oder hüpfen höchstens träge ein kleines Stück weg – Resultat der zerstörten Flugmuskeln.
Von hier werden transgene Moskitolarven zur Feldversuchsstation gebracht. Dort gibt es fünf Käfigpaare: jeweils einen zur Kontrolle mit normalen Mücken der Region und einen, in dem sich normale und transgene Mücken begegnen. Um an die Gehege heranzukommen, müssen sich die Leute durch eine Anzahl dichter Netze vorarbeiten. Man möchte in jeder Hinsicht Fehler der Vergangenheit vermeiden.
Einst war es für Industrienationen vor allem bequem, ihre Studien mit gentechnisch veränderten Organismen in Entwicklungsländern durchzuführen. Mit der Zeit provozierte die nonchalante Haltung gegenüber der dortigen Umwelt allerdings Widerstand in der Bevölkerung, der ganze Forschungsprogramme scheitern ließ. Vielleicht erfährt kein Wissenschaftszweig mehr eingebildeten oder wirklichen Missbrauch als das Gebiet der transgenen Organismen.
Indien liefert dafür ein Beispiel. 1969 beschlossen die Weltgesundheitsorganisation WHO und die indische Regierung, gemeinsam Strategien zu erforschen, um drei wichtige Moskitoarten mit Hilfe von gentechnischer Manipulation zu kontrollieren. Ins Programm kamen eine Malariamücke, eine Culex-Mücke, die durch Fadenwürmer Lymphschwellungen – Elephantiasis – hervorruft und die Gelbfiebermücke. Zu den Geldgebern gehörte auch die US-Regierung.
1972 schrieb jemand anonym in der indischen Zeitung "National Herald", Forscher hätten in dörflichen Brunnen Mückenlarven ausgesetzt, die mit einem gebräuchlichen Krebsmittel behandelt worden waren, das bei Tieren Geburtsschäden und Krebs hervorruft. Die verantwortlichen Wissenschaftler verfassten eine Gegendarstellung, wollten allerdings keine Interviews geben. Zwei Jahre später brachte die indische Nachrichtenagentur Press Trust eine Meldung mit dem Titel "WHO betreibt in Indien Geheimforschung für die USA". Darin hieß es, in dem Moskitoprojekt würde die Eignung von Gelbfiebermücken zur biologischen Kriegsführung geprüft. Man teste Chemikalien und Methoden, die in den Geldgeberländern nicht erlaubt sind. Die Eier von Aedes aegypti könne man – im Gegensatz zu denen anderer Arten – getrocknet in einem Briefumschlag verschicken. Zwar wiesen die Forscher diese Anschuldigungen entschieden zurück. Doch das mediale Spektakel war so groß, dass die WHO das Programm schließlich aufgab.
Vielleicht erfährt kein Forschungszweig mehr eingebildeten oder wirklichen Missbrauch als das Gebiet der transgenen Organismen
Seitdem graut es vielen Wissenschaftlern vor Feldstudien mit gentechnisch veränderten Organismen, erklärt Stephanie James, Leiterin der Initiative Grand Challenges in Global Health von der Stiftung der National Institutes of Health – nicht verwandt mit Anthony James. "Die psychische Hürde war enorm. Man wusste, man durfte sich keinen Fehler leisten."
Auch Anthony James erzählt: "Alle meinten immer nur, es würde mir nie gelingen, eine Bevölkerung für mein Vorhaben zu gewinnen." Er suchte Rat bei einem Experten für Öffentlichkeitsarbeit: Jim Lavery, der am Center for Global Health Research am St. Michael’s Hospital in Toronto untersucht, wie man die Menschen bei Forschungsprojekten einbeziehen kann.
Laverys Empfehlung: eine Region wählen, die stark unter Denguefieber leidet und wo man das Problem trotz aller Anstrengungen bisher nicht in den Griff bekommt. Es sollte außerdem ein Land mit hoch entwickelten Strukturen und stringenten Vorschriften sein, dessen Behörden die Risiken und Vorteile solch eines Projekts abschätzen können. So müssten die Menschen nicht befürchten, dass man sie übervorteilt oder gefährdet. Mit Hilfe von Lavery und dem langjährigen Experten für Moskitofeldforschung Thomas Scott von der University of California in Davis brachte James nun ein international zusammengewürfeltes Team von Moskitoökologen, Anthropologen und Ethikern zusammen.
Erfolg mit Öffentlichkeitsarbeit
2006 erkoren die Forscher Tapachula zum Favoriten für eine Versuchsstation. Mexiko besaß Gesetze zu genetisch veränderten Organismen. Das Land hatte auch das Cartagena-Protokoll zur biologischen Sicherheit unterzeichnet – das seit 2003 gültige internationale Abkommen zum Umgang mit transgenen Organismen und auch deren Import. Und wegen der guten Erfahrungen in Tapachula mit der Ausrottung der Mittelmeerfruchtfliege würde die Bevölkerung beim Gedanken an ein gentechnisch manipuliertes Insekt nicht gleich in Panik geraten.
"Zuerst kam uns das komisch vor, dass diese Forscher Land haben wollten", erinnert sich Martimiano Barrios Matute, Vorsteher der betroffenen Gemeinde. Wieso wollte jemand große Käfige bauen, nur um eine Menge veränderte Mücken hineinzutun? Und was würde passieren, wenn einige davon freikämen? Könnten sie den Menschen oder ihren Feldern schaden? Oder würden dann auch andere Insekten steril?
James und seine Mitarbeiter redeten mit den Leuten, gingen auf die verschiedenen Bedenken ein und erklärten ihr Vorhaben so genau wie möglich. Informationsveranstaltungen finden weiterhin regelmäßig statt. Zu der wöchentlichen Versammlung im Kulturhaus von Tapachula, die ich besuche, haben sich etwa 30 Männer und 5 Frauen eingefunden, alle in verantwortlichen Positionen. Zunächst berichtet die Leiterin der Forschungsstation Janine Ramsey vom Stand der Versuche. Mit ihrer lebhaften, auch humorvollen Art, die so gar nicht mehr nordamerikanisch wirkt, scheint sie ihr Publikum zu fesseln. Später stellen die Leute zögernd Fragen. Ein Mann erkundigt sich, ob er die Käfige besichtigen darf. Ein anderer möchte wissen, was passieren würde, wenn Moskitos entweichen. Eine junge Frau fragt, wieso Menschen etwas gegen transgene Organismen haben. Einem älteren Mann aus einem Bergdorf ist der Unterschied zwischen Denguefieber und Malaria nicht klar. Ramsey antwortet jedem und gibt zum Abschied allen die Hand. "Wir verstehen das Projekt nun, und es gefällt uns", erklärt der Sojabauer Barrios Matute. "Das wird nicht nur Rio Florido nützen. Es kann für die ganze Gegend hier gut sein und für ganz Mexiko, überhaupt für viele Orte der Welt."
Völlig anders war Oxitec in der Karibik vorgegangen. Wie Luke Alphey auf der Jahrestagung der American Society of Tropical Medicine and Hygiene in Atlanta Ende 2010 dem überraschten Auditorium erzählte, hatten sie auf Grand Cayman die ersten genmanipulierten männlichen Gelbfiebermücken im September 2009 ausgesetzt und dann während des Sommerhalbjahrs 2010 nochmals über drei Millionen Männchen freigelassen. Laut Alphey schrumpfte die lokale Population daraufhin um 80 Prozent. Der verwendete Zuchtstamm funktioniert genetisch etwas anders als der in der Tapachula-Studie: Die im Freiland erzeugten Nachkommen sterben in beiden Geschlechtern schon als Larven und verbreiten sich deshalb nicht weiter.
Alphey verteidigt sich gegen Vorwürfe: Die Öffentlichkeitsarbeit möchte Oxitec bei seinen Projekten weit gehend den Regierungen überlassen. Die verstünden die kulturellen Empfindlichkeiten am besten. Auf Grand Cayman brachten lediglich die Abendnachrichten einen Fünfminutenbeitrag. Und es gab eine Broschüre, in der stand, die freigelassenen Moskitos seien steril – allerdings war darin keine Rede von genetischer Manipulation. Weder fanden öffentliche Informationsveranstaltungen statt noch bot man der Bevölkerung Gelegenheit, Bedenken zu äußern. Der Firmenchef sagte auf dem Kongress in Atlanta, man habe die Aktion zunächst nur auf den Kaimaninseln publik gemacht, denn nur deren Bewohner mussten davon wissen.
Einen Fürsprecher findet Alphey in dem Molekularbiologen Mark Q. Benedict von der Università degli Studi di Perugia (Italien), der selbst über sterile Insekten forscht und Berater der Bill & Melinda Gates Foundation ist. Oxitec habe keine Gesetze gebrochen. Die Kaimanstudie sei mutig gewesen, habe man doch eine Technologie geprüft, die im Guten wie im Schlechten Aufmerksamkeit erregen muss. Durch verwirrende und widersprüchliche Meldungen in den Medien sei der Eindruck entstanden, dass da ein einzelner Forscher unbekümmert einfach eimerweise Moskitos in die Gegend gekippt habe. So sei das aber nicht gewesen. Oxitec arbeite bei seinen Projekten mit den örtlichen und staatlichen Stellen zusammen und hole dort im Voraus für seine Versuche Genehmigungen ein.
Trotzdem löste Alpheys Vorstoß in der Öffentlichkeit, bei Umweltgruppen und bei vielen Kollegen Kritik, Argwohn und Enttäuschung aus. Bart Knols, Medizinentomologe an der Universität Amsterdam und geschäftsführender Direktor des Netzwerks MalariaWorld, bringt es auf den Punkt: Alle Welt frage sich, ob die Heimlichtuerei nötig war. Natürlich wecke das Misstrauen. Die Technologie selbst hält auch Knols für viel versprechend. Nur – wenn einer Mist baue und die Öffentlichkeit nicht richtig informiere, könne das auf andere Projekte mit transgenen Organismen zurückschlagen. "Wegen Oxitec bekommen wir jetzt womöglich die gleichen Problemewie die WHO 1976 in Indien." Außerdem argwöhnen manche Experten, dass sich Oxitec absichtlich Länder mit laxen Gesetzen aussucht. Laut Stephanie James war auf den Kaimaninseln ein Gesetzesentwurf zur biologischen Sicherheit gerade verabschiedet, das Gesetz aber noch nicht gültig.
Das Für und Wider der Freisetzung
Ebenfalls umstritten ist die Situation in Malaysia, wo Oxitec Ende 2010 in einer unbewohnten Gegend eine Feldstudie begann – unter dem Protest verschiedener Organisationen. Das Land verfügt zwar über einen Rat für biologische Sicherheit und seit Kurzem auch über Gesetze dazu. Doch es herrscht Skepsis, ob die nötige Expertise vorhanden ist, solche Versuche zu bewerten und zu überwachen. Auch im nordost-brasilianischen Bundesstaat Bahia, in einem armen Vorort von Juazeiro, nahm Oxitec 2011 einen halbjährigen Freisetzungsversuch in Angriff. Die Menschen dort sind das ganze Jahr über von Moskitos und Denguefieber geplagt. Auf Grand Cayman soll überdies das Potenzial der beiden hier beschriebenen transgenen Tigermückenstämme im Vergleich getestet werden – also mit dem schon auf der Insel erprobten und dem in Tapachula untersuchten –, um herauszufinden, welcher die günstigeren Eigenschaften hat. Interesse an der Methode meldeten mittlerweile Behördenvertreter von Panama und den Philippinen an sowie Verantwortliche von Florida, wo nach Jahrzehnten Denguefieber inzwischen wieder vorkommt.
Andererseits lehnen manche Interessengruppen das Freisetzen genmanipulierter Organismen grundsätzlich ab, selbst wenn die Forscher offen damit umgehen und alle Umsicht walten lassen. Die Wissenschaftlerin Janet Cotter von den Greenpeace-Forschungslaboren in Exeter (England) hält die Versuche von Oxitec für hochriskant. Denn es gäbe einfach keine 100-prozentige Sterilität. Allzu leicht würden unabsichtlich auch ein paar transgene reproduktionsfähige Weibchen mit frei gelassen – mit unabsehbaren Folgen.
Manche fragen sich sogar, ob es ethisch und ökologisch vertretbar ist, einen Organismus gezielt auszulöschen, und sei es nur in einem kleinen Gebiet. Die Befürworter des Vorhabens argumentieren, die Gelbfiebermücke im Umfeld menschlicher Besiedlung sei eine invasive Form mit Spezialisierung auf diese Nische und den Menschen. Laut Phil Lounibos, Moskitoökologe am Florida Medical Entomology Laboratory, gehört die urbane Form zu keiner wichtigen natürlichen Nahrungskette. Trotzdem kann er sich nicht vorstellen, dass man das Denguefieber mit solchen Vernichtungsaktionen endgültig ausrotten wird. Einerseits gab es auf dem amerikanischen Kontinent in den 1950er und 1960er Jahren schon einmal eine derartige Kampagne, damals gegen urbanes Gelbfieber, und die scheiterte kläglich. Außerdem dringt die verwandte Asiatische Tigermücke (Stegomyia albopicta oder Aedes albopictus) bereitwillig in die frei werdenden Nischen vor – auch sie eine häufige Überträgerin von Dengueviren. Aber vor allem halten sich die transgenen Mücken nicht ewig. Dann könnten sich von Randgebieten her erneut Moskitos ausbreiten. Man müsste also immer wieder veränderte Mückenmännchen freisetzen.
Deswegen beschäftigen sich James und viele seiner Kollegen auch damit, den Moskitopopulationen dauerhaft Resistenzgene gegen den Krankheitserreger aufzuzwingen. Derart manipulierte Mücken würden das Denguevirus nicht mehr übertragen. Zu diesem Zweck möchten Forscher verschiedene natürliche Genverbreitungsmechanismen nutzen. Damit ausgestattete Moskitos würden die neue Eigenschaft in die Population einbringen, wo sie mit der Zeit zunehmend um sich griffe. Bis zu ersten Feldversuchen gegen einen der Serotypen des Denguevirus dürften aber mindestens noch einige Jahre verstreichen.

Wenn Sie inhaltliche Anmerkungen zu diesem Artikel haben, können Sie die Redaktion per E-Mail informieren. Wir lesen Ihre Zuschrift, bitten jedoch um Verständnis, dass wir nicht jede beantworten können.