Physikalische Chemie: Neues Licht für katalysierte Reaktionen
Manche Prozesse kommen ohne fremde Hilfe nie in Gang. Chemische Reaktionen starten beispielsweise oft nur in Anwesenheit des passenden Katalysators. Doch der ist mitunter schwierig zu finden. Vielleicht könnte der Einsatz von Lasern die Schwierigkeiten im Labor beenden. Ihr Licht soll Molekülen auf den richtigen Weg helfen.
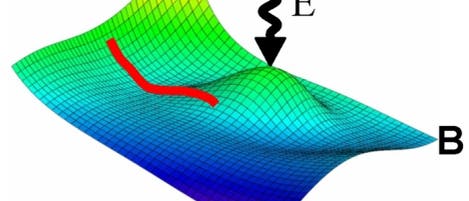
© Albert Stolow (Ausschnitt)
Eigenlich ist Chemie nicht mehr (und nicht weniger) als die Kunst, mit einem Baukasten voller unsichtbar kleiner Steinchen die verschiedensten Dinge zu zaubern. Weil sich jedoch längst nicht jede Art von Steinchen mit jeder anderen kombinieren lässt und weil dabei mitunter völlig unerwartete Sachen passieren, haben Generationen von Wissenschaftlern in mühevoller Kleinarbeit die Regeln ergründet, nach denen X mit Y, nicht aber mit Z reagiert.
Auf einen kurzen Nenner gebracht stellte sich heraus, dass die gesamte Chemie der unzähligen Substanzen eigentlich nur eine Frage von elektrischen Kräften ist. Letztlich sind es in allen Atomen, Molekülen und Kristallen die Anziehungskräfte zwischen Elektronen und Atomkernen sowie die Abstoßungen zwischen Elektronen, die bestimmen, das Wasser H2O ist und Kohlenstoff im Verein mit Wasserstoff, Phosphor, Stickstoff und Sauerstoff das langfädige Erbmolekül DNA bildet.
Elektrische Kräfte und die zugehörigen Felder sind aber auch – und vor allem – in der Physik alte Bekannte. Im modernen Gewand des Lasers haben sie längst Einzug in jedes Labor gehalten und manipulieren äußerst erfolgreich die Welt des Mikro- und Nanokosmos. Was liegt da näher, als die bunte Vielfalt der Chemie mit den gestrengen Feldern der Laser zu ordnen und zu regeln?
Zumal die Chemie seit Ewigkeiten vor dem Problem steht, dass es für gewöhnlich unzureichend ist, die richtigen Zutaten miteinander zu mixen, um ein gewünschtes Produkt zu erhalten. Entweder passiert dabei überhaupt nichts, oder die Reaktionen schlagen eine Richtung ein, die dem Experimentator reichlich unlieb ist. Es sei denn, er verfügt über den passenden Katalysator – eine Substanz, die den Ausgangsstoffen ein elektrisches Umfeld bietet, in dem sie gerne tun, was ihnen ohne fremde Hilfe nicht oder zumindest kaum möglich wäre.
Dummerweise sind stoffliche Katalysatoren schwierig zu finden. Was wem wie auf welche Sprünge hilft, sehen selbst gestandene Chemiker den Formeln nicht immer an. Und so träumen manche von einem universellen Katalysator aus Licht. Vom Laser, der auf unkomplizierte Weise Reaktionen in die gewünschten Bahnen lenkt.
Diesen Traum glauben nun Physikochemiker um Benjamin Sussman vom kanadischen Steacie Institute for Molecular Sciences in Ottawa ansatzweise erfüllen zu können. Zwar in ziemlich bescheidenen Ansätzen, doch im Prinzip beliebig erweiterbar.
Das Ziel ihrer Pionierexperimente bestand darin, Jodbromid-Moleküle, die aus einem Jod- und einem Brom-Atom bestehen, so zu spalten, dass sie in einem von zwei möglichen Endzuständen landeten: Entweder nahmen beide Elemente ihren energetischen Grundzustand ein, oder das Brom war angeregt, was für chemische Folgereaktionen einen erheblichen Unterschied machen würde. Damit aber überhaupt etwas passierte, versetzten die Wissenschaftler zunächst einmal das intakte Molekül mit einem grünen Laser in einen instabilen Zustand. Blieb die Probe sodann sich selbst überlassen, zerfiel sie in neutrales Jod und Brom, von dem fast 80 Prozent angeregt waren.
Um dieses Verhältnis von angeregtem zu entspanntem Brom zu verschieben, beschossen die Forscher die laufende Reaktion mit einem zweiten Laserstrahl, diesmal mit infrarotem Licht. Dessen Energie reicht nicht aus, um die elektronischen Zustände der Atome selbst zu ändern.
Stattdessen veränderte sein elektrisches Feld über den so genannten dynamischen Stark-Effekt die Bedingungen für den weiteren Reaktionsverlauf. In Anwesenheit des Feldes waren bestimmte Übergangszustände energetisch nicht mehr so günstig wie im ungestörten Vergleich. Bildlich gesprochen haben Sussman und seine Kollegen mit dem Laser die Reaktionslandschaft mit neuen Hügeln und Tälern versehen.
Der Eingriff war erfolgreich. Je nachdem, wann der infrarote Laser einschlug, verschob er das Verhältnis der Bromzustände auf die angeregte Seite oder jene des Grundzustands. Bis zu 60 Prozent konnte diese Manipulation ausmachen. Kein absolut reines Ergebnis, dafür aber eine universelle Vorgehensweise. Da das Laserlicht die Reaktanden nicht direkt anregt, sondern mehr die Reaktionslandschaft verändert, sollte die Methode auch für andere chemische Umsätze nutzbar sein.
Abhängig vom Zeitpunkt, wann der Blitz einschlägt, kann er den weiteren Verlauf in unterschiedliche Bahnen lenken. Nun muss der Laser nur noch mit der schillernden Vielfalt des chemischen Baukastens zurechtkommen. Vielleicht gehört ihm dann schon bald ein Stammplatz im Labor – neben Reagenzglas und Bunsenbrenner.
Auf einen kurzen Nenner gebracht stellte sich heraus, dass die gesamte Chemie der unzähligen Substanzen eigentlich nur eine Frage von elektrischen Kräften ist. Letztlich sind es in allen Atomen, Molekülen und Kristallen die Anziehungskräfte zwischen Elektronen und Atomkernen sowie die Abstoßungen zwischen Elektronen, die bestimmen, das Wasser H2O ist und Kohlenstoff im Verein mit Wasserstoff, Phosphor, Stickstoff und Sauerstoff das langfädige Erbmolekül DNA bildet.
Elektrische Kräfte und die zugehörigen Felder sind aber auch – und vor allem – in der Physik alte Bekannte. Im modernen Gewand des Lasers haben sie längst Einzug in jedes Labor gehalten und manipulieren äußerst erfolgreich die Welt des Mikro- und Nanokosmos. Was liegt da näher, als die bunte Vielfalt der Chemie mit den gestrengen Feldern der Laser zu ordnen und zu regeln?
Zumal die Chemie seit Ewigkeiten vor dem Problem steht, dass es für gewöhnlich unzureichend ist, die richtigen Zutaten miteinander zu mixen, um ein gewünschtes Produkt zu erhalten. Entweder passiert dabei überhaupt nichts, oder die Reaktionen schlagen eine Richtung ein, die dem Experimentator reichlich unlieb ist. Es sei denn, er verfügt über den passenden Katalysator – eine Substanz, die den Ausgangsstoffen ein elektrisches Umfeld bietet, in dem sie gerne tun, was ihnen ohne fremde Hilfe nicht oder zumindest kaum möglich wäre.
Dummerweise sind stoffliche Katalysatoren schwierig zu finden. Was wem wie auf welche Sprünge hilft, sehen selbst gestandene Chemiker den Formeln nicht immer an. Und so träumen manche von einem universellen Katalysator aus Licht. Vom Laser, der auf unkomplizierte Weise Reaktionen in die gewünschten Bahnen lenkt.
Diesen Traum glauben nun Physikochemiker um Benjamin Sussman vom kanadischen Steacie Institute for Molecular Sciences in Ottawa ansatzweise erfüllen zu können. Zwar in ziemlich bescheidenen Ansätzen, doch im Prinzip beliebig erweiterbar.
Das Ziel ihrer Pionierexperimente bestand darin, Jodbromid-Moleküle, die aus einem Jod- und einem Brom-Atom bestehen, so zu spalten, dass sie in einem von zwei möglichen Endzuständen landeten: Entweder nahmen beide Elemente ihren energetischen Grundzustand ein, oder das Brom war angeregt, was für chemische Folgereaktionen einen erheblichen Unterschied machen würde. Damit aber überhaupt etwas passierte, versetzten die Wissenschaftler zunächst einmal das intakte Molekül mit einem grünen Laser in einen instabilen Zustand. Blieb die Probe sodann sich selbst überlassen, zerfiel sie in neutrales Jod und Brom, von dem fast 80 Prozent angeregt waren.
Um dieses Verhältnis von angeregtem zu entspanntem Brom zu verschieben, beschossen die Forscher die laufende Reaktion mit einem zweiten Laserstrahl, diesmal mit infrarotem Licht. Dessen Energie reicht nicht aus, um die elektronischen Zustände der Atome selbst zu ändern.
Stattdessen veränderte sein elektrisches Feld über den so genannten dynamischen Stark-Effekt die Bedingungen für den weiteren Reaktionsverlauf. In Anwesenheit des Feldes waren bestimmte Übergangszustände energetisch nicht mehr so günstig wie im ungestörten Vergleich. Bildlich gesprochen haben Sussman und seine Kollegen mit dem Laser die Reaktionslandschaft mit neuen Hügeln und Tälern versehen.
Der Eingriff war erfolgreich. Je nachdem, wann der infrarote Laser einschlug, verschob er das Verhältnis der Bromzustände auf die angeregte Seite oder jene des Grundzustands. Bis zu 60 Prozent konnte diese Manipulation ausmachen. Kein absolut reines Ergebnis, dafür aber eine universelle Vorgehensweise. Da das Laserlicht die Reaktanden nicht direkt anregt, sondern mehr die Reaktionslandschaft verändert, sollte die Methode auch für andere chemische Umsätze nutzbar sein.
Abhängig vom Zeitpunkt, wann der Blitz einschlägt, kann er den weiteren Verlauf in unterschiedliche Bahnen lenken. Nun muss der Laser nur noch mit der schillernden Vielfalt des chemischen Baukastens zurechtkommen. Vielleicht gehört ihm dann schon bald ein Stammplatz im Labor – neben Reagenzglas und Bunsenbrenner.

Wenn Sie inhaltliche Anmerkungen zu diesem Artikel haben, können Sie die Redaktion per E-Mail informieren. Wir lesen Ihre Zuschrift, bitten jedoch um Verständnis, dass wir nicht jede beantworten können.