Genregulation: Schnelle Einsatztruppe für den Notfall
Die Messenger-RNA übernimmt, wie schon der Name sagt, Botenfunktion: Sie trägt die genetische Information der DNA aus dem Zellkern ins Zellplasma, wo sie schließlich die Proteinsynthese ankurbelt. Doch warum nur vertrödelt so manche mRNA ihre Zeit im Zellkern, anstatt auf Dienstreise zu gehen?
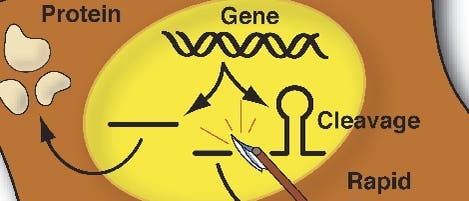
© Cold Spring Harbor Laboratory (Ausschnitt)
Das Leben ist ein einziges Reagieren auf veränderte Bedingungen. Steht beim sonntäglichen Ausflug plötzlich ein Wildschwein vor dem arglos flanierenden Spaziergänger, schaltet dessen Körper schlagartig von gedankenverlorenem Dahinwandeln auf sofortige Bereitschaft zur Flucht um. Doch nicht nur äußere Veränderungen, sondern auch innere fordern Reaktionen: Liegt das Frühstück schon einige Stunden zurück, melden Hormone ans Gehirn, dass dringender Nachfüllbedarf besteht und der Ausflügler doch schleunigst Ausschau nach einem netten Wanderlokal halten sollte.
Um angemessen auf derartige externe und interne Anforderungen reagieren zu können, greifen die entsprechenden Körperzellen auf ihre genetische Ausstattung zurück und schalten die benötigten Gene bedarfsgerecht an oder aus. Beim Anknipsen eines aktuell benötigten Erbfaktors setzten sie die Transkriptionsmaschinerie in Gang: Die Gene auf der DNA werden abgelesen und deren Information auf Boten-RNA (mRNA) übertragen. Diese transportiert die Botschaft aus dem Zellkern ins Zellplasma und kurbelt dort die Produktion der benötigten Proteine an.
Nun gibt es aber auch mRNA-Typen, die statt ins Zellplasma zu wandern im Zellkern verweilen und dort so genannte Kernflecken (nuclear speckles) bilden. Kaum vorstellbar, dass die Natur so verschwenderisch sein sollte, die aufwändige Transskription zu betreiben, nur um einen Haufen nutzlos herumlungernder mRNA-Moleküle zu produzieren. Welche unentdeckte Funktion hat also diese im Zellkern verbleibende mRNA?
Das Interesse der Forscher weckte aber vor allem die Funktion des mCAT2-Oberflächenproteins: Es synthetisiert in Stress-Situationen, wie sie beispielsweise Virusinfektionen oder die Wundheilung verursachen, Stickstoffoxid. Sollte die CTN-RNA womöglich als stille Reserve dienen und in Notsituationen eine schnelle Reaktion ermöglichen?
Um diese Frage zu beantworten, gaukelte nun das Team um Prasanth Mäusezellen eine Stress-Situation vor, indem es die Zellen mit Interferon behandelte. Und tatsächlich: Unter Stress wurde der im Zellkern herumlungernden CTN-RNA ihr langes Schwänzchen, das sie von der mCAT2-mRNA unterscheidet, abgeschnitten. Der funktionelle Teil wanderte daraufhin ins Zellplasma, wo er die Produktion des benötigten Proteins in Gang setzte. Gleichzeitig produzierte der Zellkern – wie auch unter stressfreien Bedingungen – weiterhin die mCAT2-mRNA.
Die CTN-RNA ist demnach quasi als schnelle Einsatztruppe im Zellkern stationiert. Bei Stress wird sie umgehend aktiviert und ermöglicht so der Zelle eine schnelle Reaktion auf gefährliche oder belastende Situationen. Nun gilt es noch herauszufinden, ob dieser Mechanismus ein Einzelfall ist oder ob er als generelles Prinzip für Notsituationen auch bei anderen Genen zum Einsatz kommt.
Um angemessen auf derartige externe und interne Anforderungen reagieren zu können, greifen die entsprechenden Körperzellen auf ihre genetische Ausstattung zurück und schalten die benötigten Gene bedarfsgerecht an oder aus. Beim Anknipsen eines aktuell benötigten Erbfaktors setzten sie die Transkriptionsmaschinerie in Gang: Die Gene auf der DNA werden abgelesen und deren Information auf Boten-RNA (mRNA) übertragen. Diese transportiert die Botschaft aus dem Zellkern ins Zellplasma und kurbelt dort die Produktion der benötigten Proteine an.
Nun gibt es aber auch mRNA-Typen, die statt ins Zellplasma zu wandern im Zellkern verweilen und dort so genannte Kernflecken (nuclear speckles) bilden. Kaum vorstellbar, dass die Natur so verschwenderisch sein sollte, die aufwändige Transskription zu betreiben, nur um einen Haufen nutzlos herumlungernder mRNA-Moleküle zu produzieren. Welche unentdeckte Funktion hat also diese im Zellkern verbleibende mRNA?
"Dieser 'cut-and-run'-Mechanismus ist ein ganz neues Muster der Genregulation"
(David Spector)
Die Aufgabe der im Zellkern verweilenden mRNA des Mausgens mCAT2 entschlüsselte nun das Team um Kannanganattu Prasanth unter der Leitung von David Spector vom Cold Spring Harbor Laboratory. Die Arbeitsgruppe war auf dieses Gen aufmerksam geworden, weil es zwei Typen von mRNA produziert: Zum einen in geringerer Menge die "normale" mRNA (mCAT2-mRNA), die ins Zellplasma gelangt und dort die Produktion eines Oberflächenproteins ankurbelt. Zum anderen entsteht in größerem Maßstab eine längere Version, die CTN-RNA (CAT2 transcribed nuclear RNA), die im Zellkern verbleibt. (David Spector)
Das Interesse der Forscher weckte aber vor allem die Funktion des mCAT2-Oberflächenproteins: Es synthetisiert in Stress-Situationen, wie sie beispielsweise Virusinfektionen oder die Wundheilung verursachen, Stickstoffoxid. Sollte die CTN-RNA womöglich als stille Reserve dienen und in Notsituationen eine schnelle Reaktion ermöglichen?
Um diese Frage zu beantworten, gaukelte nun das Team um Prasanth Mäusezellen eine Stress-Situation vor, indem es die Zellen mit Interferon behandelte. Und tatsächlich: Unter Stress wurde der im Zellkern herumlungernden CTN-RNA ihr langes Schwänzchen, das sie von der mCAT2-mRNA unterscheidet, abgeschnitten. Der funktionelle Teil wanderte daraufhin ins Zellplasma, wo er die Produktion des benötigten Proteins in Gang setzte. Gleichzeitig produzierte der Zellkern – wie auch unter stressfreien Bedingungen – weiterhin die mCAT2-mRNA.
Die CTN-RNA ist demnach quasi als schnelle Einsatztruppe im Zellkern stationiert. Bei Stress wird sie umgehend aktiviert und ermöglicht so der Zelle eine schnelle Reaktion auf gefährliche oder belastende Situationen. Nun gilt es noch herauszufinden, ob dieser Mechanismus ein Einzelfall ist oder ob er als generelles Prinzip für Notsituationen auch bei anderen Genen zum Einsatz kommt.

Wenn Sie inhaltliche Anmerkungen zu diesem Artikel haben, können Sie die Redaktion per E-Mail informieren. Wir lesen Ihre Zuschrift, bitten jedoch um Verständnis, dass wir nicht jede beantworten können.